Alina Kabata-Pendias
A. KABATA-PENDIAS es Profesora de Geoquímica del Instituto de Cultivos y Ciencia de los Suelos de Pulawy, Polonia, y del Instituto Geológico de Varsovia. Es coautora de un libro de próxima aparición, titulado Trace elements in soils and plants.
Se necesita aún una labor considerable para que el hombre llegue a tener una idea más clara de los complejos procesos que derivan de los daños producidos a la biosfera por la contaminación. Se precisan demostraciones convincentes de que las tensiones ambientales contribuyen mucho al retraso, tanto cuantitativo como cualitativo, de los árboles y plantas naturales y cultivados. La toma de conciencia de este problema deberá contribuir a establecer una relación adecuada entre la industria y la agricultura, por una parte, y las necesidades de la biosfera por la otra.
Las características químicas y físicas de la biosfera son determinadas por las propiedades de elementos básicos como el clima y el suelo. También tienen importancia la litosfera - parte inferior de la atmósfera - y la hidrosfera, que incluye todas las masas de agua además de todo el vapor de agua existente en la atmósfera.
INVESTIGACIÓN DE LA CONTAMINACIÓN QUÍMICA EN INDIA. La industrialización ya causa problemas
Los árboles y las plantas son muy sensibles a los daños que provocan los contaminantes químicos, daños que no son fáciles de predecir. Entre el aire, el agua y el suelo hay una acción recíproca y compleja, y los efectos de los productos químicos dependen del tipo de cubierta vegetal, las condiciones atmosféricas y los tipos de suelo. El control de los contaminantes químicos y de sus efectos requiere no so o mas conocimientos, sino una cooperación y planificación internacional mayores.
Las características químicas de la biosfera, y especialmente de los organismos biológicos, se han ido adaptando por evolución durante un largo periodo geológico. Las concentraciones de elementos en la biosfera están generalmente relacionadas con su abundancia en la corteza terrestre.
El hombre, elemento integrante de la biosfera, no se adapta biológicamente a su ambiente como otros organismos, sino mediante cambios tecnológicos y culturales. La influencia del hombre en la biosfera ha sido muy amplia y compleja, y con frecuencia ha conducido a cambios irreversibles.
Mientras las modificaciones geológicas y biológicas de la superficie terrestre han sido muy lentas, los cambios introducidos y/o estimulados por el hombre se han acumulado con extremada rapidez en años recientes. Todos los cambios introducidos por el hombre perturban el equilibrio natural de cada ecosistema formado a lo largo del tiempo mediante el cambio evolutivo. Estos cambios han conducido muy a menudo a una degradación del ambiente natural. El fomento de actividades agropecuarias, por ejemplo, ha convertido varios ecosistemas en agroecosistemas artificiales. Aunque la influencia del hombre sobre la biosfera data del período neolítico, el problema del deterioro de los ecosistemas por la contaminación ha aumentado a un ritmo alarmante durante los dos últimos decenios.
La contaminación ambiental, especialmente la debida a productos químicos, es uno de los factores más potentes de destrucción de los componentes de la biosfera. De todos los contaminantes químicos, se considera que el dióxido de azufre (SO2), los complejos oxidantes (O3, NO2 y PAN, peroxiacetilnitratos), los hidrocarburos y los oligoelementos son los más importantes del punto de vista ecológico, biológico y sanitario. Además, todo compuesto químico producido como residuo industrial o urbano puede crear perturbaciones ambientales en la biosfera.
La industrialización y las emigraciones de zonas rurales a centros urbanos han dado lugar a concentraciones anormales de contaminantes químicos, al haberse centralizado mucho las necesidades energéticas. Sin embargo, las concentraciones de contaminantes químicos no suelen permanecer localizadas, sino que con frecuencia se difunden mucho e incluso atraviesan fronteras nacionales o continentales.
El consumo energético y de minerales por parte del hombre es la causa principal de la contaminación química de la biosfera. Una estimación de la descarga total de elementos químicos contaminantes al ambiente puede basarse en el consumo y la demanda de energía y minerales en el mundo que, como se sabe, han aumentado rápidamente en los últimos años. Todavía no hay nociones claras sobre el transporte, tiempo de permanencia, destino y efectos a largo plazo de los contaminantes en cada ecosistema específico, pero el número y el alcance de las investigaciones sobre las propiedades y las interacciones ambientales de los productos químicos han aumentado a un ritmo sostenido en los dos últimos decenios.
En esta etapa en que aumenta la comprensión de la agresión química a la biosfera, las características generales de los contaminantes químicos pueden resumirse como sigue:
· amplia dispersión y transporte por el aire a larga distancia;
· fijación rápida en fracciones minerales y orgánicas del agua;
· larga permanencia de la mayoría de los contaminantes en la superficie del suelo;
· deposición en la superficie de las plantas, con la consiguiente reducción de su capacidad de absorción de luz solar;
· acumulación biológica que muy a menudo altera la composición química de las plantas sin causar daños visibles
· perturbación de los procesos metabólicos de los tejidos vivos;
· resistencia a la detoxificación metabólica, y consiguiente entrada en la cadena alimentaria;
· reacción con los componentes del suelo, lo que provoca cambios en el pH y degradación.
«La deposición de ácidos por las lluvias fue tres veces superior en terrenos cubiertos de pinos que en terreno abierto; en terrenos cubiertos de abetos fue aproximadamente 1,5 veces superior, y en terrenos con abedules fue más baja que en terreno abierto.»
La mayor parte de la contaminación del aire se debe a la combustión de carbón y otros combustibles fósiles, así como a la fundición del hierro y de metales no ferrosos; sin embargo, los hornillos domésticos, la combustión de leña y los incendios forestales también contribuyen mucho a la contaminación local. Los desechos de las actividades humanas no son los únicos factores de la contaminación general del aire; también deben tenerse en cuenta algunas fuentes naturales como el polvo producido por la erosión eólica, las erupciones volcánicas y la evaporación de las superficies de agua.
La contaminación del aire es una importante fuente de contaminación del agua y del suelo. En muchos países la contaminación del agua causada por agentes anemófilos, aguas residuales y aguas negras, provoca la muerte de los organismos vivos de pequeñas cuencas hidrográficas; este problema está también muy vinculado con los recursos de agua potable. La mayor parte de los elementos químicos, especialmente los oligometales, no se encuentran en el agua en forma soluble, sino sobre todo como coloides en suspensión, o fijados en las sustancias orgánicas y minerales. Con el tiempo, tienden a concentrarse en los sedimentos del fondo marino y en el plancton. Sin embargo, los elementos volátiles (yodo, bromo) y los elementos fácilmente alkilizados por los microorganismos (mercurio, selenio, arsénico) se movilizan y pueden evaporarse en la superficie del agua.
Los sedimentos contaminados del fondo marino pueden constituir una importante fuente de contaminación del suelo. El suelo es el componente más específico de la biosfera, porque actúa no sólo como vertedero geoquímico de los contaminantes, sino también como compensador natural que controla el transporte (ciclaje) de elementos y sustancias químicas a la atmósfera, la hidrosfera y la biota.
Todos los contaminantes químicos, de cualquier proveniencia, acaban por llegar a la superficie terrestre, y su acción futura dependerá de las propiedades químicas y físicas del suelo que los recibe. Los contaminantes aniónicos como el dióxido y el fluoruro de azufre, afectan negativamente a varias propiedades de los suelos, se lixivien con relativa facilidad a través del suelo, y penetran en las aguas subterráneas. La persistencia en el suelo de los contaminantes catiónicos, y especialmente de los metales pesados, es mucho mayor que en otros componentes de la biosfera. Los metales acumulados en la superficie del suelo se reducen lentamente mediante la lixiviación, el consumo por las plantas, la erosión y la deflación. Los suelos contaminados con algunos metales pesados (zinc, cadmio, plomo) pueden tardar de varios decenios a varios miles de años en reducir el volumen de metal a un 50% (Kitagishi y Yamane, 1981).
La presencia en el suelo de oligocontaminantes se debe a los fertilizantes, a los plaguicidas y a los materiales transportados por las aguas residuales y por el aire. Las fuentes industriales y agropecuarias de metales pesados acrecen la concentración natural de éstos en la superficie de los suelos.
Las plantas son buenos indicadores de la composición química y del estado físico del suelo; si el suelo presenta desequilibrios naturales o debidos al exceso de cultivos o a contaminaciones de diverso tipo, las plantas lo indicarán con cambios de apariencia, de composición química y de funciones bioquímicas.
La contaminación del suelo ha llegado a ser relativamente común en todo el mundo, y probablemente aumentará. A menudo se advierte que los suelos están afectados simultáneamente por varios contaminantes químicos (dióxido de azufre, dióxido de nitrógeno, fluoruro de hidrógeno) muchas veces acompañados por precipitación ácida. La posible interacción sinérgica entre estos contaminantes del suelo complica enormemente su repercusión en la biosfera.
... Y EN RÍO DE JANEIRO... la lluvia ácida no necesita pasaportes para cruzar las fronteras
A nivel mundial, los óxidos de azufre en particular SO2 - son los contaminantes más destructivos de la vegetación y del suelo, además de los productos de la actividad del hombre, entre ellos los edificios. Se considera que sólo una tercera parte de los óxidos de azufre de la atmósfera derivan de la actividad humana (Taylor, 1980). Las emisiones de SO2 se oxidan fácilmente en la atmósfera para formar SO3, que reacciona con el vapor de agua atmosférico (H2O) y forma el ácido sulfúrico (SO4H2), causante de la precipitación ácida (lluvia ácida) que provoca graves daños tanto a la vegetación como al suelo.
La distribución de las emisiones de azufre por regiones varía mucho. En los países europeos se calcula que es de menos de una a más de 30 toneladas de SO2/km2/año. A pesar de los muchos estudios realizados, todavía no se conocen bien los efectos de la precipitación ácida, de la caída de azufre seco en suspensión y del SO2 gaseoso en la vegetación. Sin embargo, puede decirse que los complejos efectos directos e indirectos de la contaminación debida al dióxido de azufre en los suelos, dependen de factores climáticos, de la capacidad de compensación del suelo y de la tolerancia de la planta.
Aunque un ligero aumento de la acidez de los suelos puede estimular la presencia de nutrientes, y con ello la capacidad productiva, la precipitación ácida también provoca el desplazamiento y lixiviación de varios nutrientes. La acidez excesiva de los suelos puede producir como efectos secundarios niveles tóxicos de aluminio, manganeso y otros metales que las plantas absorben fácilmente (Hutchinson y Collins, 1978). A menudo, la actividad biológica del suelo acidificado se inhibe, ya que la mayor parte de los microorganismos prospera en suelos neutros.
AGUAS NEGRAS AFLUYEN AL TÍBER, desde que Tarquinio Prisco construyó la Cloaca Maxima
Las consecuencias ecológicas de la precipitación ácida son más graves en los suelos ligeramente ácidos y de escasa capacidad de compensación de las regiones templada y boreal, donde incluso una pequeña acidificación puede ocasionar una gran pérdida de productividad. La precipitación del azufre en suspensión tiene efectos destructivos sobre el suelo de las regiones áridas y semiáridas, donde un aumento de las sales en el mantillo puede limitar mucho la fertilidad.
El tipo de suelo determina la susceptibilidad del ecosistema a la precipitación ácida, que puede ser neutralizada con sales alcalinas, intercambiada por cationes (iones con carga positiva), o lixiviada a través del suelo para penetrar en los sistemas acuáticos.
En general, es más probable que los suelos de las regiones templadas eliminen los aniones de SO4, mientras que los suelos de las regiones tropicales muestran una capacidad de adsorción mucho mayor del SO4 debido a su contenido más elevado de sesquióxidos.
Como es sabido, la vegetación, y en particular la cubierta forestal, altera las precipitaciones. Los resultados dependen mucho del árbol predominante en esa cubierta. Por ejemplo, la deposición de ácidos por las precipitaciones fue tres veces superior en terrenos cubiertos de pinos que en terreno abierto; en terrenos cubiertos de abetos fue aproximadamente 1,5 veces superior, y en terrenos con abedules fue más baja que en terreno abierto (Bjor, Horntvedt y Joranger, 1974).
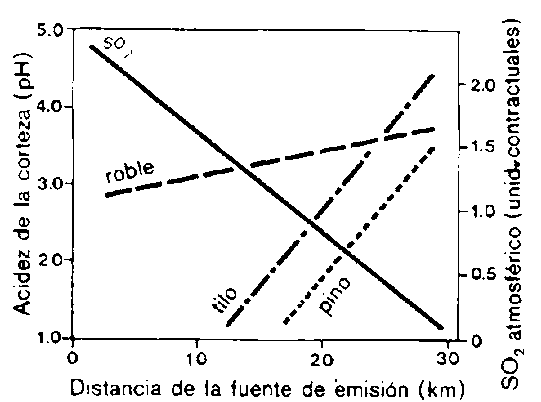
El agua de lluvia que corre por la superficie de las plantas tiene una mayor concentración de elementos debido al lavado o lixiviación de iones del follaje. Como consecuencia, aumenta la acidez en la superficie de las plantas, por ejemplo, en la corteza de los árboles (Fig. 1). Los efectos directos de la precipitación ácida sobre la vegetación son:
· daños en la estructura superficial protectora;· perturbación del intercambio gaseoso y de los procesos metabólicos de crecimiento;
· envenenamiento de las células vegetales, que provoca lesiones necróticas;
· alteración de los procesos de exudación de las hojas y las raíces, que afecta a las poblaciones de microorganismos asociadas a ellas;
· interacción sinérgica con otras tensiones ambientales.
Uno de los efectos más frecuentes de la precipitación ácida es la reducción de la productividad de ecosistemas naturales no ordenados, como los bosques. Las prácticas agrícolas normales no sufren los efectos destructores de la deposición del azufre, si la precipitación ácida no afecta directamente la vegetación, o bien si los suelos tienen suficientes nutrientes para las plantas.
Se atribuyen a la lluvia ácida diversos tipos de daños a la biosfera; por ejemplo, la destrucción de vastas zonas de perennifolias, la reducción del abeto rojo en las montañas, y la moría de peces en lagos acidificados (Bengley y LaBreoque, 1982). Sin embargo, no se pueden predecir los efectos ecológicos a largo plazo de las emisiones antropogénicas de azufre, que siguen a ritmo creciente.
ASPERSIÓN DE UN TRIGAL EN MONGOLIA EXTERIOR...
... Y DE UN ARROZAL EN LIBERIA. Fertilizantes y plaguicidas depositan oligoelementos en el suelo
En los últimos tiempos se reconoce siempre más la importancia de los oligocontaminantes inorgánicos. Los oligoelementos ya no se consideran sólo como un problema de micronutrientes.
En la materia viva hay muchos oligoelementos en concentraciones inferiores al 0,1%. Algunos de ellos, sobre todo micronutrientes o microelementos (aluminio, boro, cobalto, cobre, cromo, flúor, hierro, yodo, manganeso, molibdeno, níquel, selenio, silicio, estaño, vanadio y zinc), son esenciales para el crecimiento, el desarrollo y la salud de los organismos vegetales y animales. Generalmente es muy difícil diferenciar las concentraciones inofensivas de las tóxicas.
Cuadro 1. Equilibrio de la entrada desde la atmósfera y la salida por acción del agua de algunos oligoelementos metálicos en diversos suelos (g/ha/año)
|
País |
Tipo de suelo |
Tipo de vegetación |
Cadmio |
Cobre |
Plomo |
Zinc |
||||
|
entrada |
salida |
entrada |
salida |
entrada |
salida |
entrada |
salida |
|||
|
Dinamarca |
Arcilla arenosa |
Cultivos |
3 |
0,3 |
- |
- |
260 |
0,3 |
250 |
120 |
|
Rep. Fed. De Alemania |
Arcilla limosa |
Bosque de pinos |
4,5 |
1,4 |
18 |
7 |
110 |
6 |
210 |
76 |
|
Polonia |
Arcilla arenosa |
Cultivos |
5 |
3 |
39 |
25 |
207 |
40 |
547 |
180 |
|
Suecia |
Suelo forestal |
Bosque de abetos |
2 |
5 |
20 |
29 |
150 |
81 |
180 |
270 |
|
EE.UU. |
Arcilla arenosa |
Bosque caducifolio |
21 |
7 |
- |
- |
286 |
6 |
538 |
140 |
Fuente: Kabata-Pendias y Pendías (en prensa).
La mayor parte de los oligoelementos, y especialmente los metales pesados, se acumulan en la superficie del suelo, debido tanto a la contaminación local como al transporte vía aire de los contaminantes desde largas distancias En distintos países se ha investigado el equilibrio de entrada y salida de los oligoelementos metálicos en los suelos (Cuadro 1), y se ha demostrado que sus concentraciones aumentarán probablemente a escala mundial, a medida que crezcan las actividades industriales y agropecuarias.
Se ha estimado que el incremento anual medio de metales pesados provocado por el depósito de polvo en el suelo de la región de Tokio, es de 0,05 ppm de cadmio y 0,5 ppm de plomo y zinc (Kitagishi y Yamane, 1981). Los valores equivalentes para los países europeos, teniendo en cuenta la corriente de salida de elementos, son los siguientes (en ppm): cadmio, 0,001; níquel, 0,003; cromo, 0,007; cobre; 0,02; plomo, 0,05; zinc, 0,08 (Kabata-Pendias y Pendías, en prensa).
Los diferentes tipos de suelo, especies de plantas y condiciones de crecimiento, hacen que la contaminación del suelo influya de modo diverso en la presencia de oligoelementos en las plantas. Aunque las directrices sobre concentraciones seguras de oligoelementos en el suelo todavía están en una fase experimental y de estudio, algunos autores han ofrecido ya valores mínimos de acumulación fitotóxica (Cuadro 2).
Cuadro 2. Concentraciones excesivas en el suelo de algunos oligoelementos considerados fitotóxicos (ppm, PS)
|
Elemento |
Gama de la concentración |
|
Boro |
25-100 |
|
Cadmio |
3-8 |
|
Cromo |
75-100 |
|
Cobre |
60-120 |
|
Plomo |
100-400 |
|
Molibdeno |
2-10 |
|
Níquel |
100 |
|
Zinc |
70-400 |
Fuente: Kabata-Pendias y Pendías (en prensa).
En general, la capacidad del suelo para compensar los oligocontaminantes está estrechamente relacionada con su capacidad de intercambio de cationes, que controla los niveles críticos de contaminación con efectos tóxicos sobre las plantas y el ambiente. En general, la capacidad de compensación (que también se denomina «resistencia a la contaminación química») de un suelo pesado no ácido con un alto contenido de materia orgánica y de sesquióxidos, es varias voces superior a la de un suelo ácido ligero y arenoso. Los suelos arcillosos neutros pueden acumular una cantidad mayor de oligoelementos menos agresivos para la biosfera; sin embargo, en algunos casos especiales la movilización de los oligocontaminantes puede también ser alta en suelos neutros o alcalinos. Por ejemplo, en suelos arcillosos de arrozales se movilizan fácilmente diversos metales pesados, a causa del predominio de los procesos de reducción; en suelos calcáreos y lateríticos de las regiones áridas y semiáridas pueden existir algunos oligoelementos en iones complejos fácilmente solubles.
Figura 1. Acidez de la corteza de los árboles y concentración de dióxido de azufre (SO2) en el aire de los bosques, como función de la distancia a favor del viento de una planta siderúrgica. Los robles estudiados son Quercus robur; los tilos, Tilia cordata; los pinos, Pinus sylvestris. (Las líneas aproximadas de regresión se basan en K. Grodzinska, 1979.)
Las plantas cultivadas en suelos contaminados absorben en general más oligoelementos, y la concentración de éstos en los tejidos vegetales está a menudo directamente relacionada con su abundancia en los suelos, y especialmente en la solución húmeda (Fig. 2).
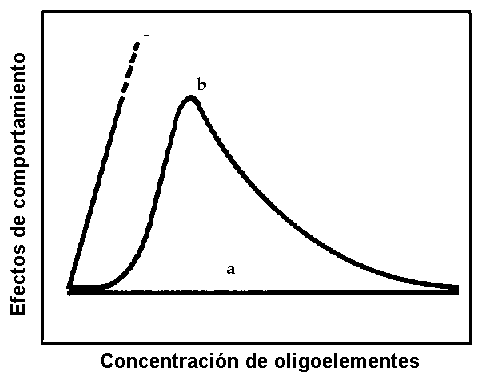
Aunque las plantas controlan la absorción o el rechazo de algunos elementos químicos mediante reacciones fisiológicas adecuadas, son receptoras pasivas de los oligoelementos absorbidos por las raíces y de los que llegan en las precipitaciones. La deposición atmosférica de oligoelementos directamente en la superficie vegetal, contribuye decisivamente a la agresión química a las plantas. Aunque muchos de los oligoelementos son esenciales para el crecimiento, pueden producir efectos tóxicos en el metabolismo vegetal si se encuentran en concentraciones elevadas. La Figura 3 muestra esquemas de hipótesis de reacción de las plantas al aumento de las concentraciones de oligoelementos esenciales y no esenciales.
Los desórdenes metabólicos de las plantas surgen tanto por defecto como por exceso de oligoelementos. Un equilibrio adecuado de los elementos químicos del tejido vegetal es de gran importancia, pues todos se relacionan en el organismo vegetal por sinergismo y/o antagonismo.
Las reacciones básicas relacionadas con los efectos tóxicos del exceso de oligoelementos, tanto en organismos animales como vegetales, son las siguientes:
· cambios en la permeabilidad de las membranas celulares;· reacciones con los grupos tiol que provocan la desnaturalización de las proteínas;
· competencia por lugares con los metabolitos esenciales, y reacción con los compuestos químicos esenciales;
· sustitución de iones esenciales, y ocupación de lugares para conseguir los compuestos químicos esenciales.
A pesar de la gran diversidad de niveles de toxicidad, puede decirse que los elementos más tóxicos, para las plantas superiores y para ciertos microorganismos son el níquel, el mercurio, el cobre, el plomo, el cobalto, el culombio, la plata, el berilio y el estaño. Un aumento de las concentraciones ambientales de mercurio, cadmio, plomo, berilio, cromo, cobre, níquel, plata, arsénico, antimonio, talio, zinc, flúor, selenio, telurio y radionúclidos, constituye un gran peligro para la salud de los organismos animales, entre ellos el hombre.
Figura 2. Absorción de oligoelementos por las plantas, como función de su concentración en soluciones nutrientes.
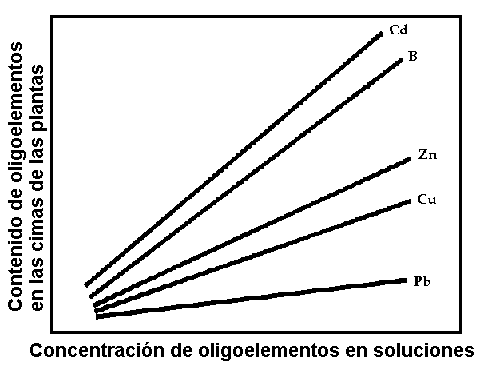
Figura 3. Diagrama esquemático de la plasticidad de comportamiento de las plantas sometidas a tensión química: a) no hubo cambios de comportamiento en especies absolutamente tolerantes, que por lo tanto no sufrieron daños; b) especies no tolerantes al principio, desarrollaron luego tolerancia en el comportamiento; c) en las especies no tolerantes, los cambios de comportamiento provocaron daños orgánicos seguidos de una incapacidad de recuperación.
Una característica común de las plantas es su capacidad de sobrevivir incluso con un exceso de oligoelementos en el ambiente, sobre todo en los suelos. Las plantas inferiores, especialmente los microorganismos, los musgos, las hepáticas y los líquenes, tienen una capacidad extremadamente alta de adaptación a las agresiones químicas. Aunque se supone que las plantas superiores son menos tolerantes, se sabe que acumulan oligoelementos y sobreviven en suelos contaminados con cantidades tóxicas de diversos oligoelementos.
Se ha comunicado la presencia de concentraciones cada vez mayores de oligoelementos metálicos en diversas plantas; el mayor índice de incremento se observó en el contenido de plomo de muestras de musgos en Suecia entre 1875 y 1965 (Rühling y Tyler, 1969). Algunos grupos de árboles en localidades rurales y urbanas en los Estados Unidos acumularon durante su período de crecimiento varias voces más plomo de 1963 a 1973 que de 1910 a 1920 (Boggess y Wixson, 1977).
La evolución de la tolerancia de las plantas a los oligoelementos ha causado la aparición de nuevas especies y genotipos en lugares contaminados. Los mecanismos de la tolerancia a los oligoelementos están relacionados con factores externos (por ejemplo, baja solubilidad de los iones que rodean las raíces vegetales) y con factores internos consistentes en varios procesos metabólicos que protegen a los organismos del exceso de microiones activos.
La resistencia de las plantas a la agresión de los oligoelementos y su capacidad de acumular cantidades sumamente elevadas de éstos (Cuadro 3), pueden llegar a constituir un grave riesgo para la salud porque producen un vínculo contaminante en la cadena alimentaria.
El flúor que emiten diversas industrias (por ejemplo, las fundiciones de aluminio. las fábricas de ladrillos y de vidrio y las de fertilizantes fosfatados) es el oligocontaminante más corriente, peligroso y fitotóxico. La gran actividad química del ácido fluorhídrico formado a partir de flúor sólido o gaseoso, provoca una elevada acidificación del suelo y destruye los minerales arcillosos y los complejos minerales húmicos.
El flúor es fácilmente asimilable por las plantas cuando se presenta en los suelos en forma soluble, pero no hay pruebas de su toxicidad si es absorbido sólo por las raíces. En cambio, el flúor transportado por el aire es muy tóxico para las plantas.
La contaminación con flúor inhibe el crecimiento de diversas plantas. El daño más importante se debe a la agresión combinada del flúor y el dióxido de azufre. Los pinos parecen ser especialmente sensibles a estos contaminantes químicos.
Aunque las plantas son capaces de desarrollar mecanismos de tolerancia a la agresión de los oligoelementos, su salud y productividad pueden reducirse mucho. Las Figuras 4 y 5 muestran los efectos generalizados de las concentraciones de oligometales en la solución nutriente sobre el rendimiento y el contenido de metales de los tejidos vegetales.
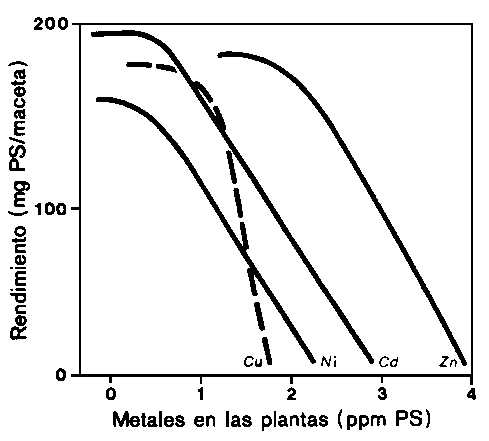
Figura 4. Efectos generalizados de las concentraciones de oligoelementos metálicos en soluciones nutrientes, sobre el rendimiento y el contenido de metal de las plantas.
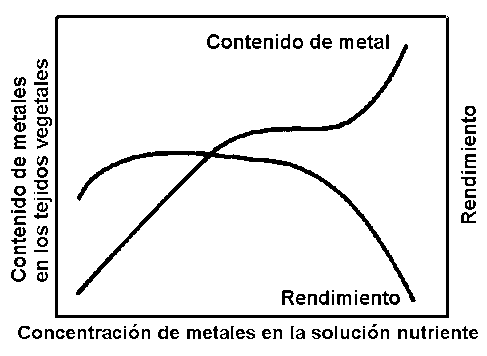
Figura 5. Reacción de los tejidos de plantas jóvenes de cebada a concentraciones de cuatro diferentes metales pesados. Las concentraciones de metal figuran en potencias de 10. (En base a datos de Beckett, Davis y Brindley, 1979.)
Cuadro 3. Niveles excesivos de oligoelementos metálicos en cultivos alimentarios crecidos en lugares contaminados (ppm, PS)
|
Elementos |
Concentración |
Cultivos y parte afectada |
Fuente de contaminación |
País |
|
|
Excesiva 1 |
De fondo |
||||
|
Cadmio |
45 |
0,3 |
Lechuga, hojas |
Fundición de plomo |
Australia |
|
|
4,2 |
0,08 |
Arroz, grano |
Fundición de zinc |
Japón |
|
|
6,4 |
0,4 |
Espinaca, hojas |
Fundición de zinc y plomo |
Zambia |
|
Cobre |
64 |
8 |
Lechuga, hojas |
Fundición de cobre |
Australia |
|
|
14 |
5 |
Rábanos, raíz |
Jardín urbano |
Reino Unido |
|
|
4 |
2,8 |
Arroz, grano |
Tierra de cultivo de regadío |
Japón |
|
Plomo |
1000 |
2 |
Lechuga, hojas |
Fundición de plomo |
Reino Unido |
|
|
57 |
1,8 |
Zanahoria, raíz |
Fundición de plomo |
Polonia |
|
|
66 |
3 |
Espinaca, hojas |
Fundición de zinc y plomo |
Zambia |
|
Mercurio |
0,4 |
0,008 |
Lechuga, hojas |
Procesos de cloro-álcalis |
Suiza |
|
|
0,8 |
0,05 |
Zanahoria, raíz |
Mina de mercurio |
Yugoslavia |
|
|
0,6 |
0,01 |
Avena, grano |
Tratamiento de semillas |
Suecia |
|
Zinc |
710 |
25 |
Cebolla, bulbo |
Fundición de plomo |
Reino Unido |
|
|
316 |
40 |
Lechuga, hojas |
Fundición de zinc |
Australia |
|
|
114 |
35 |
Soja, grano |
Tierra agrícola cenagosa |
Estados Unidos |
1 Máximo contenido encontrado.
Fuente: Kabata-Pendias y Pendías (en prensa).
Las fuentes antropogénicas de entrada de oligoelementos en la biosfera son uno de los aspectos más graves de la contaminación ambiental. En especial, el efecto de la agresión de los oligoelementos a la biosfera de las regiones áridas y semiáridas debe ser motivo de gran preocupación. Los procesos biogeoquímicos específicos de estas regiones pueden dar lugar a alteraciones rápidas e irreversibles del medio natural.
«La agresión de los oligoelementos a la biosfera en las zonas áridas y semiáridas, debe ser motivo de gran preocupación. Los procesos biogeoquímicos específicos de estas zonas pueden dar lugar a alteraciones rápidas e irreversibles del medio natural.»
Entre los oxidantes fotoquímicos que existen en la atmósfera como contaminantes figuran el ozono (O3), el dióxido de nitrógeno (NO2) y los peroxiacetilnitratos (PAN). Otras materias pueden también intervenir en reacciones fotoquímicas, pero son de importancia mucho menor.
Esos compuestos son liberados a la atmósfera sobre todo por las industrias y los vehículos motorizados. Se ha reconocido recientemente que son las sustancias más nocivas para los vegetales y los animales, particularmente cuando se producen en forma de niebla tóxica fotoquímica, mezcla de contaminantes gaseosos, acuosos y sólidos que reacciona a los rayos ultravioleta de la luz, y produce compuestos a la vez irritantes y tóxicos para los tejidos vivos.
Algunos factores meteorológicos controlan las concentraciones, el transporte y la toxicidad de los oxidantes fotoquímicos en el aire. Normalmente, su formación y volatilidad aumentan al subir la temperatura. Otros factores, como la luz y el agua, pueden también afectar a esos procesos.
Los efectos ambientales de los oxidantes, y especialmente su absorción por las plantas, su fitotoxicidad y el mecanismo de resistencia vegetal a diversos oxidantes, han sido tema de amplios estudios (Mudd y Kozlowski, 1975). En general puede decirse que los oxidantes fotoquímicos provocan una reducción de los tejidos fotosintéticos por lesiones en el tejido de las hojas, y afectan a los procesos de intercambio gaseoso en la superficie folicular. También se ha demostrado que los aminoácidos, las proteínas y los ácidos grasos no saturados son susceptibles a la oxidación por el ozono, que provoca diversos cambios en la membrana plasmática y afecta a los procesos metabólicos.
Los contaminantes casi nunca se presentan aislados; varios gases y sustancias fitotóxicas pueden provocar diversos efectos según sus proporciones e interacciones y según la resistencia de un determinado ecosistema. Sin embargo, debe hacerse hincapié en que todos los oxidantes, y especialmente el ozono, provocan grandes daños en la vegetación, así como la descomposición de productos manufacturados.
Los compuestos fotoquímicos naturales (por ejemplo, el ozono) se volatilizan en los bosques como resultado de la acción de la luz solar sobre los terpenos y otros hidrocarburos producidos por las grandes masas de algunos tipos de vegetación forestal.
|
Glosario adsorción: adhesión de una capa muy fina de moléculas (de gases, soluciones o líquidos) a la superficie de los cuerpos sólidos o líquidos con los que entra en contacto; a diferencia de la absorción, no hay aquí penetración por debajo de la superficie de: dicho cuerpo sólido o liquido. anión: específicamente, el ion de una solución electrolizada que se desplaza hacia el ánodo, o polo positivo; en general, cualquier ion negativo. antagonismo: situación en que el efecto combinado de dos o más elementos es menor que la suma de los efectos de cada elementos por sí solo; antónimo de sinergismo. antropogénico: relativo a, o que comprende la influencia del hombre sobre la naturaleza. calcáreo: de carbonato de calcio, o que lo contiene. catión: específicamente, el ion que en una solución electrolizada se desplaza hacia el cátodo, o polo negativo; antónimo de anión (ver arriba); en general, cualquier ion positivo. coloide: sustancia en estado de división, que no pasa a través de una membrana semipermeable; sus partículas son demasiado pequeñas para la capacidad de resolución de un microscopio luminoso ordinario; en suspensión o solución, difracta un rayo de luz, y no da precipitados. PS: peso de las muestras secadas al aire. húmico: de humus, o relativo a él, o que deriva de él al menos en parte. suelos ferralíticos: suelos bien drenados, formados originariamente por rocas ígneas de base, que consisten sobre todo en hidróxidos de hierro y aluminio con poco contenido de dióxido de silicio. metabolito, metabólico: metabolito es un producto del metabolismo, o bien la suma de los procesos de generación o destrucción de protoplasma no esencial para la vida; metabólico es lo que está sujeto a un cambio relacionado con el metabolismo. necrótico: que causa la muerte de tejidos vivos. PAN: peroxiacetilnitratos. HPC: hidrocarburos policíclicos. fitotóxico: venenoso para las plantas. ppm: partes por millón. radionúclidos: tipos radiactivos de átomos, caracterizados por la constitución particular de sus núcleos; por ejemplo, en cuanto al contenido de energía y al número de protones y neutrones. sesquióxidos: óxidos hidratados de hierro, aluminio y titanio. sinergismo: situación en que el efecto combinado de dos o más elementos - por ejemplo contaminantes, productos químicos, nutrientes - es mayor que la suma de los efectos de cada elemento por si solo. antónimo de antagonismo (ver arriba). grupos tiol: también llamados grupos mercapto; cualquier compuesto de una clase análoga a los alcoholes y fenoles, pero que contiene azufre en vez de oxigeno; pueden tener olores muy desagradables. volátil, volatilizar: un elemento es volátil cuando se transforma fácilmente en vapor o gas a temperaturas relativamente bajas; volatilizar un elemento es hacerlo volátil, o sea capaz de fácil transformación en gas o vapor. |
Muchos contaminantes están presentes en la atmósfera en forma de suspensiones en aerosol compuestas de partículas sólidas o gotas de líquido. Las partículas suspendidas de polvo, productos químicos, líquidos, sal marina, pólenes, bacterias, abundan en la atmósfera, y su comportamiento e influencia sobre los organismos vivos dependen de sus propiedades físicas. Los efectos ambientales de las partículas en suspensión constituyen uno de los aspectos menos conocidos de la contaminación del aire.
La composición física de los elementos de contaminación del aire es muy variable, y las partículas pueden constituir del 10 al 50% del total de contaminantes, según las fuentes y controles de la contaminación.
Aparte de la tensión química que ejercen las partículas suspendidas, su deposición sobre las superficies vegetales provoca una reducción de la luz del sol que penetra en el tejido de la planta. Los efectos del polvo suspendido en el aire sobre la salud son también motivo de gran preocupación.
Entre las decenas de sustancias identificadas como fuente de pequeñas partículas en el aire, los contaminantes más nocivos son el hollín, los hidrocarburos policíclicos (HPC) y el asbesto. Fibras similares al asbesto, los silicatos de forma fibrosa, han provocado graves enfermedades al ser inhalados por los animales y el hombre (Maxwell, 1976).
Los oligocontaminantes orgánicos en partículas, y especialmente los que se forman en los procesos de conversión del carbón, pueden afectar al ambiente incluso en concentraciones bajas. De este grupo de partículas, los hidrocarburos y los HPC representan un riesgo especial para la salud. La ceniza en suspensión, producto de la combustión u otros procesos de conversión del carbón, contiene proporciones variables, generalmente pequeñas, de compuestos de HPC como pireno, perileno, fluoranteno y coroneno; algunos son cancerígenos, y todos ellos se combinan con vestigios de contaminantes inorgánicos para formar compuestos organometálicos. Todos los compuestos de HPC tienen elevadas propiedades de absorción y adhesión, por lo que se los considera muy nocivos para los reinos vegetal y animal.
Los contaminantes en partículas emitidos por los hornos de cemento tienen una influencia específica en el ambiente. El polvo de cemento está compuesto por partículas relativamente grandes y contiene una gran proporción de óxidos de calcio y de magnesio. Los efectos ambientales más corrientes observados cerca de las fábricas de cemento son un aumento del pH del suelo, y una reducción del crecimiento de la vegetación.
En ningún momento de la historia ha habido como ahora mayor necesidad de aumentar la producción de alimentos y combustibles, así como de conservar la biosfera. La evolución de los últimos decenios ha demostrado claramente la rápida destrucción de los recursos naturales. Es indudable que la actual degradación química de la biosfera puede convertirse en el más importante factor limitativo de la producción alimentaria a escala mundial. La contaminación del suelo con productos químicos, y particularmente con oligoelementos, debe ser un motivo de gran preocupación. Hasta ahora, todos los métodos que se han aplicado para la recuperación de los suelos después de su degradación química han fracasado.
INVESTIGACIÓN SANITARIA EN BRASIL. Patrocinada por el PNUD, el PNUMA y las OMS
Los conceptos de Y. Laulan (1982) son el mejor comentario de la situación existente: «De continuar las actuales tasas de degradación del suelo, casi un tercio de las tierras cultivables del mundo se destruirán en los próximos 20 años.»
Hasta ahora la tecnología ha dado lugar a un despilfarro de los recursos, al agotamiento, expoliación y contaminación del suelo, y a la contaminación del aire y del agua. Estos efectos, antes aislados, pueden extenderse ahora rápidamente a regiones más amplias, a continentes, e incluso a todo el mundo, como ocurre con la precipitación radioactiva.
La naturaleza de la agresión química a la biosfera es tal que ninguna medida o control local puede ser enteramente eficaz si no se considera como parte de un sistema global: la humanidad necesita urgentemente integrar la planificación de las actividades industriales y socioeconómicas.
Una esperanza final es que, aprovechando la experiencia de los países industrializados, los países en desarrollo logren evitar en lo posible, las consecuencias negativas de la industrialización y la urbanización en gran escala.
BECKETT, P.H.T., DAVIS, R.D. y BRINDLEY, P. 1979. The disposal of sewage sludge unto farmland: the scope of the problem of toxic elements. Wat. Pollution Control, 78: 419-425.
BENGLEY, S. y LABREOQUE, R. 1982. Watch out for acid fog. Newsweek, 13 de diciembre, p. 57.
BJOR, K., HORNTVEDT, R. y JORANGER, E. 1974. Distribution and chemical enrichment of precipitation in a southern Norway forest stand. SNSF-Project Res. Rep. 1, Ås, Noruega. 28 págs. (En noruego, resumen en inglés)
BOGGESS, W.R. y WIXSON, R.G. (eds.). 1977. Lead in the environment. Rep. NSF/RA-770214, Wáshington. 264 págs.
GRODZINSKA, K. 1979. Tree bark-sensitive biotest for environment acidification. Environment Int, 2: 171-176.
HUTCHINSON, T.C. y COLLINS, F.W. 1978. Effect of H+ ion activity and Ca2+ on the toxicity of metals in the environment. Environ. Health Perspect., 25: 47-52.
KABATA-PENDIAS, A. y PENDIAS, H. Trace elements in soils and plants. Boca Raton, FL, CRC Press. (En prensa)
KITAGISHI, K. y YAMANE, I. 1981. Heavy metal pollution in soils of Japan. Tokio Japan scient. Soc. Press. 302 págs.
LAULAN, Y. 1982. Economic consequences. Back to the dark ages. Ambio, 11: 149-151.
MAXWELL, K.E. 1976. Environment of life. En cino, CA, Dickenson Publ. 489 págs.
MUDD, J.B. y KOZLOWSKI, T.T. 1975. Response of plants to air pollution. Nueva York, Academic Press. 383 págs.
RÜHLING, A. y TYLER, G. 1969. Ecology of heavy metals: a regional and historical study. Botaniska Notiser, 122: 218-269.
TAYLOR, O.C. 1980. Phytotoxic air pollutants and their source. UNECE, Symp. on Effects of Air-Borne Pollution on Vegetation. Warsaw, p. 51-58.