IDENTIDAD
Rasgos biológicos
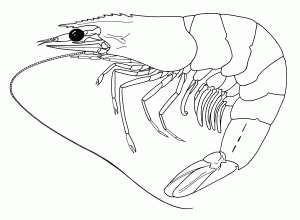
Rostrum moderadamente largo con 7–10 dientes dorsales y 2–4 dientes ventrales. En los machos maduros petasma simétrico y semi abierto. Espermatóforos complejos, consistentes de masa espermática encapsulada por la vaina. Las hembras maduras tienen el télico abierto. Seis nauplios, tres proto-zoeas, y tres etapas de mysis. Su coloración es normalmente blanca translúcida, pero puede cambiar dependiendo del sustrato, la alimentación y la turbidez del agua. Talla máxima 23 cm, con CL máxima de 9 cm. Comúnmente las hembras crecen más rápidamente y adquieren mayor talla que los machos.
Galería de imágenes
 |
 |
Progenitor hembra (Foto: Briggs, M.) |
Maduración en tanques en América Latina |
 |
 |
Estanques extensivos (Foto: Briggs, M.) |
Cosecha (Foto: Briggs, M.) |
PERFIL
Antecedentes históricos
La primera reproducción artificial de esta especie se logró en Florida en 1973 a partir de nauplios procedentes de una hembra ovada silvestre capturada en Panamá. Tras los resultados positivos obtenidos en estanques y el descubrimiento de la ablación unilateral (y nutrición adecuada) para promover la maduración en Panamá en 1976, el cultivo comercial de Penaeus vannamei se inició en Centro y Sudamérica. El desarrollo subsiguiente de las técnicas para la cría intensiva condujo a su cultivo en Hawaii, área continental de Estados Unidos de Norteamérica, y extensas zonas de Centro y Sudamérica, a principios de la década de 1980. Desde este momento, el cultivo comercial de esta especie en América Latina mostró una tendencia de rápido crecimiento (con picos cada 3 ó 4 años, en los años cálidos y húmedos de presencia de “El Niño”), y declives coincidentes con la irrupción de enfermedades durante los años fríos de presencia de “La Niña”. A pesar de estos problemas, la producción de P. vannamei en el continente americano ha continuado incrementándose. Después de su declive en 1998 en que se alcanzó un volumen pico de 193 000 toneladas, descendiendo a 143 000 toneladas en 2000, la producción volvió a aumentar a 270 000 toneladas en 2004. Asia ha experimentado un incremento fenomenal en la producción de P. vannamei. A pesar de que a la FAO no le fue reportada producción alguna en 1999, en el año 2004 se registraron casi 1 116 000 toneladas sobrepasando la producción de P. monodon en China, la Provincia China de Taiwán y Tailandia, gracias a varios factores favorables. Sin embargo, debido a los temores relativos a la importación de enfermedades exóticas, varios países asiáticos se han mostrado reacios a impulsar el cultivo de P. vannamei, por lo que su cultivo se mantiene oficialmente confinado a pruebas experimentales en Camboya, India, Malasia, Myanmar y Filipinas. Tailandia e Indonesia, permiten su libre cultivo comercial pero mantienen restricciones oficiales permitiendo únicamente la importación de progenitores libres de patógenos específicos (SPF) o resistentes (SPR). De manera similar, la mayoría de los países Latinoamericanos tienen leyes de estricta cuarentena o vedas para prevenir la importación de agentes patógenos exóticos con la importación de nuevas cepas.
Principales países productores
Los principales países productores de Penaeus vannamei se muestran en el mapa, mientras que la lista completa de países incluye: China, Tailandia, Indonesia, Brasil, Ecuador, México, Venezuela, Honduras, Guatemala, Nicaragua, Belice, Viet Nam, Malasia, P.C. de Taiwán, Islas del Pacífico, Perú, Colombia, Costa Rica, Panamá, El Salvador, Estados Unidos de América, India, Filipinas, Camboya, Surinam, Saint Kitts, Jamaica, Cuba, República Dominicana y Bahamas.
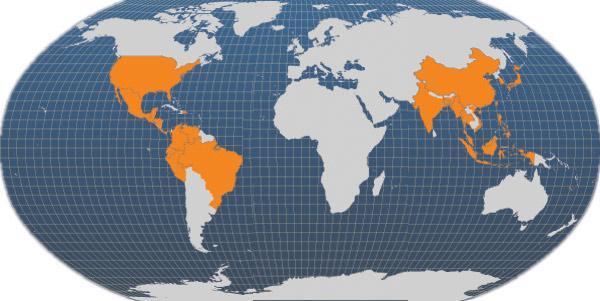

Principales países productores de Penaeus vannamei (FAO, Estadísticas Pesqueras, 2006)
Hábitat y biología
El camarón blanco es nativo de la costa oriental del Océano Pacífico, desde Sonora, México al Norte, hacia Centro y Sudamérica hasta Tumbes en Perú, en aguas cuya temperatura es normalmente superior a 20 °C durante todo el año. Penaeus vannamei se encuentra en hábitats marinos tropicales. Los adultos viven y se reproducen en mar abierto, mientras que la postlarva migra a las costas a pasar la etapa juvenil, la etapa adolescente y pre adulta en estuarios, lagunas costeras y manglares. Los machos maduran a partir de los 20 g y las hembras a partir de los 28 g en una edad de entre 6 y 7 meses. Cuando P. vannamei pesa entre 30 y 45 g libera entre 100 000 y 250 000 huevos de aproximadamente 0,22 mm de diámetro. La incubación ocurre aproximadamente 16 horas después del desove y la fertilización. En la primera etapa, la larva, denominada nauplio, nada intermitentemente y es fototáctica positiva. Los nauplios no requieren alimentación, sino que se nutren de su reserva embrionaria. Las siguientes etapas larvarias (protozoea, mysis y postlarva temprana respectivamente) continúan siendo planctónicas por algún tiempo, se alimentan del fitoplancton y del zooplancton, y son transportados a la costa por las corrientes mareales. Las postlarvas (PL) cambian sus hábitos planctónicos unos 5 días después de su metamorfosis a PL, se trasladan a la costa y empiezan a alimentarse de detritos bénticos, gusanos, bivalvbos y crustáceos.
PRODUCCIÓN
La semilla silvestre de Penaeus vannamei fue utilizada en América Latina para los cultivos extensivos en estanques hasta finales de la década de 1990. Los programas de domesticación y selección genética permitieron un suministro más consistente de postlarvas de alta calidad, libres de patógenos específicos (SPF) y/o resistentes (SPR), que eran criadas en incubadoras. Algunas PL fueron enviadas a Hawaii en 1989, obteniéndose las líneas de producción SPF y SPR y que posteriormente condujeron a su industrialización en Estados Unidos de Norteamérica y en Asia.
Existen tres fuentes de abasto de progenitores de P. vannamei:
Los sistemas de incubadoras varían desde los altamente especializados hasta los pequeños, no sofisticados, casi siempre tierra adentro, desde patios traseros hasta instalaciones sofisticadas e instalaciones con control ambiental y coordinadas con unidades para maduración. Los nauplios se colocan en tanques planos, preferiblemente en forma de 'V' o 'U' con un volumen de 4 a 100 m³, construidos con concreto, fibra de vidrio o recubiertos con membranas de materiales plásticos. Las larvas se crían, o bien hasta PL10–12 en un solo tanque para la cría larvaria, o se cosechan hasta PL4–5 y se transfieren a tanques de flujo rápido con fondo plano y se crían hasta PL10–30. Las tasas de supervivencia de PL10–12 en promedio deben ser superiores al 60 por ciento. El agua se intercambia regularmente (entre el 10 y el 100 por ciento diariamente) para mantener buenas condiciones ambientales. La alimentación normalmente consiste de organismos vivos (microalgas y Artemia), complementada con microcápsulas de alimentos preparados secos o líquidos. El período de crecimiento hasta PL 12 es de aproximadamente 21 días. Se brindan los cuidados necesarios para reducir la contaminación bacteriana/patógena de las instalaciones larvarias, mediante el empleo de una combinación periódica de secado y desinfección, sedimentación del agua de entrada, filtración y/o clorinación, desinfección de los nauplios, recambio de agua y el uso de antibióticos o (preferiblemente) probióticos.
La mayoría de las granjas de cultivo del P. vannamei no incluyen criaderos, sino que las PL 10–12 se transportan a una temperatura menor, sea en bolsas plásticas o en tanques de transportación oxigenados, hasta los es tanques en donde son introducidos directamente. En algunos casos, se utilizan sistemas de cría que incluyen tanques de concreto separados o estanques de tierra, o aún corrales de redes o jaulas ubicadas en los estanques de producción. Esos sistemas de crianza pueden utilizarse entre 1 y 5 semanas. Los criaderos son útiles en áreas de clima más frío, cuyas temporadas de crecimiento son limitadas, por lo que las PL se crían hasta una talla mayor (0,2–0,5 g) en estanques o tanques con calentamiento, antes de ser sembradas en estanques. El empleo de técnicas súper intensivas, control de temperatura, invernaderos, canales de concreto, etc. han dado buenos resultados en Estados Unidos de Norteamérica.
Las técnicas para el crecimiento se pueden sub-dividir en 4 grandes categorías: extensivas, semi-intensivas, intensivas y súper-intensivas, que representan respectivamente, densidades de siembra baja, media, alta y extremadamente alta.
Extensiva
Esta técnica es común en los países latinoamericanos. Los cultivos extensivos de P. vannamei desarrollan en las zonas inter mareales, donde no hay bombeo de agua ni aireación. Los estanques suelen ser de forma irregular, con una superficie de entre 5 y 10 ha (o hasta 30 ha) y una profundidad de entre 0,7 y 1,2 m. Generalmente, se empleaba semilla silvestre que entraba a los estanques con la marea alta, o se adquiría a los recolectores de semilla; desde la década de 1980 se utiliza PL obtenida de las incubadoras, con una densidad de 4–10/m2. El camarón se alimenta a base de alimentos producidos naturalmente mediante fertilización, y dosis una vez al día de alimentos balanceados de bajas proteínas. A pesar de la baja densidad, a los 4 ó 5 meses se cosechan camarones pequeños de entre 11 y 12 g. El rendimiento en estos sistemas extensivos es de 150–500 kg/ha/cosecha, con una ó dos cosechas anuales.
Semi-intensiva
Los estanques de cultivo semi intensivo (1–5 ha) emplean semillas producidas en incubadoras, con densidades de siembra entre 10 y 30 PL/m 2 ; estos sistemas son comunes en América Latina. El agua se bombea para su recambio, los estanques tienen una profundidad de entre 1 y 1,2 m y si acaso, emplean un mínimo de aireación artificial. El camarón se alimenta de productos naturales propiciando su producción mediante fertilización del estanque, complementado con alimentación 2 ó 3 veces al día. Los rendimientos de la producción en estanques semi intensivos varían entre 500 y 2 000 kg/ha/cosecha, con dos cosechas por año.
Intensiva
Las granjas intensivas comúnmente se ubican fuera de las áreas intermareales, donde los estanques puedan drenarse totalmente, secarse y prepararse antes de cada ciclo; cada vez más se ubican lejos del mar, en tierras más baratas y de baja salinidad. Este sistema de cultivo es común en Asia y en algunas granjas de América Latina que están procurando elevar su productividad. Comúnmente los estanques son de tierra, pero también se utilizan membranas de recubrimiento para reducir la erosión y mejorar la calidad del agua. En general los estanques son pequeños (0,1–1,0 ha) sean cuadrados o redondos. La profundidad suele ser mayor a 1,5 m. Las densidades varían entre 60 y 300 PL/m 2 . Se requiere una aireación continua de 1 HP/400–600 kg de camarón cosechado, para la oxigenación y circulación del agua. La alimentación se basa en dietas artificiales suministradas 4 a 5 veces diarias. Los factores de conversión alimenticia fluctúan entre 1,4 y 1,8:1.
Desde la irrupción de síndromes virales, se ha generalizado el uso de cepas domesticadas libres o resistentes de patógenos específicos (SPF) o (SPR) respectivamente; la implementación de medidas de bioseguridad y sistemas de bajo recambio de agua. Sin embargo la alimentación, la calidad y recambio del agua, aireación y el florecimiento del fitoplancton requieren de un cuidadoso monitoreo y manejo. Los rendimientos de la producción varían entre 7 y 20 000 kg/ha/cosecha, pudiéndose lograr de 2 a 3 cosechas por año, con un máximo de 30 a 35 000 kg/ha/cosecha.
En el sistema de floculación bacterial, los estanques (0,07–1,6 ha) se manejan con alta aireación, recirculación y sistemas de bacterias heterotróficas. Se utilizan alimentos bajos en proteínas, suministrándolos de 2 a 5 veces al día, en un esfuerzo por elevar la relación C:N a >10:1 y desviar los nutrientes adicionados a través procesos bacterianos en vez de la vía algal. Se utilizan densidades de 80–160 PL/m2 , los estanques se hacen heterotróficos y se forman flóculos de bacterias, que son consumidos por los camarones, reduciendo la dependencia de alimentos altos tanto en proteínas como en tasa de conversión alimenticia incrementándose la eficiencia costo-beneficio. Esos sistemas han logrado una producción de 8–50 000 kg/ha/cosecha en Belice e Indonesia.
Super-intensiva
La investigación desarrollada recientemente en Estados Unidos de Norteamérica se ha enfocado al crecimiento del P. vannamei ien sistemas de canales de flujo rápido súper-intensivos en invernaderos, sin recambio de agua (salvo el reemplazo de pérdidas por evaporación) o la descarga, utilizando larvas de cepas SPF. Por lo tanto son bioseguros, sustentables, con poco impacto ecológico pudiendo producir camarón de alta calidad con eficiencia costo-beneficio. El cultivo en canales de 282 m2 con 300–450 juveniles/m2 de entre 0,5 y 2 g para su crecimiento entre 3 y 5 meses, ha logrado obtener producciones de entre 28 000 y 68 000 kg/ha/cosecha a tasas de crecimiento de 1,5 g/semana, tasas de sobrevivencia de 55–91 por ciento, con un peso promedio de entre 16 y 26 g y factores de conversión alimenticia de 1,5–2,6:1.
P. vannameies muy eficiente en la utilización de la productividad natural de los estanques, aún bajo condiciones de cultivo intensivo. Adicionalmente, los costos de alimentación son generalmente menores para P. vannamei que para P. monodon, que es más carnívoro, debido a sus menores requerimientos proteicos (entre 18 y 35 por ciento, comparado con un requerimiento de entre 36 y 42 por ciento), especialmente donde se emplean sistemas de floculación de bacterias. Los precios de los alimentos para P. vannamei varían de 0,6 USD/kg en Latinoamérica y Tailandia hasta 0,7–1,1 USD/kg en los demás países de Asia. Generalmente se alcanzan Factores de Conversión Alimenticia de 1,2 a 1,8:1.
Para realizar la cosecha de los estanques de cultivos extensivos y semi intensivos, se drenan los estanques durante la marea baja, a través de redes instaladas en la compuerta de salida. Si la marea no permite la cosecha, el agua debe bombearse. En algunas granjas grandes, maquinaria de cosecha bombea el agua y al camarón al borde del estanque, en donde se elimina el agua. Los estanques de cultivos intensivos pueden cosecharse de manera similar, arrastrando también pequeñas redes por 2 a 6 personas para acorralar al camarón hacia un lado del estanque, de donde se retiran mediante redes atarraya o con cucharas de red o cubetas perforadas.
En los cultivos intensivos asiáticos, las cosechas parciales son comunes a partir del tercer mes. En Tailandia se instala temporalmente una compuerta en una esquina, en el interior del estanque para cosechar estanques con sistemas cerrados. El camarón es capturado en las redes adosadas a esta compuerta, cuando se bombea el agua.
En sistemas súper intensivos, el camarón simplemente se cosecha con grandes redes cuchara, conforme se vaya requeiriendo camarón para ser procesado.
Cuando el camarón se vende directamente a las plantas de procesamiento, comúnmente se utilizan equipos de cosecha y manejo para mantener la calidad del camarón. Una vez que se selecciona, el camarón se lava, pesa y se mata al introducirlo en agua helada (0 a 4 °C). Frecuentemente se agrega metabisulfato de sodio al agua helada, para evitar la melanosis y la cabeza roja. Posteriormente el camarón se conserva en hielo dentro de contenedores aislados y es transportado en camiones hacia las plantas de procesamiento o a los mercados de camarón. En las plantas de procesamiento, el camarón se coloca en cubos helados, se limpia y selecciona por tallas para su exportación. El camarón se procesa, se congela rápidamente a -10 °C y se conserva a -20 °C para su exportación por barco o carga aérea. Debido a una creciente demanda, exención de impuestos y altos márgenes de ganancia, muchas plantas procesadoras tienen varias líneas de productos con valor agregado.
Los costos de producción varían dependiendo de muchos factores. Los costos de operación para la producción de semilla oscilan en promedio entre 0,5 y 1,0 USD/1 000 PL, en tanto que los precios de venta varían de 0,4 USD/1 000 PL8–10 en China y 1,0–1,2 USD/1 000 PL12 en Ecuador a 1,5–3,0 USD/1 000 PL12 en los países de Asia. Menores costos de alimentación y mayores niveles de intensidad generan costos promedios de producción para la etapa de crecimiento de aproximadamente 2,5 a 3,0 USD/kg para P. vannamei, comparados con los 3,0 a 4,0 USD/kg en los cultivos extensivos de P. monodon.
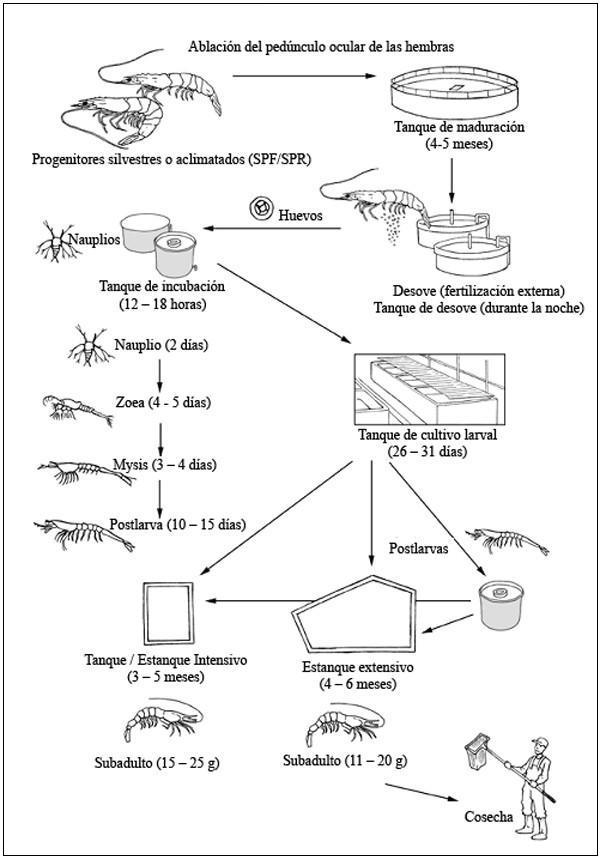
Ciclo de producción

Ciclo de producción de Penaeus vannamei
Sistemas de producción
Suministro de semilla
La semilla silvestre de Penaeus vannamei fue utilizada en América Latina para los cultivos extensivos en estanques hasta finales de la década de 1990. Los programas de domesticación y selección genética permitieron un suministro más consistente de postlarvas de alta calidad, libres de patógenos específicos (SPF) y/o resistentes (SPR), que eran criadas en incubadoras. Algunas PL fueron enviadas a Hawaii en 1989, obteniéndose las líneas de producción SPF y SPR y que posteriormente condujeron a su industrialización en Estados Unidos de Norteamérica y en Asia.
Maduración de reproductores, desove e incubación
Existen tres fuentes de abasto de progenitores de P. vannamei:
- En donde existen en el medio silvestre, los reproductores se capturan en el mar, (generalmente de un año de edad, con un peso superior a los 40 g) para inducir posteriormente su desove.
- De las cosechas de camarón cultivado en estanques (tras cuatro o cinco meses, con un peso de entre 15 y 25 g), se continúan cultivando durante 2 ó 3 meses y posteriormente se transfieren a instalaciones de maduración hasta alcanzar una edad superior a los 7 meses, cuando alcanzan un peso de entre 30 y 35 g.
- Los reproductores libres y resistentes a patógenos específicos (SPF/SPR) cultivados y producidos en tanques se adquieren de Estados Unidos de Norteamérica, (con una edad de entre 7 y 8 meses y un peso de entre 30 y 40 g).
Producción en viveros
Los sistemas de incubadoras varían desde los altamente especializados hasta los pequeños, no sofisticados, casi siempre tierra adentro, desde patios traseros hasta instalaciones sofisticadas e instalaciones con control ambiental y coordinadas con unidades para maduración. Los nauplios se colocan en tanques planos, preferiblemente en forma de 'V' o 'U' con un volumen de 4 a 100 m³, construidos con concreto, fibra de vidrio o recubiertos con membranas de materiales plásticos. Las larvas se crían, o bien hasta PL10–12 en un solo tanque para la cría larvaria, o se cosechan hasta PL4–5 y se transfieren a tanques de flujo rápido con fondo plano y se crían hasta PL10–30. Las tasas de supervivencia de PL10–12 en promedio deben ser superiores al 60 por ciento. El agua se intercambia regularmente (entre el 10 y el 100 por ciento diariamente) para mantener buenas condiciones ambientales. La alimentación normalmente consiste de organismos vivos (microalgas y Artemia), complementada con microcápsulas de alimentos preparados secos o líquidos. El período de crecimiento hasta PL 12 es de aproximadamente 21 días. Se brindan los cuidados necesarios para reducir la contaminación bacteriana/patógena de las instalaciones larvarias, mediante el empleo de una combinación periódica de secado y desinfección, sedimentación del agua de entrada, filtración y/o clorinación, desinfección de los nauplios, recambio de agua y el uso de antibióticos o (preferiblemente) probióticos.
Criadero
La mayoría de las granjas de cultivo del P. vannamei no incluyen criaderos, sino que las PL 10–12 se transportan a una temperatura menor, sea en bolsas plásticas o en tanques de transportación oxigenados, hasta los es tanques en donde son introducidos directamente. En algunos casos, se utilizan sistemas de cría que incluyen tanques de concreto separados o estanques de tierra, o aún corrales de redes o jaulas ubicadas en los estanques de producción. Esos sistemas de crianza pueden utilizarse entre 1 y 5 semanas. Los criaderos son útiles en áreas de clima más frío, cuyas temporadas de crecimiento son limitadas, por lo que las PL se crían hasta una talla mayor (0,2–0,5 g) en estanques o tanques con calentamiento, antes de ser sembradas en estanques. El empleo de técnicas súper intensivas, control de temperatura, invernaderos, canales de concreto, etc. han dado buenos resultados en Estados Unidos de Norteamérica.
Técnicas de engorda
Las técnicas para el crecimiento se pueden sub-dividir en 4 grandes categorías: extensivas, semi-intensivas, intensivas y súper-intensivas, que representan respectivamente, densidades de siembra baja, media, alta y extremadamente alta.
Extensiva
Esta técnica es común en los países latinoamericanos. Los cultivos extensivos de P. vannamei desarrollan en las zonas inter mareales, donde no hay bombeo de agua ni aireación. Los estanques suelen ser de forma irregular, con una superficie de entre 5 y 10 ha (o hasta 30 ha) y una profundidad de entre 0,7 y 1,2 m. Generalmente, se empleaba semilla silvestre que entraba a los estanques con la marea alta, o se adquiría a los recolectores de semilla; desde la década de 1980 se utiliza PL obtenida de las incubadoras, con una densidad de 4–10/m2. El camarón se alimenta a base de alimentos producidos naturalmente mediante fertilización, y dosis una vez al día de alimentos balanceados de bajas proteínas. A pesar de la baja densidad, a los 4 ó 5 meses se cosechan camarones pequeños de entre 11 y 12 g. El rendimiento en estos sistemas extensivos es de 150–500 kg/ha/cosecha, con una ó dos cosechas anuales.
Semi-intensiva
Los estanques de cultivo semi intensivo (1–5 ha) emplean semillas producidas en incubadoras, con densidades de siembra entre 10 y 30 PL/m 2 ; estos sistemas son comunes en América Latina. El agua se bombea para su recambio, los estanques tienen una profundidad de entre 1 y 1,2 m y si acaso, emplean un mínimo de aireación artificial. El camarón se alimenta de productos naturales propiciando su producción mediante fertilización del estanque, complementado con alimentación 2 ó 3 veces al día. Los rendimientos de la producción en estanques semi intensivos varían entre 500 y 2 000 kg/ha/cosecha, con dos cosechas por año.
Intensiva
Las granjas intensivas comúnmente se ubican fuera de las áreas intermareales, donde los estanques puedan drenarse totalmente, secarse y prepararse antes de cada ciclo; cada vez más se ubican lejos del mar, en tierras más baratas y de baja salinidad. Este sistema de cultivo es común en Asia y en algunas granjas de América Latina que están procurando elevar su productividad. Comúnmente los estanques son de tierra, pero también se utilizan membranas de recubrimiento para reducir la erosión y mejorar la calidad del agua. En general los estanques son pequeños (0,1–1,0 ha) sean cuadrados o redondos. La profundidad suele ser mayor a 1,5 m. Las densidades varían entre 60 y 300 PL/m 2 . Se requiere una aireación continua de 1 HP/400–600 kg de camarón cosechado, para la oxigenación y circulación del agua. La alimentación se basa en dietas artificiales suministradas 4 a 5 veces diarias. Los factores de conversión alimenticia fluctúan entre 1,4 y 1,8:1.
Desde la irrupción de síndromes virales, se ha generalizado el uso de cepas domesticadas libres o resistentes de patógenos específicos (SPF) o (SPR) respectivamente; la implementación de medidas de bioseguridad y sistemas de bajo recambio de agua. Sin embargo la alimentación, la calidad y recambio del agua, aireación y el florecimiento del fitoplancton requieren de un cuidadoso monitoreo y manejo. Los rendimientos de la producción varían entre 7 y 20 000 kg/ha/cosecha, pudiéndose lograr de 2 a 3 cosechas por año, con un máximo de 30 a 35 000 kg/ha/cosecha.
En el sistema de floculación bacterial, los estanques (0,07–1,6 ha) se manejan con alta aireación, recirculación y sistemas de bacterias heterotróficas. Se utilizan alimentos bajos en proteínas, suministrándolos de 2 a 5 veces al día, en un esfuerzo por elevar la relación C:N a >10:1 y desviar los nutrientes adicionados a través procesos bacterianos en vez de la vía algal. Se utilizan densidades de 80–160 PL/m2 , los estanques se hacen heterotróficos y se forman flóculos de bacterias, que son consumidos por los camarones, reduciendo la dependencia de alimentos altos tanto en proteínas como en tasa de conversión alimenticia incrementándose la eficiencia costo-beneficio. Esos sistemas han logrado una producción de 8–50 000 kg/ha/cosecha en Belice e Indonesia.
Super-intensiva
La investigación desarrollada recientemente en Estados Unidos de Norteamérica se ha enfocado al crecimiento del P. vannamei ien sistemas de canales de flujo rápido súper-intensivos en invernaderos, sin recambio de agua (salvo el reemplazo de pérdidas por evaporación) o la descarga, utilizando larvas de cepas SPF. Por lo tanto son bioseguros, sustentables, con poco impacto ecológico pudiendo producir camarón de alta calidad con eficiencia costo-beneficio. El cultivo en canales de 282 m2 con 300–450 juveniles/m2 de entre 0,5 y 2 g para su crecimiento entre 3 y 5 meses, ha logrado obtener producciones de entre 28 000 y 68 000 kg/ha/cosecha a tasas de crecimiento de 1,5 g/semana, tasas de sobrevivencia de 55–91 por ciento, con un peso promedio de entre 16 y 26 g y factores de conversión alimenticia de 1,5–2,6:1.
Suministro de alimento
P. vannameies muy eficiente en la utilización de la productividad natural de los estanques, aún bajo condiciones de cultivo intensivo. Adicionalmente, los costos de alimentación son generalmente menores para P. vannamei que para P. monodon, que es más carnívoro, debido a sus menores requerimientos proteicos (entre 18 y 35 por ciento, comparado con un requerimiento de entre 36 y 42 por ciento), especialmente donde se emplean sistemas de floculación de bacterias. Los precios de los alimentos para P. vannamei varían de 0,6 USD/kg en Latinoamérica y Tailandia hasta 0,7–1,1 USD/kg en los demás países de Asia. Generalmente se alcanzan Factores de Conversión Alimenticia de 1,2 a 1,8:1.
Técnicas de cosecha
Para realizar la cosecha de los estanques de cultivos extensivos y semi intensivos, se drenan los estanques durante la marea baja, a través de redes instaladas en la compuerta de salida. Si la marea no permite la cosecha, el agua debe bombearse. En algunas granjas grandes, maquinaria de cosecha bombea el agua y al camarón al borde del estanque, en donde se elimina el agua. Los estanques de cultivos intensivos pueden cosecharse de manera similar, arrastrando también pequeñas redes por 2 a 6 personas para acorralar al camarón hacia un lado del estanque, de donde se retiran mediante redes atarraya o con cucharas de red o cubetas perforadas.
En los cultivos intensivos asiáticos, las cosechas parciales son comunes a partir del tercer mes. En Tailandia se instala temporalmente una compuerta en una esquina, en el interior del estanque para cosechar estanques con sistemas cerrados. El camarón es capturado en las redes adosadas a esta compuerta, cuando se bombea el agua.
En sistemas súper intensivos, el camarón simplemente se cosecha con grandes redes cuchara, conforme se vaya requeiriendo camarón para ser procesado.
Manipulación y procesamiento
Cuando el camarón se vende directamente a las plantas de procesamiento, comúnmente se utilizan equipos de cosecha y manejo para mantener la calidad del camarón. Una vez que se selecciona, el camarón se lava, pesa y se mata al introducirlo en agua helada (0 a 4 °C). Frecuentemente se agrega metabisulfato de sodio al agua helada, para evitar la melanosis y la cabeza roja. Posteriormente el camarón se conserva en hielo dentro de contenedores aislados y es transportado en camiones hacia las plantas de procesamiento o a los mercados de camarón. En las plantas de procesamiento, el camarón se coloca en cubos helados, se limpia y selecciona por tallas para su exportación. El camarón se procesa, se congela rápidamente a -10 °C y se conserva a -20 °C para su exportación por barco o carga aérea. Debido a una creciente demanda, exención de impuestos y altos márgenes de ganancia, muchas plantas procesadoras tienen varias líneas de productos con valor agregado.
Costos de producción
Los costos de producción varían dependiendo de muchos factores. Los costos de operación para la producción de semilla oscilan en promedio entre 0,5 y 1,0 USD/1 000 PL, en tanto que los precios de venta varían de 0,4 USD/1 000 PL8–10 en China y 1,0–1,2 USD/1 000 PL12 en Ecuador a 1,5–3,0 USD/1 000 PL12 en los países de Asia. Menores costos de alimentación y mayores niveles de intensidad generan costos promedios de producción para la etapa de crecimiento de aproximadamente 2,5 a 3,0 USD/kg para P. vannamei, comparados con los 3,0 a 4,0 USD/kg en los cultivos extensivos de P. monodon.
Enfermedades y medidas de control
Los mayores problemas de enfermedad que afectan al P. vannameise muestran en la siguiente tabla. La disponibilidad de cepas libres de patógenos (SPF) y cepas resistentes a patógenos (SPR) constituyen un mecanismo para evitar estas enfermedades, pero también son importantes los procedimientos de bioseguridad, incluyendo:
En algunos casos, se han empleado antibióticos y otros fármacos para el tratamiento, pero su inclusión en esta tabla no implica una recomendación de la FAO en tal sentido.
Expertos en patologías
Se puede obtener asistencia de:
- Secado y escarificado total del fondo de los estanques entre ciclos productivos.
- Reducción del intercambio de agua y tamizado fino de todos los ductos de abasto de agua.
- Uso de mallas anti-pajareras o de espanta-pájaros.
- Colocación de barreras al rededor de los estanques.
- Procedimientos sanitarios.
En algunos casos, se han empleado antibióticos y otros fármacos para el tratamiento, pero su inclusión en esta tabla no implica una recomendación de la FAO en tal sentido.
| ENFERMEDAD | AGENTE | TIPO | SÍNDROME | MEDIDAS |
| Mancha blanca (WSD); también conocida como WSBV o WSSV | Parte del síndrome de manchas blancas, complejo (recientemente reclasificado en una nueva familia como nimavirus) | Virus | El camarón severamente infectado manifiesta reducción en el consumo de alimentos, letargo; alta mortalidad, hasta del 100 por ciento entre 3 y 10 días a partir de la manifestación de signos clínicos; cutículas sueltas con manchas blancas de 0,5–2,0 mm de diámetro, más evidentes dentro del caparazón; el camarón moribundo muestra coloración entre rosada y rojiza-café debido a la expansión de cromatóforos cuticulares y escasas manchas blancas. | Uso de cepas libres de patógenos específicos (SPF); lavar y desinfectar los huevos/nauplios con iodo, formalina; tamizar y separar los reproductores, los nauplios, las postlarvas y los juveniles; evitar cambios bruscos de calidad del agua; mantener temperatura del agua >30 °C; evitar el estrés; evitar uso de alimentos frescos; minimizar recambio de agua para evitar entrada de portadores de virus; tratamiento a estanques e incubadoras infectados con cloro a 30 ppm para matar el camarón infectado y a los portadores; desinfección de equipo. |
| Síndrome del Taura (TS); también conocido como Virus del Síndrome de Taura (TSV) o Enfermedad de Cola Roja | Virus de ARN de una sola banda (Picornaviridae) | Virus | Ocurre durante la única muda en los juveniles a los 5 a 20 días tras la siembra, o tiene un curso crónico de varios meses; debilidad, caparazón blando, tracto digestivo vacío y expansión difusa de cromatóforos rojos en los apéndices; la mortalidad varía de 5 a 95 por ciento; los sobrevivientes pueden presentar lesiones negras y ser portadores de por vida. | Uso de cepas libres de patógenos específicos o resistentes a patógenos específicos; lavar y desinfectar huevos y nauplios; limpiar y desinfectar vehículos y equipo contaminado; ahuyentar aves (vectores); destruir el stock y desinfectar totalmente las instalaciones. |
| Necrosis infecciosa hypodermal y hematopoiética (IHHNV), causando Síndrome de Deformidad Runt (RDS) | Parvovirus sistémico | Virus | Baja mortalidad de P. vannamei; resistente; pero hay una reducción en la alimentación y baja eficiencia en alimentación y crecimiento; deformaciones cuticulares (rostrum encorvado – RDS) ocurren en <30 por ciento de la población infectada, mayor variación en el peso a la cosecha final y menor precio de mercado. | Uso de cepas llibres de patógenos específicos SPF y resistentes a patógenos específicos (SPR); lavar y desinfectar huevos y nauplios; desinfección total de las instalaciones de cultivo para evitar la reintroducción. |
| Necrosis Baculoviral de la Glándula Intestinal (BMN); también conocida como enfermedad de la glándula intestinal turbia, enfermedad del hígado blanco turbio o enfermedad turbia blanca. | Baculovirus entérico no ocluído | Virus | Infecta los estadíos larvales y postlarvales, causando una gran mortandad; turbiedad blanca del hepatopancreas causado por necrosis del epitelio tubular; la larva flota inactiva en la superficie; en etapas posteriores muestra resistencia; los reproductores portadores también son una fuente de infección. | Separar los huevos de las heces, lavar huevos y nauplios con agua de mar limpia y desinfectarlos con iodo y/o formalina; desinfectar instalaciones infectadas para evitar nuevos brotes. |
| Vibriosis | Vibrio spp., particularmente V. harveyi & V. parahaemolyticus | Bacteria | Puede causar varios síndromes importantes, tales como luminiscencia y los llamados síndromes zoea-2 y de bolitas. En incubadora, se ve como luminiscencia en el agua y/o cuerpo del camarón; menor alimentación y alta mortandad. En estanques, los altos niveles de vibrios se asocian con la decoloración roja del camarón (especialmente en las colas) y necrosis interna y externa; menor alimentación y mortandad crónica; una segunda infección resultado de un pobre manejo ambiental debilita al camarón, el cual es susceptible de infecciones virales. |
Manejo cuidadoso del sistema. En incubadoras, desinfectar las instalaciones, equipo, agua y trabajadores; utilizar alimentos vivos libres de bacterias; cubrir tanques de cultivo con cubiertas de plástico para evitar la transferencia a los estanques. En estanque, prevenir con preparación apropiada; control de florecimientos algales; agua limpia y manejo de alimento; controlar la densidad de siembra y la aireación para mantener condiciones ambientales óptimas a lo largo del ciclo de cultivo. |
Expertos en patologías
Se puede obtener asistencia de:
-
Prof. Lightner, D.
Aquaculture Pathology Section - Department of Veterinary Science - University of Arizona
Building 90, Room 202 - Tucson, AZ 85721, United States of America
Telephone: (+1) 520 6218414 - Fax: (+1) 520 6214899
E-mail: [email protected] -
Prof. Chen, S.N.
Department of Zoology Director, Institute of Fishery Biology - National Taiwan University
No. 1 Roosevelt Road, Section 4. - Taipei, Taiwan 10764, Taiwan, Province of China
Telephone: (+886) 2 3687101 - Fax: (+886) 2 3687122
E-mail: [email protected] -
Prof. Flegel, T.
Centex Shrimp, Chalern Prakiat Building - Faculty of Science - Mahidol University
Rama 6 Road - Bangkok, 10400, Thailand
Telephone: Personal (+66) 2 2015876 Mobile Phone (+66) 1 4035833 - Office (+66) 2 20158-70 or -71 or -72 - Fax: (+66) 2 2015873
E-mail: [email protected] -
Dr. Walker, P.
Associate Professor and Principal Research Scientist - CSIRO Livestock Industries
PMB 3 Indooroopilly - Queensland - 4068, Australia
Telephone: (+61) 7 32143758 - Fax: (+61) 7 32142718
E-mail: [email protected]
ESTADÍSTICAS
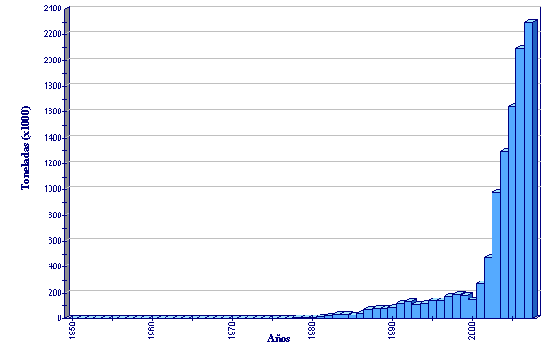
Estadísticas de producción
Producción de acuicultura global de Penaeus vannamei
(FAO Estadísticas pesqueras)
(FAO Estadísticas pesqueras)

Mercado y comercio
Productos
Las presentaciones de congelado con cabeza, sin cabeza y camarón pelado fueron los principales productos de exportación hacia los principales mercados de Estados Unidos de Norteamérica, la Unión Europea y Japón. La actual tendencia es hacia el procesamiento de productos con valor agregado. Ello se debe a la falta de tarifas anti-dumping para productos procesados para el mercado de Estados Unidos, menor afluencia de consumo en restaurantes y la mayor tendencia a consumir productos “listos para cocinarse” o “listos para comerse” a nivel doméstico.
Precios y estadísticas de mercado
El principal mercado del camarón lo constituyen los Estados Unidos de Norteamérica, de quien se esperaba que la importación fuese de aproximadamente 477 000 toneladas con un valor de 3,1 billones de USD en 2005; es decir, 1,8 veces más que las 264 000 toneladas importadas en 2000. Los Estados Unidos, tradicionalmente se abastecían de camarón pequeño congelado o procesado sin cabeza procedente de América Latina. Más recientemente, los Estados Unidos se han tornado a Asia para satisfacer su creciente demanda (1,9 kg/capita en 2004). Los principales proveedores para los Estados Unidos en 2005, fueron Tailandia, Ecuador, India, China y Vietnam. Sin embargo, el rápido incremento de la producción de P. vannamei ha generado una grave caída de los precios en los mercados internacionales. De manera similar, los precios a pie de granja del camarón blanco con peso de 15–20 g ha bajado sistemáticamente de 5 USD/kg en 2000 a unos 3,0 ó 3,5 USD/kg en 2005.
El siguiente mercado más importante lo constituye la Unión Europea (que importó unas 183 000 toneladas durante el primer semestre de 2005), con preferencia por el camarón pequeño (talla 31/40), entero y congelado. Japón, cuyo Mercado prefiere el camarón grande (talla 16/20) sin cabeza, se abastece preferentemente de P. monodonprocedente de las grandes granjas extensivas de Asia.
Regulaciones de mercado
Los estándares de sanidad y el empleo de medicamentos y productos químicos, así como las regulaciones de seguridad alimentaria para los mariscos (particularmente el camarón) son muy elevados en todos los países importadores. Sin embargo, la Unión Europea es aún mas estricta en sus regulaciones (tolerancia cero) en relación a los residuos de productos químicos y antibióticos, así como el Sistema General de Preferencia (GSP) en impuestos de importación. El mercado estadounidense enfatiza más las medidas sanitarias tales como HACCP o Evaluación Sensorial, pero también ha insistido en controles estrictos en relación a los antibióticos prohibidos para el camarón. Desde junio de 2005, se impusieron tarifas antidumping para el camarón cultivado importado por Estados Unidos procedente de 6 países productores de camarón y se fijaron (en términos generales) en aproximadamente 113 por ciento para China, 16 por ciento para Vietnam, 10 por ciento para India, 7 por ciento para Brasil, 6 por ciento para Tailandia, y 4 por ciento para Ecuador. México e Indonesia se libraron de esta imposición de tarifas.
Las presentaciones de congelado con cabeza, sin cabeza y camarón pelado fueron los principales productos de exportación hacia los principales mercados de Estados Unidos de Norteamérica, la Unión Europea y Japón. La actual tendencia es hacia el procesamiento de productos con valor agregado. Ello se debe a la falta de tarifas anti-dumping para productos procesados para el mercado de Estados Unidos, menor afluencia de consumo en restaurantes y la mayor tendencia a consumir productos “listos para cocinarse” o “listos para comerse” a nivel doméstico.
Precios y estadísticas de mercado
El principal mercado del camarón lo constituyen los Estados Unidos de Norteamérica, de quien se esperaba que la importación fuese de aproximadamente 477 000 toneladas con un valor de 3,1 billones de USD en 2005; es decir, 1,8 veces más que las 264 000 toneladas importadas en 2000. Los Estados Unidos, tradicionalmente se abastecían de camarón pequeño congelado o procesado sin cabeza procedente de América Latina. Más recientemente, los Estados Unidos se han tornado a Asia para satisfacer su creciente demanda (1,9 kg/capita en 2004). Los principales proveedores para los Estados Unidos en 2005, fueron Tailandia, Ecuador, India, China y Vietnam. Sin embargo, el rápido incremento de la producción de P. vannamei ha generado una grave caída de los precios en los mercados internacionales. De manera similar, los precios a pie de granja del camarón blanco con peso de 15–20 g ha bajado sistemáticamente de 5 USD/kg en 2000 a unos 3,0 ó 3,5 USD/kg en 2005.
El siguiente mercado más importante lo constituye la Unión Europea (que importó unas 183 000 toneladas durante el primer semestre de 2005), con preferencia por el camarón pequeño (talla 31/40), entero y congelado. Japón, cuyo Mercado prefiere el camarón grande (talla 16/20) sin cabeza, se abastece preferentemente de P. monodonprocedente de las grandes granjas extensivas de Asia.
Regulaciones de mercado
Los estándares de sanidad y el empleo de medicamentos y productos químicos, así como las regulaciones de seguridad alimentaria para los mariscos (particularmente el camarón) son muy elevados en todos los países importadores. Sin embargo, la Unión Europea es aún mas estricta en sus regulaciones (tolerancia cero) en relación a los residuos de productos químicos y antibióticos, así como el Sistema General de Preferencia (GSP) en impuestos de importación. El mercado estadounidense enfatiza más las medidas sanitarias tales como HACCP o Evaluación Sensorial, pero también ha insistido en controles estrictos en relación a los antibióticos prohibidos para el camarón. Desde junio de 2005, se impusieron tarifas antidumping para el camarón cultivado importado por Estados Unidos procedente de 6 países productores de camarón y se fijaron (en términos generales) en aproximadamente 113 por ciento para China, 16 por ciento para Vietnam, 10 por ciento para India, 7 por ciento para Brasil, 6 por ciento para Tailandia, y 4 por ciento para Ecuador. México e Indonesia se libraron de esta imposición de tarifas.
ESTATUS Y TENDENCIAS
Investigación
Algunas de las áreas prioritarias de la investigación relativa al cultivo de P. vannamei son las siguientes:
Dado que el cultivo de P. vannamei se ha expandido rápidamente en los últimos años, particularmente en Asia, el valor del camarón cultivado ha disminuido. Se espera que esta tendencia continúe. Bajo tales circunstancias, los productores menos eficientes no estarán en condiciones de competir con quienes producen camarón ecológico o más económico. Las tendencias mundiales recientes apuntan a la integración de la industria, como respuesta a los requerimientos de trazabilidad y control en los sistemas de cultivo.
Mercado
Los mercados mundiales han mostrado una demanda ligeramente creciente del camarón cultivado, debido al estancamiento de las capturas pesqueras, a la mayor afluencia de la población y a la preferencia por consumir productos saludables. A pesar del aumento en la demanda, el precio de P. vannamei ha bajado continuamente. Se espera que en el futuro, el mercado de P. vannameisea más competitivo, debido principalmente a la saturación de los mercados de exportación y la reducción en el crecimiento económico mundial, así como la imposición de barreras no arancelarias al comercio del camarón. Adicionalmente, la industria deberá satisfacer los requerimientos de los países importadores en los siguientes aspectos:
Todos los productores de camarón están cobrando conciencia de la necesidad de cultivar el camarón de manera responsable, cumplir con la trazabilidad y generar bajos impacto a fin de contribuir a la bioseguridad y a la protección del ambiente, paralelamente a lograr una mayor eficiencia productiva en términos de costo. Los sistemas super intensivos recientemente desarrollados con empleo de flóculos bacterianos podrían tener el potencial de reunir estas características por lo que deben investigarse más a fondo. A fin de que el crecimiento en el cultivo de camarón continúe siendo estable a largo plazo, se requiere promover internamente el consumo de este producto (como en China) para paliar las difíciles circunstancias de los mercados de exportación.
Algunas de las áreas prioritarias de la investigación relativa al cultivo de P. vannamei son las siguientes:
- Continuidad en el desarrollo de las líneas de cepas resistentes a patógenos específicos (SPR) de los virus del P. vannamei incluyendo TSV, WSSV, IHHNV, BMNV y IMNV.
- Desarrollo de líneas SPF y SPR de crecimiento más rápido.
- Desarrollo continuo de sistemas de cultivo bioseguros, de alta densidad y baja salinidad.
- Vacunación y otros tratamientos efectivos contra los virus del camarón.
- Sustitución de insumos no amigables al ambiente y alimentos marinos caros en la producción de alimentos para camarón.
- Sistemas de tratamiento y manejo eficiente del agua para sistemas cerrados de cultivo.
- Técnicas para reducir la carga bacteriana en sistemas de cultivo de camarón.
- Procedimientos efectivos de desinfección de huevos, nauplios y postlarvas en incubadoras.
- Sustitución efectiva de antibióticos (v.gr. probióticos e inmunoestimulantes).
Dado que el cultivo de P. vannamei se ha expandido rápidamente en los últimos años, particularmente en Asia, el valor del camarón cultivado ha disminuido. Se espera que esta tendencia continúe. Bajo tales circunstancias, los productores menos eficientes no estarán en condiciones de competir con quienes producen camarón ecológico o más económico. Las tendencias mundiales recientes apuntan a la integración de la industria, como respuesta a los requerimientos de trazabilidad y control en los sistemas de cultivo.
Mercado
Los mercados mundiales han mostrado una demanda ligeramente creciente del camarón cultivado, debido al estancamiento de las capturas pesqueras, a la mayor afluencia de la población y a la preferencia por consumir productos saludables. A pesar del aumento en la demanda, el precio de P. vannamei ha bajado continuamente. Se espera que en el futuro, el mercado de P. vannameisea más competitivo, debido principalmente a la saturación de los mercados de exportación y la reducción en el crecimiento económico mundial, así como la imposición de barreras no arancelarias al comercio del camarón. Adicionalmente, la industria deberá satisfacer los requerimientos de los países importadores en los siguientes aspectos:
- Residuos químicos.
- Seguridad alimentaria.
- Certificación.
- Trazabilidad.
- Etiquetado de certificación ecológica.
- Sustentabilidad ambiental.
Todos los productores de camarón están cobrando conciencia de la necesidad de cultivar el camarón de manera responsable, cumplir con la trazabilidad y generar bajos impacto a fin de contribuir a la bioseguridad y a la protección del ambiente, paralelamente a lograr una mayor eficiencia productiva en términos de costo. Los sistemas super intensivos recientemente desarrollados con empleo de flóculos bacterianos podrían tener el potencial de reunir estas características por lo que deben investigarse más a fondo. A fin de que el crecimiento en el cultivo de camarón continúe siendo estable a largo plazo, se requiere promover internamente el consumo de este producto (como en China) para paliar las difíciles circunstancias de los mercados de exportación.
PRINCIPALES ASUNTOS
La reciente expansión del cultivo del camarón ha generado muchos debates públicos en torno a los efectos sobre el medio ambiente y su sustentabilidad; los temas de mayor preocupación son:
- Utilización de los ecosistemas de manglares para la construcción de estanques.
- Utilización de estanques por pocos años, bajo el estilo de roza y quema, y su posterior desplazamiento a otras áreas.
- Salinización de las aguas subterráneas y tierras agrícolas.
- Contaminación de aguas costeras por efecto de las descargas de los estanques.
- Sobreuso de harinas de origen marino conduciendo a un aprovechamiento ineficiente de fuentes vitales de proteína y alteración de los ecosistemas marinos.
- Preocupación por la biodiversidad, como resultado de la recolección de semilla y reproductores silvestres e introducción de especies exóticas, así como agentes patógenos asociados.
- Conflictos sociales con otros usuarios de los recursos naturales.
- Descargas de las granjas, causando autocontaminación en las áreas de cultivo de camarón.
Prácticas de acuicultura responsable
Debido a la rápida expansión y a la creciente conciencia de los impactos negativos de las prácticas de cultivo de camarón sobre el ambiente y su propia producción, muchos países productores de camarón están realizando genuinos esfuerzos para cumplir con el concepto de acuicultura responsable, tal como se detalla en el Artículo 9 del Código de Conducta de Pesca Responsable (CCRF) de la FAO. La formulación y adopción de Buenas Prácticas de Manejo “BPM” (Buenas Prácticas Acuícolas – BPA) están empezando a prevalecer en aras de una mayor bioseguridad, incrementar la eficiencia en costos, reducir los residuos de productos químicos e incrementar la trazabilidad. La certificación de cultivo orgánico del camarón se está considerando seriamente. Las normas de HACCP e ISO, ya en práctica en las plantas de procesamiento y alimentos, se están adoptando para las granjas e incubadoras. La FAO y otras organizaciones han desarrollado un sistema de lineamientos y Buenas Prácticas Acuícolas para ayudar a los países productores a cumplir con los diversos aspectos del Código de Conducta de Pesca Responsable CCRF (FAO et.al, 2006).
REFERENCIAS
Bibliograf�a
| Boyd, C.E. & Clay, J.W. 2002. Evaluation of Belize Aquaculture Ltd: A superintensive shrimp aquaculture system. Report prepared under the World Bank, NACA, WWF and FAO Consortium Program on Shrimp Farming and the Environment. Published by the Consortium and obtainable through NACA, Bangkok, Thailand. 17 pp. |
| Briggs, M., Funge-Smith, S., Subasinghe, R. & Phillips, M. 2004. Introductions and movement of Penaeus vannamei and Penaeus stylirostris in Asia and the Pacific. FAO Regional Office for Asia and the Pacific. RAP Publication 2004/10:1–12. |
| Browdy, C.L., Moss, S.M., Lotz, J.M., Weirich, C.R., Otoshi, C.A., Ogle, J.T., Macabee, B.J., Montgomeries, A.D. & Matsuda, E.M. 2003. Recent USMSFP advances in the development of biosecure environmentally sound superintensive shrimp production systems. p. 35 In: Abstracts of Aquaculture America 2003. World Aquaculture Society, Baton Rouge, Louisiana, USA. |
| FAO. 1995. Code of Conduct for Responsible Fisheries. FAO, Rome, Italy. 41 pp. |
| Macabee, B.J., Bruce, J.W., Weirich, C.R., Stokes, A.D. & Browdy, C.L. 2003. Use of super-intensive greenhouse-enclosed raceway systems for the production of juvenile Litopenaeus vannamei. p. 169 In: Abstracts of Aquaculture America 2003. World Aquaculture Society, Baton Rouge, Louisiana, USA. |
| Parker, J.C., Conte, F.S., MacGrath, W.S. & Miller, B.W. 1974. An intensive culture system for penaeid shrimp. Proceedings of the World Mariculture Society, 5:65–79. |
| Pérez Farfante, I. 1969. Western Atlantic shrimps of the genus Penaeus. Fishery Bulletin, 67(3): 461–591. |
| Pérez Farfante, I. & Kensley, B. 1997. Penaeoid and sergestoid shrimps and prawns of the world. Keys and diagnoses for the families and genera. Memoires du Museum National d'Historie Naturelle, Paris, France. 233 pp |
| Samocha, T.M., Lawrence, A.L., Collins, C.A., Castille, F.L., Bray, W.A., Davies, C.J., Lee, P.G. & Wood, G.F. 2004. Production of the Pacific white shrimp, Litopenaeus vannamei, in high-density greenhouse enclosed raceways using low-salinity groundwater. |
| Taw, N. 2005. Indonesia Shrimp Production. Presented in the Indonesian shrimp farmers session of World Aquaculture 2005, May 9–13, 2005, Nusa Dua, Bali, Indonesia. Charoen Pokphand, Jakarta Indonesia. 18 pp. |
| Wyban, J.A. & Sweeney, J.N. 1991. Intensive shrimp production technology. High Health Aquaculture, Hawaii, USA. 158 pp. |