El estudio de los problemas patológicos en cultivos de camarón concierne diferentes aspectos de profilaxia general, de terapia, y de diagnósticos.
El informe de M. Weppe reune las recomendaciones teóricas en este campo. Además, durante la asesoría anterior de cría larval, una parte del trabajo fue dedicada a los estudios bacteriológicos en el Centro de Tunas, así como también a los aspectos importantes de gestion sanitaria y a la determinación de enfermedades de las larvas.
El presente trabajo reune los resultados logrados en bacteriología hasta Octubre 1990 y las recomendaciones para continuar el estudio en patología.
Medios utilizados : agar-nutrientes 2 % NaCl y TCBS para la numeración de bacterias, Mueller/Hinton para antibiogramas. Conseguir absolutamente el medio Zobell apropiado a las bacterias marinas, TCBS y Mueller/Hinton en mayor cantidad para poder trabajar.
Aqua-plak : se recomienda usar todas estas placas de numeración bacteriana (material Sanofi) inmediatamente, antes de la fecha de vencimiento de los reactivos. Las Aqua-plak son muy útiles para el seguimiento diario de todos los tanques de crías larvales.
Durante la asesoría, se efectuaron numeraciones de bacterias en todos los medios 1 a 2 veces por semana y también la compilación de todos los datos desde Mayo 1990. Con esta compilación se llegó a las observaciones presentadas a continuación.
Evolución en el tiempo - mes de Octubre/90 : (véase gráfico no1 pág. 14).
GRAFICA No 1 : Evolucion en el tiempo de las colonias bacterianas (mes de octubre 90)
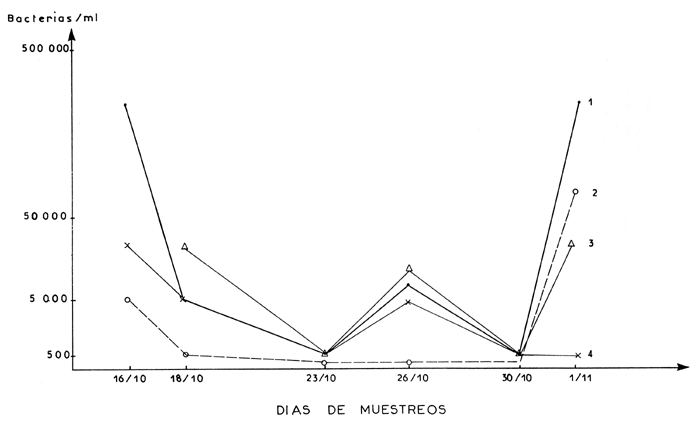
Bacterias totales cisternas 
Vibrio cisternas o-----
Bacterias totales redes de cría larval  ——
——
Bacterias totales redes de agua U.V x——
Se pueden observar :
Fluctuaciones muy importantes en el tiempo, en cuanto a la cantidad total de bacterias de los reservorios de agua de mar. Esto, está relacionado con el ritmo irregular de limpieza en el mes de Octubre. Se debería también averiguar si existe una correlación con la calidad del agua del medio natural ; posible contaminación en la zona de la toma de agua debido a la proximidad de una procesadora pesquera.
Niveles altos de bacterias totales en las cisternas (hasta 500 000 bact./ml), o sea, 100 veces más elevados que en el mes de mayo (véase cuadro no2 pág. 16). Se señala nuevamente la falta de rigor en la limpieza y también la falta de cloro desde hace dos meses para lavar.
Las cantidades de colonias TCBS/ml son más estables (promedio de 500 a 5 000 col/ml), sin embargo son 10 veces más altas que en Mayo.
La flora bacteriana en las redes de cría larval sigue lógicamente la evolución general en el medio. En cambio, se nota una disminución importante de la cantidad de bacterias en las redes, algas y desove (500 a 5 000 bact./ml - TCBS < 500/ml), debida al efecto de las lámparas U.V.
Concentraciones bacterianas más bajas en los sedimentadores que en las cisternas de agua filtrada con filtros de arena y cartuchos (8 micrones) : ¿ Dudas sobre la limpieza de los filtros de arena y cartuchos y el cambio de estos cartuchos ?
Datos promedios : (véase cuadro no2 pág. 16).
En Octubre, las cantidades de colonias TCBS/ml son muy elevadas para los estadios jovenes de larvas en Octubre (más de 100 000 Vibrio/ml en unas muestras). Cantidades hasta 20 000 Vibrio/ml son aceptables para los estudios protozoea.
Debido a la contaminación del agua de mar en las cisternas, se observa un ensuciamiento general del medio de cría larval, lo que constituye un peligro grave para el buen desarrollo de las crías.
Cuadro no2 : Comparación de las cantidades promedios de colonias bacterianas/ml en diferentes épocas del año.
| MUESTREOS DEL AGUA DE | ANO 1990 | ||||
|---|---|---|---|---|---|
| MAYO | JUNIO A AGOSTO | OCTUBRE | |||
| Bact. totales/ml | TCBS/ml | Bact. totales/ml | Bact. totales/ml | TCBS/ml | |
| Sedimentodores | 2 000 | < 500 | 2 000 | 50 000 | 500 |
| Cisterna arena | 2 000 | < 500 | 4 000 | 150 000 | 50 000 |
| Cistern cartuchos | 1 500 | < 500 | 3 000 | 150 000 | 10 000 |
| Redes de algas | 200 | 0 | 1 400 | 3 000 | 500 |
| Redes de desove | 34 000 | 2 500 | 500 | ||
| Algas : | |||||
- Chaeto 52 | 50 | 0 | 28 000 | 0 | 0 |
- Chaeto 1 m3 | 10 000 | 0 | 10 000 | 15 000 | 2 000 |
| Larvas : | |||||
- Nauplii | 150 | 5 000 | 50 000 | 20 000 | |
- Z1 | 2 000 | 41 000 | 100 000 | 100 000 | |
- Z2 | 10 000 | 5 000 | 30 000 | 100 000 | 5 000 |
- Z3 | 50 000 | 5 000 | 50 000 | 400 000 | 400 000 |
- M1 M2 | 50 000 | 50 000 | 100 000 | 500 000 | 500 000 |
- M3 | 500 000 | 500 000 | 400 000 | ||
Generalmente, existe una buena correlación entre los resultados sobre el Aqua-plak y las cajas de Petri. Con excepción de los volumenes interiores de algas :
Contaminados, según el crecimiento importante en agar-nutrientes.
Limpios, según la Aqua-plak.
Una preparación de muestras en el medio Zobell podría comprobar este resultado. Los tanques de Chaetoceros de 1 m3 presentan cantidades altas de bacterias/ml y presencia de Vibrio. Continuar la flora TCBS de estos tanques luego de haber limpiado a fondo con cloro las cisternas y redes.
Antibiogramas :
La lectura indicó una resistencia a la eritromicina de las colonias presentes en el agua de tanques de eclosión, larvas y artemia y una sensibilidad al efecto del cloranfenicol de todas estas colonias. Se vuelve a mencionar la inutilidad del tratamiento diario con la eritromicina efectuado en los tanques de desove y de eclosión.
Se deben seguir los muestros al ritmo planteado en la misión anterior, para cumplir las numeraciones bacterias y efectuar antibiogramas.
Seguir la identificación visual de las diferentes colonias de bacterias, para controlar el equilibrio y la diversificación de la flora.
Un programa de identificación bioquímica de las cepas aisladas en el centro, debería empezar con el apoyo del laboratorio de investigación de la Habana, o, con envios de muestras al Aqua-Cop (centro IFREMER en Tahiti).
Es primordial analizar los datos enseguida para sacar provecho de los estudios realizados, lo que permite seguir la evolución general de la flora bacteriana y enfocar inmediatamente los problemas en la producción o, en la calidad sanitaria del medio (ejemplo del problema de calidad del agua en Octubre). Así se puede hablar de prevención.
El control de todas las normas de profilaxia planteadas para todos los departamentos, forma parte de las prioridades de trabajo en el servicio de patología.
En la cría larval :
Las observaciones diarias de las larvas permiten una intervención rápida en caso de problemas patológicos, con tratamientos curativos de cloranfenicol (bacterias), o de verde de malachita (hongos).
Faltan todavía la furazolidone (antibiótico necesario para un tratamientos preventivos) y el treflan.
En maduración :
La observación de los progenitores al llegar al departamento, permite descartar los animales con necrosis, hongos, microsporidias. En caso de mortalidad, buscar siempre en el hepatopancreas la presencia eventual del baculovirus (BP).
En engorde :
Se debe seguir el análisis bacteriológico del agua de entrada a los estanques para determinar las variaciones de su calidad.
En caso de mortalidad inexplicable, se tomarán muestras de animales para el estudio histológico a fin de diagnósticar la aparición de una contaminación viral.
En las hojas de recomendaciones entregadas al personal, se detallan los medios de conservación de muestras de bacterias o animales, la metodología, asi que unas coloraciones para la identificación de los cuerpos de inclusión virales (véase anexo 2).
Cabe decir, que el servicio de patología del centro de desove de Tunas de Zaza, tiene ahor a su disposición una gran cantidad de datos y de informes sobre la evolución de la flora bacteriana desde el mes de Mayo 1990.
Conservando la rutina de muestreos y con la identificación de cepas y los muestreos para el estudio histológico, el trabajo estará realmente completo.
Ahora una continuidad en el trabajo es necesaria, así que una mejor repartición de las tareas entre los técnicos del departamento.