L'approvisionnement en eau est un élément essentiel de la ferme aquacole d'eau douce ou salée.
L'évaluation des besoins en eau par rapport à un objectif de production, la connaissance du potentiel en eau naturelle, la coût de la valorisation de ce potentiel : pompage, recyclage, chauffage, etc… autant de démarches, que l'entrepreneur aura à effectuer s'il veut minimiser les risques et optimiser la rentabilité de son affaire.
L'eau est nécessaire comme :
Milieu d'élevage: un volume d'eau minimum doit être conservé pour permettre la vie des animaux. L'évaporation, les infiltrations tendent à réduire ce volume.
Transporteur d'oxygène : les animaux utilisent de l'oxygène dissous, celui-ci est emprunté au milieu extérieur, ou produit dans l'élevage à partir d'oxygène de l'air ou d'oxygène industriel.
Transporteur de résidus alimentaires ou de produits du métabolisme : ces déchets sont évacués dans le milieu extérieur ou détruits à l'intérieur de l'élevage (épuration).
Transporteur de calories: pour éviter l'échauffement des bassins, le maintien d'un débit d'eau important peut être requis (cas de certains étangs tropicaux). En écloserie, ou recherche au contraire à limiter le débit d'apport pour éviter les dépenses d'énergie liées au refroidissement (stockage de géniteurs) ou au chauffage (incubation et alevinage).
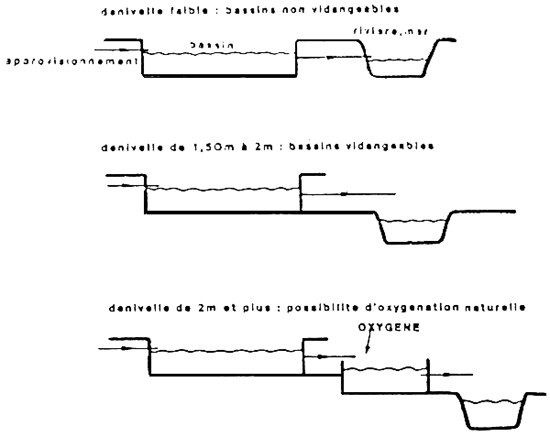
On constate ainsi que seule la fonction № 1: l'apport d'eau pour compenser les pertes, nécessite toujours une source d'eau naturelle (fig. 1).
Les fonctions d'oxygénation, d'épuration, de thermorégulation peuvent toutes s'effectuer à l'INTERIEUR de l'élevage, sans appel au milieu naturel (fig. 2):
- soit par équilibre biologique dans l'élevage, c'est le cas d'un ETANG,
- soit par une machinerie, qui assure ces fonctions : c'est le cas d'une ECLOSERIE en CIRCUIT FERME.
Signalons enfin que l'eau peut être un transporteur de nourriture. Dans les élevage de bivalves, par exemple, cette fonction peut être déterminante pour la détermination de besoins en eau.
L'évaluation du potentiel en eau d'un site aquacole dépend donc :
- des capacités du site à remplir une ou plusieurs des fonctions décrites ci-dessus,
- du niveau d'investissement et du coût de fonctionnement, en matériel de traitement d'eau, compatibles avec la rentabilité de l'affaire.
L'analyse de ce potentiel en eau suppose donc que l'on connaisse les cycles de production (en fonction du marché) qui peut être envisagé.
De ces cycles de production découleront un certain nombre de valeurs de stocks à maintenir, ce sont elles qui détermineront les besoins en eau à satisfaire. On déduit ainsi, pour un site donné, le degré de mécanisation (d'investissement) à assurer pou le poste “EAU”
Les besoins en eau varient considérablement avec le mode de nourissage et par conséquent avec la croissance des animaux.
Sachant que les fonctions 1 et 2 (maintien du volume, fourniture d'oxygène sont nettement moins coûteuses à mécaniser que les fonctions 3 et 4 (transport des résidus, thermorégulation) on aura intérêt à étudier des cycles de production avec différentes stratégies de nourrissage.
| EXEMPLE: | Le point de blocage d'un système d'élevage pour sa rentabilité est l'oxygène disponible en été (soit du fait du débit limité ou de la température élevée, ou encore du fait des deux facteurs conjugués). |
| Solution 1 - | Vente du stock avant l'été (pas d'investissement supplémentaire) |
| Solution 2 - | Oxygénation + nourrissage à la ration minimale (maintien en poids du stock, sans croissance). Cette solution permet de maximaliser le stock conservé pendant l'été, (en vue d'une vente à des cours intéressants en automne par exemple). L'aliment n'est pas rentabilisé au niveau de l'indice de transformation (gain de poids nul). |
| Solution 3 - | Oxygénation + nourrissage à un taux supérieur à la ration minimale, donnant lieu à la croissance du stock. Cette solution obilge à réduire le stock (consommation d'oxygène, autopollution), mais permet d'amener les animaux à la taille recherchée. Elle rentabilise mieux le poste aliment que la solution précédente. |
| Solution 4 - | Oxygénation + épuration de l'eau + nourrissage Le stockage est maximum et la croissance est maintenue. Cette solution, très coûteuse en investissement, reste possible sur de petites unités et sur un poste particulier de l'élevage (écloserie, stockage de géniteurs). |
Le maintien du volume d'élevage suppose le maintien d'un débit compensant les pertes naturelles (évaporation et infiltration) et volontaires : renouvellements d'eau dus aux traitements sanitaires, aux nettoyages des installations, etc…
Le choix des structures (bassins en terre, en béton), la possibilité de couverture, les facilités d'isolement hydraulique des différentes parties de l'installation, influeront sur les besoins.
Les valeurs à affecter à ces différents types de pertes sont à collecter sur place pour chaque site : elles dépendent en effet des caractéristiques climatiques et pédologiques locales (température, hygrométrie, couleur des eaux, perméabilité, etc…)
En tant que transporteur d'oxygène, nous aurons à déterminer deux paramètre de l'eau de l'élevage :
- La quantité d'oxygène qu'il sera nécessaire d'introduire dans l'eau pour satisfaire les besoins des animaux, (et éventuellement l'oxydation des déchets). en terme de flux de gaz (Kg d'oxygène par heure),
- la teneur en oxygène à maintenir pour le confort des animaux (seuil en dessous duquel la croissance, l'indice de transformation, la reproduction sont perturbés), il s'agit alors d'une concentration (gramme d'oxygène par mètre cube d'eau).
Ces deux paramètres varient avec l'espèce, la taille, la température, l'alimentation et l'activité des animaux. Leur calcul va servir à dimensionner l'ensemble du système d'oxygénation, qui comporte :
- l'eau d'apport
- les dispositifs et machines de production d'oxygène dissous.
A un instant donné, le système d'oxygénation de l'élevage aura une capacité maximale d'oxygénation fixe, correspondant aux investissements que l'on aura jugé utile de faire pour le poste “oxygène”.
Face à cette capacité fixe on aura une demande en oxygène variable du fait de l'alimentation et d l'activité des animaux, des teneurs en oxygène à maintenir variables suivant les bassins du fait des différences de tailles des animaux.
Le dimensionnement du dispositif d'oxygénation se fera donc généralement à partir de la connaissance :
- de la moyenne sur 24 H, de la demande en oxygène,
- des bassins instantanés maximum liés au nourrissage.
On admet que la capacité d'oxygénation du système doit couvrir la totalité des besoins moyens, et dans une proportion moindre les besoins instantanés maximum (ce qui implique qu'on admet des baisses de la teneur en oxygène dans les bassins).
En effet, le coût des installations nécessaires pour couvrir la totalité des besoins en oxygène, représente souvent un investissement non rentable et n'est pas justifié par une amélioration significative des résultats d'élevage (mortalités, indice de transformation, croissance).
Besoins moyens: Annexes I
La plupart des modèles de calculs se basent sur la taille des animaux et la température de l'eau pour évaluer la demande moyenne en oxygène.
Comme ces deux paramètres servent également à déterminer la ration alimentaire, il est possible, dans un élevage nourri, d'évaluer la quantité d'oxygène à fournir à partir de la quantité d'aliment distribué.
Ainsi pour un aliment type “Truite” (40 % de protéines) on constate qu'il faut 300 g d'oxygène dissous par kilo d'aliment.
Besoins instantanés
Le mode de nourrissage est souvent déterminant sur les fluctuations journalières de la demande en oxygène. (fig. 3)
La comparaison de la concentration d'oxygène des bassins suivant que le nourrissage a été fait manuellement, en libre service, rationné ou non, met en évidence le phénomène (FAURE, 1983) fig. 4).
La conception du planning de nourrissage est donc à faire en concordance avec le dispositif d'oxygénation.
Contrairement aux élevages terrestres, les déchets de nourriture et les déjections des animaux ne sont pas captables à l'émission dans un élevage aquatique.
Ces déchets sont immédiatement dilués dans le milieu et peuvent donc, s'ils ne sont pas éliminés s'y accumuler et perturber les animaux.
Eliminer les déchets suppose un déchets suppose un débit d'eau évacuant ceux-ci à l'extérieur, combiné ou non à des dispositifs d'épuration.
Les besoins en eau et l'importance des dispositifs d'épuration vont dépendre de la teneur en polluants qui peut être considérés comme admissible dans l'exploitation, en terme de mortalités, d'indice de transformation et de croissance.
Comme pour l'oxygène un premier dimensionnement pourra être établi à partir de la composition moyenne du rejet des bassins sur 24 h., dimensionnement qui pourra être affiné à partir de la connaissance des fluctuations journalières et des valeurs maximales de pollution.
Les expériences menées en trutticulture montrent qu'il est acceptable et plus simple de calculer la pollution à partir des quantités d'aliments déversés dans les bassins.
A titre indicatif, voici les valeurs obtenues avec de l'aliment type “truite” (aliment sec, 40 – 45 % de protéines) d'après FAURE (1983)
AMMONIAC : (NH3 + NH4) = 0,03 A × Ks.
Ks, facteur compris entre 1 et 2 lorsque l'on dépasse 1 mg/1 d'ammoniac dans l'eau. Ks est un facteur prenant en compte le fait que la présence d'ammoniac au dessus de 1 mg/1 entraîne augmentation de la production d'ammoniac par Kg de truites.
Calcul de Ks ou coefficient de stress : ce coefficient est calculé à partir du nombre de réutilisation de l'eau.
Ks = 0,875 + 0,125 N
N, nombre de réutilisation de l'eau après désoxygénation.

La quantité de matières solides émises varie fortement avec l'indice de conversion de l'aliment.
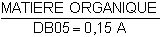
DCO = 3,7 DBO5
Pour l'évaluation des redevances à la pollution le calcul est fait à raison de :
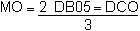
PHOSPHATES PO4 = 0,014 A
PT (phosphate total) = 0,025 A
Note : Ces résultats diffèrent sensiblement de ceux obtenus auparavant aux U.S.A. KRAMER, CHIN and MAYO, 1972).
Ces relations sont valables pour des animaux nourris avec rationnement.
Les cas des animaux en période de jeûne, et des animaux soumis à une suralimentation devra être traité séparément.
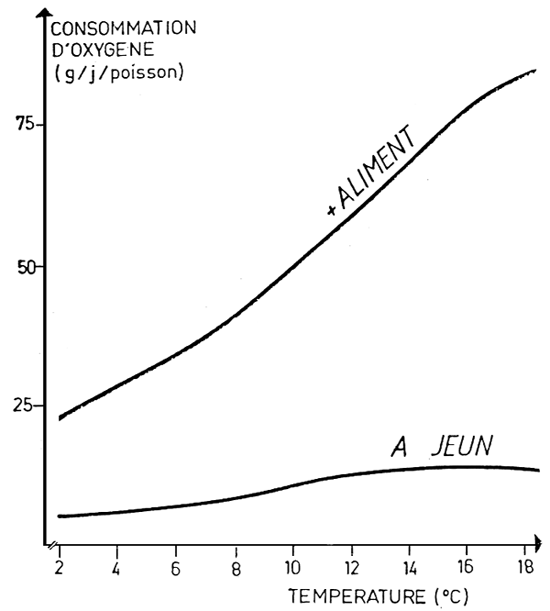
Ainsi l'excrétion azotée est 3 fois plus élevée pour un poisson après alimentation, que pour un poisson à jeun. (KAUSHIK, 1980) fig. 5 – 6.
La température de l'eau est toujours un facteur coûteux à maîtriser.
Le contrôle de la température se limite généralement à l'eau alimentant l'écloserie avec trois circuits distincts :
Les bassins de stockage des géniteurs(à refroidir)
Cette pratique de développe en salmoniculture pour les reproducteurs soumis à un conditionnement photopériodique destiné à obtenir des pontes d'été.
Le stockage des géniteurs de turbots, daurades et loups pose des problèmes similaires (perturbation de la maturation des gamètes à températures excédant 10 – 15° C suivant les espèces).
Les écloseries, c'est à dire les installations recevant les oeufs et les alevins, AVANT nourrissage. Le chauffage ou le refroidissement peuvent être recherchés.
Les stations d'alevinage avec nourrissage, où l'on recherche une accélération de la croissance par chauffage de l'eau.
Le contrôle de la température est atteint avec des conditions économiques acceptables dans le cas des eaux réchauffées de centrales. Lorsque le traitement thermique s'effectue dans l'exploitation piscicole, un recyclage intensif des calories ou des frigories est nécessaire, ce qui implique des dispositifs d'épuration coûteux, soit pour regénérer la qualité de l'eau d'élevage (recyclage), soit pour protéger les échangeurs de l'encrassement par les salissures de l'élevage (cas des échangeurs entrée-sortie).
La conception du chauffage de l'eau doit en outre prendre en compte les problèmes de stress thermique, et de sursaturation en gaz.
L'évaluation des quantités d'oxygène et de calories à fournir, et de la quantité déchets à évacuer, permet de déterminer les débits d'eau requis, et la machinerie à acquérir et donc d'avoir un ordre de grandeur de l'investissement.
Le choix du site et du matériel suppose la connaissance précise des caractéristiques physico-chimiques que l'on souhaite voir maintenues au niveau de l'eau des bassins.
Les paramètres mesurables ou calculables avec des moyens relativement simple sont au nombre de 10 : la température, l'oxygène, l'ammoniaque, les nitrites, les nitrates , le pH, le gaz carbonique, l'alcalinité), (la dureté), les matières en suspension et la matière organique. Pour les eaux salées, il s'y ajoute la salinité.
D'autres paramètres sont à contrôler lors de l'évaluation du site : polluants de toute nature, métaux lourds, etc…
Les dix paramètres cités précédemment sont ceux qui intéressent tous les aquaculteurs en routine.
Si l'on est amené à fournir mécaniquement une quantité déterminée d'oxygène (Kg/H), le coût du Kg d'oxygène fourni sera d'autant plus élevé que la teneur en oxygène dans les bassins sera élevée.
Ceci tient au rendement décroissant des appareils d'aération, lorsque la concentration en oxygène dissous s'élève (voir plus loin).
En terme de rendement énergétique de l'appareillage, on a donc intérêt à choisir la valeur la plus basse possible.
Mais d'autres critères interviennent et l'on peut résumer les critères de choix de la manière suivante (fig 7).
- seuil de résistance:
ex : 2,5 – 3,0 mg/1 pour la truite
1,0 – 2,0 mg/1 pour le bar
Des mortalités importantes sont constatées à ces teneurs. Elles sont en principe incompatible avec l'élevage.
Elles représentent les valeurs minimales qui peuvent être tolérées sur des périodes transitoires (post alimentation par exemple).
- seuil de dépendance physiologique :
ex : 5,0 – 5,5 mg/1 pour la truite
3,0 – 4,0 mg/1 pour le bar
Des teneurs inférieures à ce seuil entraînent une diminution de croissance et une augmentation de l'indice transformation. L'animal réduit sa consommation d'oxygène.
Le maintien de telle teneur ne permet généralement pas un nourrissage important. Seul le coût très élevé de l'oxygénation peut conduire à conclure qu'il est plus rentable de travailler à des teneurs en oxygène dissous, inférieures à ce seuil.
- seuil de dépendance alimentaire:
ex : truitelles : 8,0 mg/1
Il existe peu d'expérience ayant permis de fixer ce seuil pour différentes espèces.
Il semble que lorsque l'on nourrit abondamment les animaux, soit plus de 60 % de la quantité maximale qu'ils auraient pu ingérer, on soit amené à relever la teneur en oxygène dissous des bassins si l'on veut éviter une baisse de l'efficacité alimentaire (augmentation de l'indice de transformation).
On détermine ainsi qu'il existe un optimum économique entre les dépenses d'aliment, qui augmentent lorsque le taux d'oxygène baisse, et les dépenses d'électricité liées à l'aération, qui augmentent lorsque le taux d'oxygène augmente.
Le contrôle de l'oxygène dissous se fait par dosage ou plus facilement à l'aide de sonde (600 à 1 200 $).
La température intervient dans tous les processus physiologiques : la croissance, les besoins alimentaires, la consommation d'oxygène augmentent avec la température.
Pour chaque espèce, il existe une température optimale.
Le chauffage ou le refroidissement visent à rétablir cette température. il s'agit en général d'aboutir à un contrôle de la vitesse de croissance des juvéniles ou encore à obtenir la maturation des géniteurs.
Une autre circonstance où intervient la prise en compte de la température est lors du transfert des animaux avec changement de température.
En règle générale, le choc thermique sera bien supporté si l'on reste dans la plage de température encadrant la température optimale.
Pour les températures extrêmes, les temps d'acclimatation seront d'autant plus longs que l'on s'éloigne de la température optimale (fig. 8).
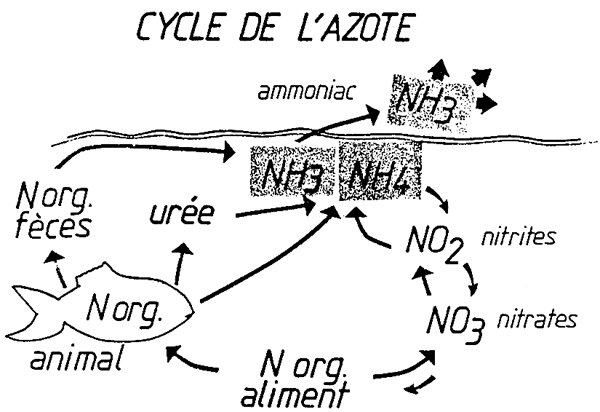
L'ammoniaque (NH4 OH) se présente dans l'eau sous forme d'ion ammonium (NH4 +) ou de gaz dissous (NH3).
Le suivi en élevage se fait à l'aide d'analyses basées sur des réactions colorimétriques dont la mesure est faite, à l'oeil pour les “trousses” (70 à 100 $), ou avec un colorimètre ou un spectrophotomètre (1 000 à 1 500 $).
La mesure effectuée donne une valeur exprimée en poids d'azote, ou en poids d'ammoniaque (la confrontation avec les valeurs seuils admises en élevage doit se faire en concordance avec le mode d'expression du résultat).
Cette valeur est toujours la sommation de l'ammoniac gazeux et de l'ion ammonium.
Pour la conduite de l'élevage, nous utiliserons :
La valeur ammoniac (NH3) + ion ammonium (NH4 +) comme indicateur général de pollution et de bon fonctionnement de l'élimination des déchets.
Des bassins correctement drainés ou épurés auront une eau qui oscille entre 0,5 et 2,5 mg/1 de (NH3 + NH 4 +).
La sensibilité des poissons eux-mêmes varie suivant l'espèce et les résultats sont très différents selon que les tests ont lieu en laboratoire avec l'ammoniaque seule ou en bassins avec un environnement complexe (MES, CO2, etc… ).
Ainsi la truite présenterait un état de stress dès 1 mg/l; alors que l'anguille serait peu sensible à l'ammoniaque.
La valeur en ammoniac non ionisé (NH3)
Sa toxicité est notoire pour à peu près toutes les espèces.
Les seuils sont de l'ordre de 2,10-3 mg/l à 5,10 -2 mg/l suivant la taille des animaux et les espèces. (tableau) HAYWOOD G.P. (1983) a fait une synthèse des seuils à prendre en compte.
La valeur d'ammouniac dissous (NH3) s'obtient par calcul à partir des valeurs de température, de pH et d'ammoniaque total (fig. 9).
Suite à une intoxication à l'ammoniaque, il est souhaitable pour une bonne récupération des animaux en eau fraîche de porter la température à 10° C au moins, et d'assurer une bonne oxygénation.
Les nitrites sont toxiques en eau douce à des doses de 0,015 à 0,2 mg/1.
Comme pour l'ammoniaque, la dissociation de deux espèces chimiques est à prendre en compte.
L'ion nitreux No2 - (mesuré en poids de l'azote ou en poids de No2) et l'acide nitreux (H No2) sont présents, mais dans la gamme de pH intéressant les élevages de poissons seul NO2 l'est en proportion significative.
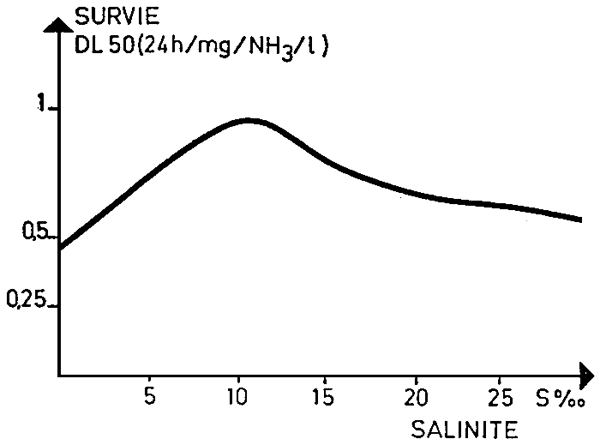
La toxicité de NO2 diminue lorsque le pH augmente (à l'inverse de H No2). Elle diminue aussi avec la salinité (présence de chlorure) d'où son importance moindre en eau de mer.
Les nitrates ne sont pas toxiques. Ils servent d'indicateurs pour le fonctionnement des systèmes d'épuration à base de filtre biologique. Les renouvellements minimum obligatoires limitent leur accumulation des valeurs de 50 – 150 mg/l.
La chevrette (Macrobrachium rosenbergii) serait incommodée à partir de 175 mg/l.
Les équilibres calco-carboniques sont très importants en milieu aquatique. Le pH est déterminant pour la toxicité de l'ammoniaque, des nitrites et du CO2.
Pour suivre l'évolution de ces facteurs les mesures simples dont dispose l'éleveur de poissons sont les suivantes :
- mesure du pH (par colorimétrie ou à l'aide de sonde, (coût 200 $).
- mesure de la dureté (colorimétrie)
La concentration de gaz carbonique peut être alors calculée de façon simple (fig. 10) en admettant que l'on n'a que des bicarbonates (et pas de carbonates) ce qui est justifié jusqu'à pH 8,3.
La concentration de gaz carbonique ainsi calculée est celle que l'on aurait à l'équilibre, elle peut être supérieure si l'aération (stripping du CO2 agressif) est insuffisante.
Le CO2 se comportant comme un acide, il influe sur le pH (fig. 11). Sa toxicité dépend étroitement du pH.
En pratique, on tiendra compte ainsi,
1) de l'accumulation de CO2 en milieu confiné (cuve de transport par exemple). Dans ce cas, l'aération peut être suffisante pour l'oxygénation, mais insuffisante pour éliminer le CO2.
On a alors accumulation de CO2 et diminution du pH. La toxicité du CO2 commence dès 9 – 10 mg/l à pH 5. (contre 20 mg/l à 6,0 et 100 mg/l au dessus de pH 7,0) Ce phénomène est lié à la respiration des poissons (44 g de CO2 produit pour 32 g d'oxygène consommé), et des plantes (la nuit essentiellement).
2) des remontées brutales de pH qui peuvent entraîner des intoxications à l'ammoniac, et qui se produisent lors des mises en route d'installation d'aération, ou du fait de la présence de plantes qui consomment le CO2 (photosynthèse le jour). (fig. 12)
La présence de MES peut être liée aux apports amont (sable) ou à une production in situ dans l'élevage.
Une bonne gestion de l'alimentation réduit considérablement les MES. (FAURE, 1983).
Leur toxicité directe est généralement, faible, par contre, ils induisent des problèmes pathologiques, tels que les attaques des branchies des alevins par myxobactéries.
Ils influent sur l'élevage de différente manières :
- si l'eau est trouble, la prise de nourriture peut être affectée, ce qui réduit l'efficacité alimentaire et accroit la pollution.
- Ils peuvent donner lieu à l'apparition d'algues microscopiques donnant une saveur désagréable à chair du poisson.
- Ils perturbent le fonctionnement des filtres biologiques destinés à la nitrification. En effet, aux particules carbonnées qui les composent sont associées des espèces bactériennes dominantes par rapport aux bactéries assurant la nitrification.
- enfin ils polluent l'environnement à la sortie des élevages
Pour toutes ces raisons, l'équipement en ouvrage de piégeage des MES est souvent nécessare.
L'essentiel des aménagements a été par diapositives. Nous ne reprendrons donc pas dans cet exposé l'étude cas par cas du matériel, ce qui demanderait un temps dépassant le cadre imparti.
Nous étudierons les principes mis en oeuvre, en vue de proposer une méthode de choix basée sur les objectifs d'élevage, exposés précédemment, et les performances du matériel.
Les techniques en cause sont:
L'équipement de la prise d'eau : on se reportera à l'annexe 2
L'aération et l'oxygénation
L'épuration de l'eau
la stérilisation de l'eau.
Ces techniques concernent :
- tous les élevages (1).
- le grossissement du poisson en bassins, et à moindre degré en cages (2),
- les écloseries et stations de production des juvéniles (2) (3) (4).
Nous réserverons le terme “Aération” aux procédés utilisant l'air, et le terme “Oxygénation” aux appareils utilisant l'oxygène industriel.
L'aération est un poste énergétique important en élevage intensif : 13 – 15 % pour grossissement de truites en bassin, 23 % dans une station d'alevinage (ALAVOINE - 1981).
Le coût et l'importance que devra lui accorder l'exploitant varieront d'un pays à l'autre suivant la législation fixant la prix de l'énergie.
ex. : En France, l'aération des bassins de grossissement n'est pas un facteur économique déterminant : le prix du Kw/h d'été est faible. Inversement, l'implantation d'une écloserie fonctionnant l'hiver devra être étudié : le prix du Kw/h d'hiver est en effet élevé.
L'objectif de l'aération est de faire passer de l'oxygène gazeux contenu dans l'air à l'état dissous, seule forme utilisable par la plupart des poissons.
L'utilisation de l'air comporte un avantage important : il est gratuit
A cet avantage, s'associent deux inconvénients :
- L'air ne contient que 21 % d'oxygène,
- L'air contient 78 % d'azote.
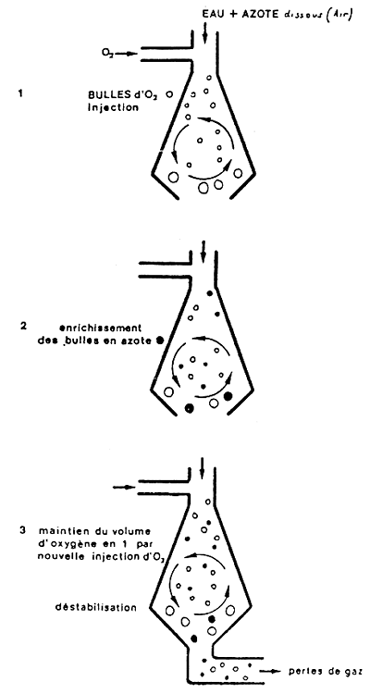
En conséquence, l'appareil devra être efficace, puisqu'il travaille avec un gaz pauvre en oxygène, mais pas “trop efficace”, car il peut alors dissoudre une quantité importante d'azote. La quantité de gaz dissous est alors telle que l'on a “sursaturation”. c'est à dire que la pression des gaz dissous est supérieure à celle du gaz au contact de l'eau, entrainant des phénomènes d'embolie gazeuse dans le cheptel.
La dissolution d'oxygène résulte d'un ensemble de phénomènes, dont chacun d'eux est utilisé de façon plus ou moins importante suivant les procédés (fig. 13).
1) “Enrichissement” de l'air à l'aide d'oxygène industriel,
2) agitation de l'interface gaz-liquide: en effet, il existe un “film” s'opposant au passage des gaz dont l'épaisseur diminue avec l'agitation.
3) temps de contact gaz-liquide: plus les bulles resteront longtemps dans l'eau ou les gouttelettes d'eau dans l'air, plus l'oxygénation sera importante.
4) Surface de contact gaz-liquide: plus les bulles ou les gouttelettes seront petites, plus l'efficacité du dispositif sera grande.
5) Pression du mélange diphasique: le fait de préssuriser le mélange d'eau et d'air augmente les échanges (attention aux sursaturations).
6) Renouvellement de l'eau dans le volume de travail de l'aération: plus le renouvellement sera important plus le rapport Kg d'o2 dissout produit/Kw/h dépensé sera important, mais dans le même temps le rapport Kg d'O2 dissous/m3 d'eau (concentration) diminue. La prise en compte de ce facteur a lieu lors de l'utilisation de l'appareil et dépend donc de l'installation réalisée par l'éleveur.
L'annexe 3 donne l'expression mathématique de ces phénomènes.
La détermination du résultat obtenu en bassins pour un procédé donné dépend de nombreux facteurs, nous proposons ci-dessous un système d'évaluation simplifié, qui, à notre avis suffit souvent en aquaculture.
L'aquaculteur devra se procurer ou déterminer:
- auprès du constructeur de l'appareil ou du concepteur du procédé deux caractéristiques générales: l'apport spécifique brut (ASB) et la capacité d'oxygénation standard (COS). La première caractéristique s'exprime en kg d'O2/H
- La température et la salinité de l'eau à aérer,
- une table de saturation en oxygène, en fonction de la température et de la salinité,
- la concentration en oxygène de l'eau avant aération,
- la concentration en oxygène de l'eau après aération,
- le débit à traiter et la demande en O2 du stock.
Conduite du calcul:
1) Calcul du facteur de correction de performances
Les performances annexées par le constructeur ayant été établies en conditions standard, il faut les corriger pour les adapter aux conditions d'élevage.
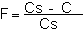
F, facteur de correction
Cs, saturation de l'eau en oxygène dans les conditions de température et salinité (utiliser la table)
C, concentration en O2 de l'eau avant l'aérateur.
2) Apport de l'appareil
CO = COS × F
CO, capacité d'oxygénation en Kg d'O2/H
COS, donnée constructeur
Rendement de l'appareil
R = ASB × F
R = rendement en Kg d'O2 dissous/KWK
ASB = donnée constructeur
3) Exemple
Données: - Bassins contenant 6 T de Turbots à 18° C
- Demande en Oxygène du turbot: 180 g/T/H à cette température (JONES, 1981)
- Débit d'eau: 225 m3/H, oxygène entrée: 2 mg/1
- Concentration d'oxygène désirée: 3 mg/1 en sortie de bassin
- Saturation en oxygène à 18° et 35 0/00 de salinité: 7,66/1 (R.F. WEISS, 1970).
Appareil: aération par bulles et air lift combiné. Les turbots ayant un comportement de fond, ce type d'aérateurs à l'intérêt de mettre l'eau en circulation verticale et en surface.
COS = 1,5 Kg/H
ASB = 0,4 Kg/KWH
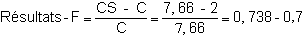
Note: La concentration C avant l'aérateur, dépend de la teneur de l'eau d'entrée du bassin et de la teneur dans le bassin. Il conviendrait de la déterminer exactement si la concentration d'entrée et la concentration en bassin étaient très différentes. Elle est ici assimilée à la concentration d'entrée du bassin.
- Co = COS × F = 1,5 × 0,7 = 1,05Kg O2/H
- R = ASB × F = 0,4 × 0,7 = 0,28 Kg O2/KWH
- Nombre d'appareil (n)
- Oxygène nécessaire au poisson: 6 T × 180 g/H = 1080 g/H
- Rétablissement de la teneur en bassin: 225 × (3 -2 ) = 225 g/H
- Total à fournir DO = 1,305 Kg/H
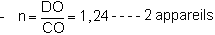
On devra implanter deux appareils fonctionnant périodiquement ou chercher des appareils plus petits:
- Puissance consommée:
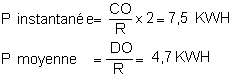
Remarques importantes:
L'application du facteur de correction montre que plus on relève la teneur en oxygène dissous; (pour une fourniture d'oxygène donné en terme de Kg/H) plus la puissance à fournir augmente.
Il en est de même si la concentration à saturation diminue, c'est à dire si la température augmente.
C'est ce qui explique l'inefficacité des aérateurs à haute température et l'utilité dans ce cas d'utiliser l'oxygène pur.
On trouvera en Annexes les éléments caractérisant la matériel d'aération et d'oxygénation.
Annexe 4
L'épuration de l'eau se pratique essentiellement en écloserie.
Les procédés mis en oeuvre sont:
- La décantation,
- la filtration,
- la nitrification sur support,
- l'écumage.
A un niveau expérimental, il existe des procédés utilisant:
- L'échange d'ions (sur réolithes)
- les cultures hydroponiques
- la flottation
- la dénitrfication.
Nous n'en parlerons pas ici.
La décantation:
C'est l'élimination des particules solides par captage et dépôt sur un support. C'est un procédé relativement simple et peu coûteux.
Les déchets issus d'un élevage aquacole seront d'autant plus difficiles à capter qu'ils auront séjourné longtemps dans les bassins et les systèmes d'évacuation de l'eau (FAURE, 1984)
La conception des bassins et de l'hydraulique est donc déterminante.
Le rendement étant généralement faible (40% environ), il faudra admettre une certaine pollution ou disposer d'autres procédés en sortie de décanteur.
On se reportera à l'Annexe 5, pour la description des principaux procédés de décantation.
La filtration biologique
Sous le terme de filtration biologique on désigne des procédés utilisant la propriété de certaines souches de bactéries de transformer certains polluants.
En aquaculture, c'est la transformation de l'ammoniac toxique en nitrates qui est visée. Il y a en même temps développement de matières vivantes (bactéries).
Il s'agit d'éliminer une pollution solubilisée pour la transformer en matières vivantes particulaires.
Les conséquences pour l'élevage sont:
- des difficultés importantes pour traiter les animaux en cas de maladie, la plupart des produits de traitement étant toxiques pour les bactéries épuratrices.
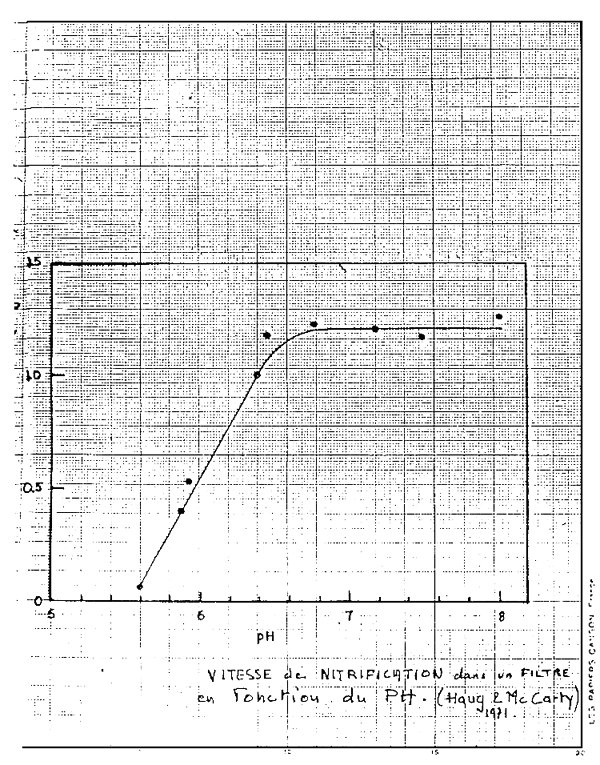
- une maintenance assez lourde, le développement du film bactérien sur le support implique des lavages si l'on veut garder son efficacité et éviter l'apparition de processus anaérobie dangereux pour les poissons. Le pH doit être contrôlé et maintenu au-dessus de 6,8 (chaulage).
Le gain retiré de la mise en place d'un tel système doit donc être conséquent:
- Gain important en énergie (chauffage, refroidissement) grâce au recyclage que permet la filtration.
- gain important des résultats d'élevage (croissance, maîtrise du cycle reproducteur…)
Les coûts liés au système, en dehors de l'investissement proviennent de:
- la circulation forcée de l'eau, nécessitant la plupart du temps un pompage.
- la fourniture d'oxygène : 5 g d'oxygène par gramme d'azote ammoniacal éliminé.
- du lavage, nécessitant la plupart du temps de l'eau et de l'air comprimé sous pression.
LES PROCEDES: (Annexe 6)
- Les boues activées: il n'y a pas de support, les bactéries épuratrices se développent sur les déchets maintenus en suspension par l'aération. Ce procédé est inadapté aux effluents très dilués de l'aquaculture. Il est parfois utilisé en carpiculture ou anguillicuture.
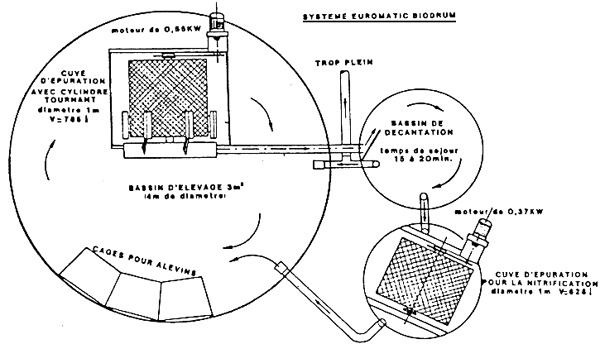
- Les disques biologiques: Ils ne nécessitent pas de lavage. Leur efficacité conduit, soit à des installations volumineuses et coûteuses, soit des qualités d'eau médiocre.
Le principe consiste à immerger périodiquement le support et le film bactérien. L'oxygénation se fait lors de l'émersion.
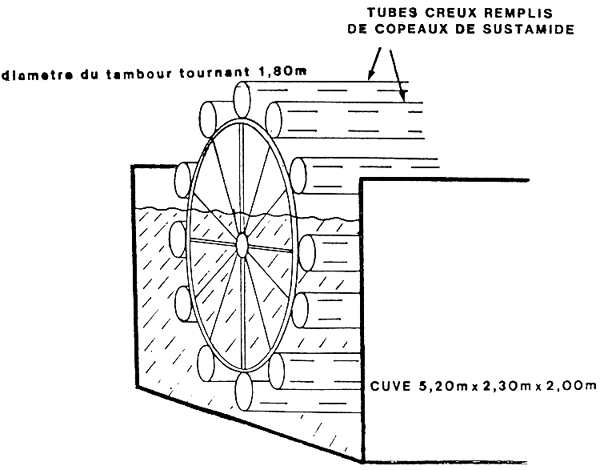
- Les filtres à supports immergés: Il en existe de nombreux types. Les plus efficaces et les plus compacts sont ceux utilisant des matériaux performants mis au point pour la nitrification des eaux de rivière en vue de leur potabilisation. Ils offrent l'avantage important d'une filtration mécanique.
En dehors de performances annoncées (Kg N-ammoniacal éliminé par 24h. et par m3 de matériau) on s'efforcera de déterminer:
- les qualités d'eau exigées à l'entrée: le prétraitement peut être plus coûteux que le filtre lui-même.
- les pressions nécessaires en fin de cycle (avant lavage)
- la qualité des répartitions d'eau à l'entrée et en sortie: une mauvaise répartition de l'eau rend le filtre inefficace (court circuit hydraulique de la masse filtrante)
- la complexité et l'efficacité du système.
On s'assurera:
- que l'oxygène en sortie d'élevage est suffisant pour l'oxydation de l'ammoniac (5 g O2/g N - NH4), sinon il faudra recirculer l'eau sur le filtre ou aérer dans le filtre.
- que l'eau est débarassée avant le filtre des MES et de la MO, sinon la nitrification n'aura pas lieu.
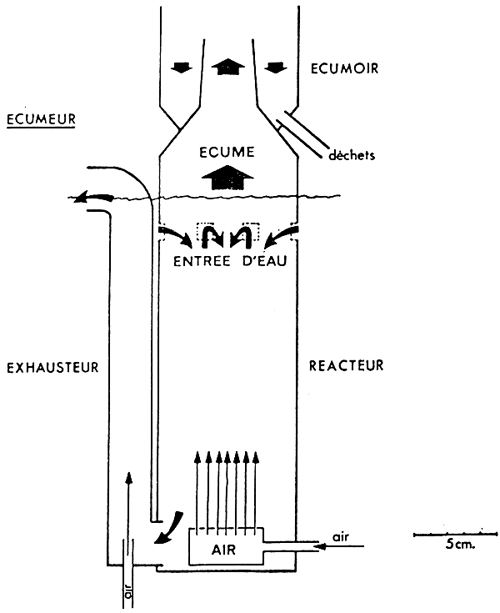
L'ECUMAGE: (voir Annexe 6)
Cette technique consiste à provoquer l'apparition d'une mousse, qui est riche en composés azotés et qui peut contenir une quantité notable de particules.
Cette mousse se forme spontanément en eau de mer au niveau des aérateurs.
La mise en oeuvre consiste donc à établir un bullage à l'intérieur d'une cheminée. La mousse est évacuée en haut de la cheminée.
Des appareils qu commerce existent, l'installation comporte comme unique réglage la hauteur de la cheminée au dessus du plan d'eau:
- trop haute, les mousse ont du mal à s'évacuer et l'épuration n'a pas lieu,
- trop basse, les mousses très hydratées du bas de la colonne sont évacuées et la perte d'eau devient excessive.
L'application de ce procédé à l'aquaculture a été étudiè par DIVANACH, (1978).
L'utilisation d'appareil de stérilisation des eaux est réservée aux écloseries.
La stérilisation de l'eau d'apport par le chlore est également pratiquée en écloserie; la neutralisation est faite par le sulfite avant utilisation.
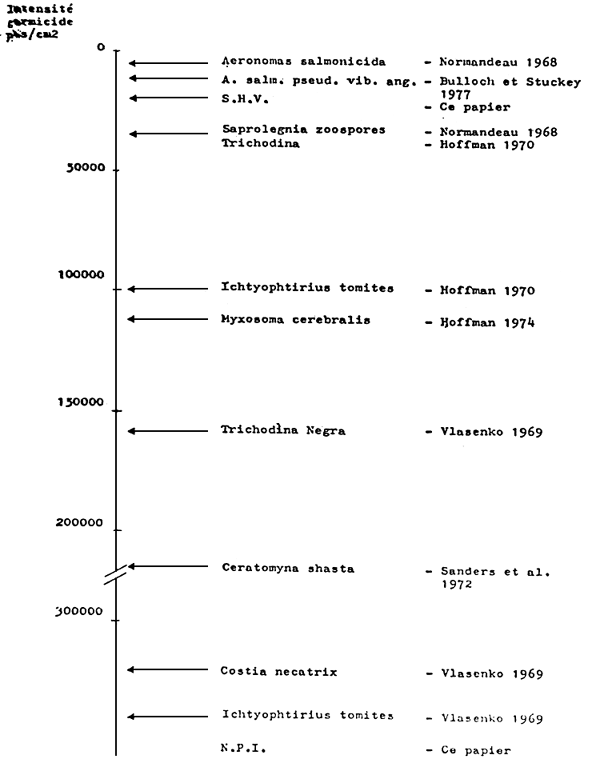
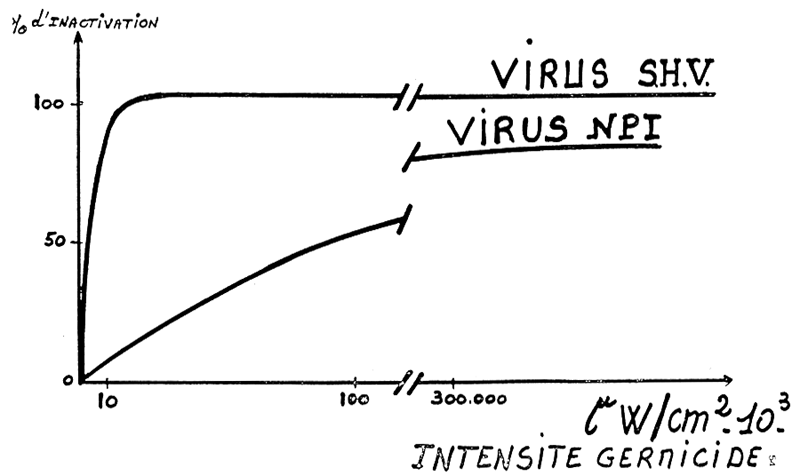
La mise en oeuvre de la stérilisation suppose la connaissance des germes que l'on veut détruire. En effet, l'intensité germicide à appliquer diffère suivant les germes: un virus tel que la S.H.V. en salmoniculture est détruit par de faibles densités germicides, tandis que le virus de l'I.P.N. demandera des intensités considérables, qui en pratique ne pourront jamais être atteintes, (MAISSE et coll., 1980) (fig. 14)
HOFFMAN (1974) de ROSENTHAL (1981) ont fait la synthèse des données disponibles pour l'aquaculture.
La stérilisation par les U. V. est aisée à mettre en oeuvre, mais reste réservée aux petits débits. Compte-tenu des coûts d'investissement et fonctionnement (changement des lampes).
L'ozone utilisé pour les coquillages, reste d'application limitée vu la sensibilité des poissons aux résidus d'ozone (0,01 à 0,06 mg/1).
Le chlore est utilisé sur l'eau d'apport. Une neutralisation au sulfite gazeux, facile à réaliser, évite les problèmes de toxicité.
La réutilisation de l'eau permet d'accroître les stocks en place, et de pratiquer en écloserie et en élevage de juvéniles, le chauffage de l'eau dans des conditions économiquement acceptables.
L'aération et le traitement des eaux recyclées est généralement nécessaire.
Pour déterminer le rendement des procédés du'il faut mettre en place, on se fixe un objectif de concentration en bassin, le rendement nécessaire est obtenu par la formule suivante:
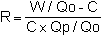
avec W, quantité de polluant déversé en gr/j (moyenne sur 24 h.)
Qo, débit d'apport en m3/j
C, objectif de concentration du polluant en bassin
Qp, débit recirculé
Par ce calcul, l'éleveur peut apprécier le matériel qui lui est proposé, par rapport à ses besoins.
4. CONCLUSIONS
La Maîtrise de l'eau en aquaculture suppose que l'on ait procédé à l'évaluation des flux d'oxygène et de polluants, que l'eau va avoir en charge d'amener et d'évacuer de l'élevage.
Un certain nombre de matériels peuvent permettre d'apporter des solutions en cas d'insuffisance du milieu naturel.
La connaissance des capacités et des rendements du matériel permet d'établir un projet d'aménagement.
Au cours de l'élevage, les données économiques (coût de l'énergie), commerciales (date de vente des produits), les méthodes de nourrissage, interfèreront avec la maîtrise de l'eau pour concourir aux décisions. La gestion de l'ensemble amène à prendre de nombreuses données, qui l'apparition de l'informatique peut aider à traiter.
BIBLIOGRAPHIE
ALAVOINE F., 1981: Analyse énergétique et salmoniculure intensive. Mémoire d'études. CEMAGREF - Groupement de Bordeaux
DIVANACH P., 1978: Conditions d'application et valeur épuratrice de la flottation et de l'écumage en aquaculture intensive marine. Thèse de Docteur de 3ème cycle de l'Université d'Aix - Marseille II 132 p.
FAURE A., 1983: Intérêt et pratique de l'alimentation libre service en salmoniculture intensive. La Pisciculture Française № 74, p. 15–26
FAURE A., 1983: L'épuration en salmoniculture, Problèmes et perspectives. La Pisciculture Française № 73 : p. 18–22
FAURE A., 1983: Salmoniculture et Environnement. Evaluation de la pollution rejetée par les salmoniculture intensives. Vol. 1 - Etude № 16 - CEMAGREF
FAURE A., 1984: Moyen de lutte contre la pollution des salmonicultures intensives. Vol. 2 - Tome 1 - Etude № 19 - CEMAGREF.
HAYWOOD G.P., 1983: Ammonia toxicity in teleost fishes. A review. Can. Techn. Rep. Fish. Aquat. Sci. 1177, 35 p.
HOFFMAN G.L., 1974: Disinfection of contamined water by U.V. irradations, with emphasis on whirling diseases (Myxosoma cerebralis) and its effects on fish. Trans. Am. Fish. Soc. Vol. 103 № 3 : 541–550.
JONES A., BROWN J.A.G., DOUGLAS M.T., THOMPSON S.J. and WHITEFIELD R.J., : Progress towards developing methods for the intensive farming of turbot (Scophtalmus maximus 1.) in cooling water from a Nuclear power station. EIFAC/80/Symp : E/13.
KAUSHIK S.J., 1980: Influence of a rise in temperature on the nitrogen excretion of rainbow trout (Salmo gairdneir R) Proc. World Symp. on Aquaculture in Heated Effluents and Recirculation Systems p. 77 à 90.
KRAMER, CHIM AND MAYO, 1972: A study for development of fish hatchery water treatment systems. Prepared for Walla Walla District Corps of Engineers.
LIAO P.B., 1971: Water requirements of salmonids. Prog. fish. Cult. 33 : 210–215.
MAISSE G., DORSON M. et TORCHY C., 1980: Inactivation de deux virus pathogènes pour les salmonidés (virus de la nécrose pancréatique infectieuse et de la septicémie hémorragique virale) par les rayons ultra-violets. Bull. Franç. Pisc. № 278, 3ème trim. pp. 39–40.
ROSENTHAL H., 1980: Ozonation and sterilization. Proc. World Symposium in Heated Effluents and Recirculation Systems. Stavanger 28–30 May 1980. vol. 1 p. 219–277.
SPARRE A., 1976: Markovian decision process applied to optimization planning in fish farming. Meddr. Danm. Fisk og Havunders N.S. 7 : 111–197.
WEISS R.F., 1970: Deep Sea Research, 17 : 721–735.
- TABLEAU -
Seuil admis comme maximum en exposition de longue durée et n'ayant pas d'effet sur la croissance et l'indice de transformation:
| ESPECES | SEUIL D'AMMONIAC EN POIDS D'AZOTE N - NH3 (mg/1) | AUTEURS (dans J.F. Wickins 1980). | ||
| Oncorhynchus tshawytsha | 0,06 | Robinson - Wilson et Seim 1975 | ||
| Salmo gairdneri | 0,4 – 0,14 après acclimatation | Schultre Wiehenbrauck 1976 | ||
| Poisson chat | 0,01 – 0,06 | Robinette 1976 | ||
| Sole | 0,06 | Alderson 1979 | ||
| Turbot | 0,11 | Alderson 1979 | ||
| Chevrette | 0,09 | Wickens 1976 | ||
| (Macrobrachium rosenbergii) | 0,07 – 0,18 | AQUACOP 1977 | ||
| Homard (Larve 4ème stade) (Homarus americanus) | 0,14 | Deslestraty et al 1977 | ||
| Huître (Crassostrea virginia) | 0,06 | Hartman et al 1973 | ||
- TABLEAU -
Seuil admis comme maximum en exposition de longue durée et n'ayant pas d'effet sur la croissance et l'indice de transformation:
| ESPECES | SEUIL D'AMMONIAC EN POIDS D'AZOTE N - NH3 (mg/1) | AUTEURS (dans J.F. Wickins 1980). | ||
| Oncorhynchus tshawytsha | 0,06 | Robinson - Wilson et Seim 1975 | ||
| Salmo gairdneri | 0,4 – 0,14 après acclimatation | Schultre Wiehenbrauck 1976 | ||
| Catfish | 0,01 – 0,06 | Robinette 1976 | ||
| Sole | 0,06 | Alderson 1979 | ||
| Turbot | 0,11 | Alderson 1979 | ||
| Chevrette | 0,09 | Wickens 1976 | ||
| (Macrobrachium rosenbergii) | 0,07 – 0,18 | AQUACOP 1977 | ||
| Homard (larve 4è stade) (Homarus americanus) | 0,14 | Delslestraty et al 1977 | ||
| Huitre (Crassostrea virginia) | 0,06 | Hartman et al 1973 | ||
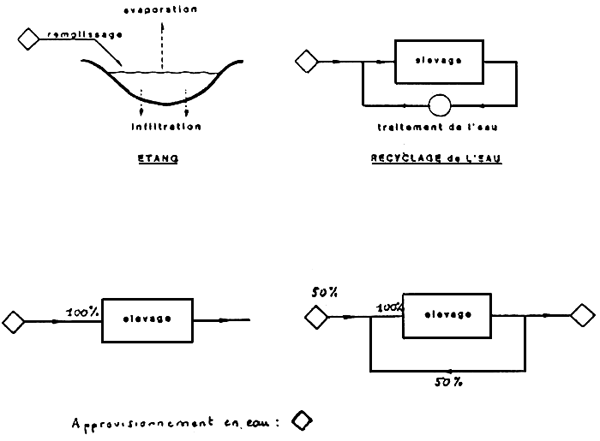
Fig. 1. - Approvisionnement en eau: l'étang et la recirculation de l'eau à 100% sont les deux cas de systèmes en équilibre ne demandant qu'un appoint d'eau. Le premier cas fait appel à des équilibres naturels, le second dépend des procédés d'oxygénation et d'épuration mis en place. En élevage intensif sans recirculation, le débit demandé à l'approvisionnement sera maximum.
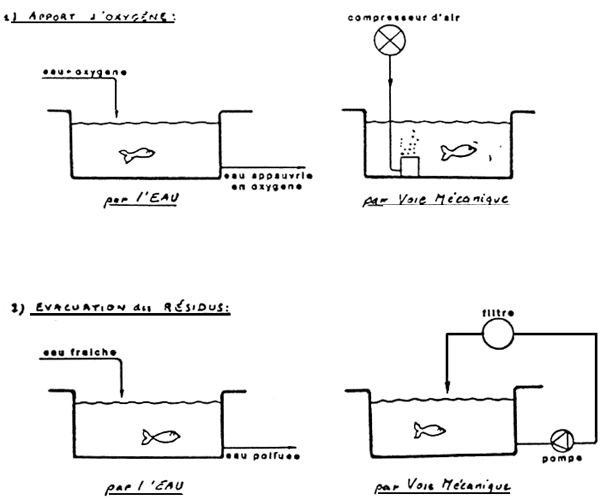
Fig. 2 - Les fonctions de l'eau et leur équivalent mécanique.
Fig. 3 - Consommation d'oxygène après alimentation
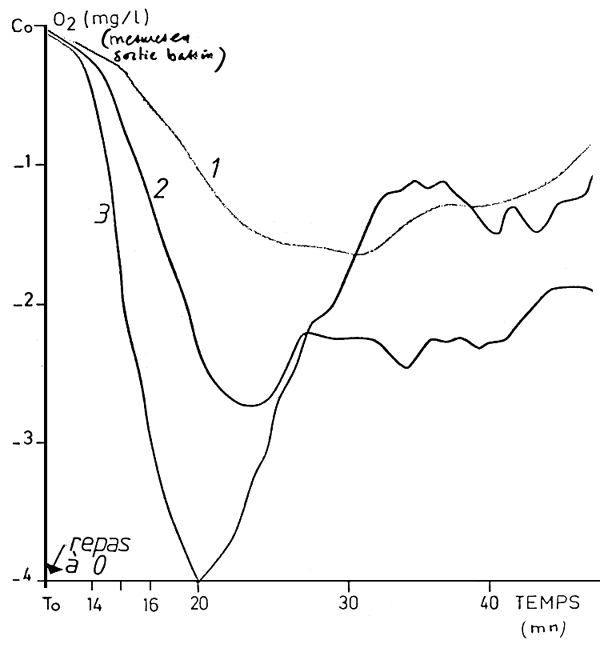
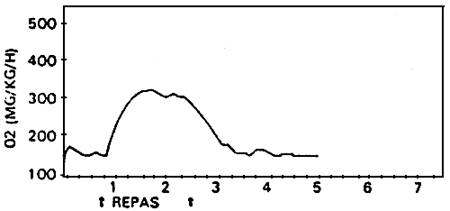
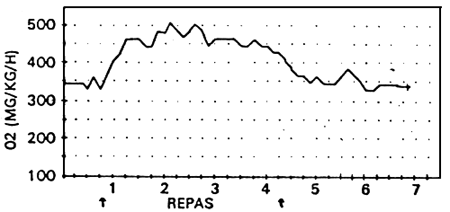
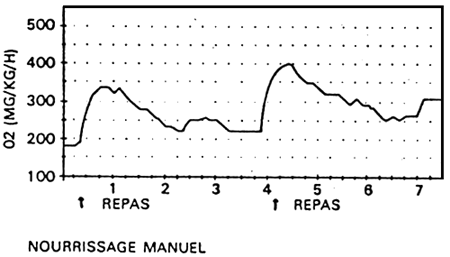
Fig. 4 Allure générale des courbes de consommation d'oxygène (mg/kg/h) pour les différents modes de nourrissage.
(d'après FAURÉ)
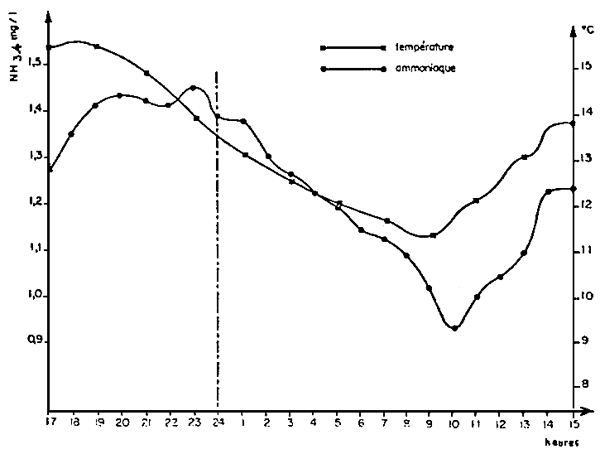
Fig. 5 - Fluctuations de la concentration d'ammoniac en Bassins
(Pisciculture de la Rochotte)
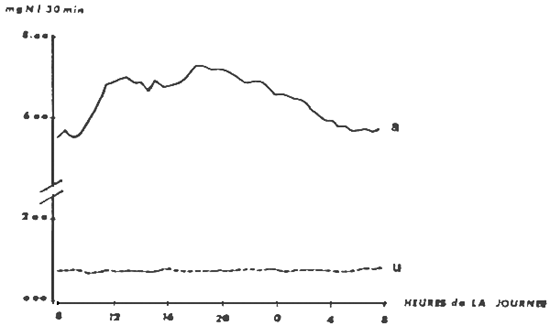
Fig. 6 Fluctuations de l'excretion azotee chez la truite à 10°C d'après KAUSHIK
u=urée a=ammoniac en mg/kg P.V/30'
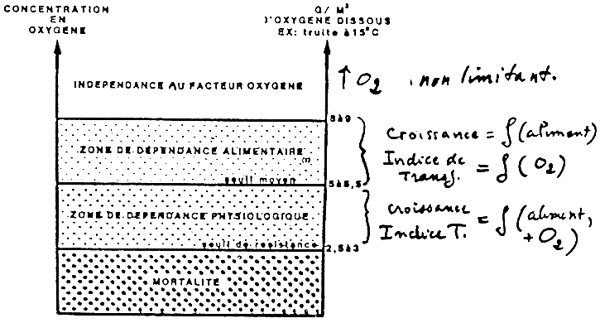
Fig. 7 CRITERES DE CHOIX DES TAUX D'OXYGENE ENBASSIN
Fig. 8
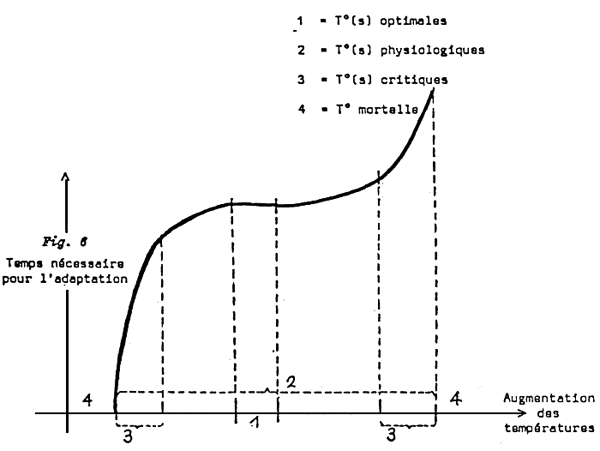
La rapport Temps/Variation de températures doit être d'autant plus grand que l'on s'éloigne de la phase 1.
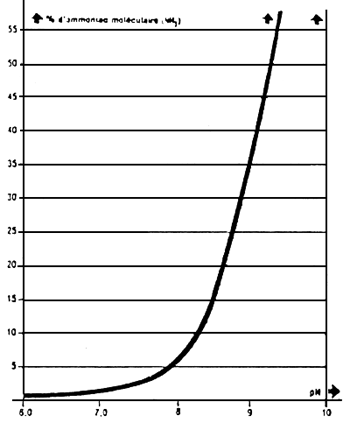
Fig. 9 Pourcentage d'ammoniac moléculaire (NH3) en fonction du pH à température constante (20 °C)
Ce pourcentage est également fonction de la température. Aussi le risque d'intoxication est-il particullérement grave à pH basique (au-dessus de 7, 5) et à température élevés (d'oprés TERVER)
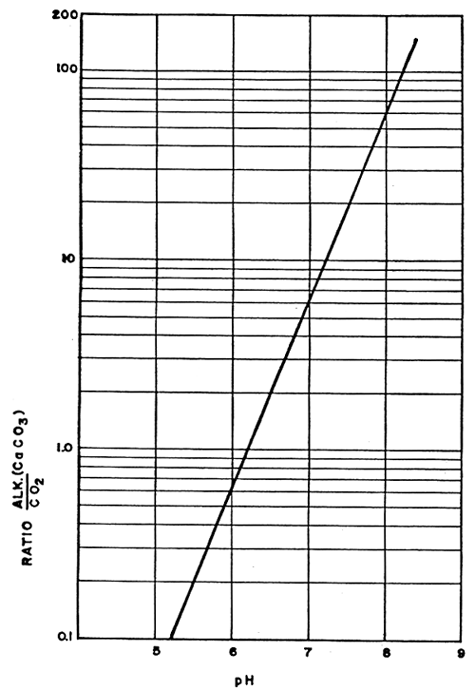
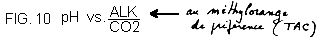
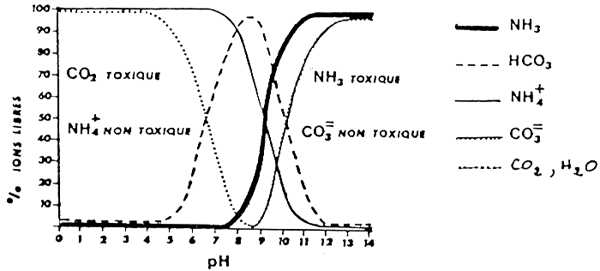
Fig. 11 - Zone de toxicité respective du CO2, et de NH3 en fonction du pH
Fig. 12 - CAUSES DE MODIFICATIONS DU pH A L'INTERIEUR DE L'ELEVAGE
- effet sur le pH du dimarrage de l'aération en bassins chargés-
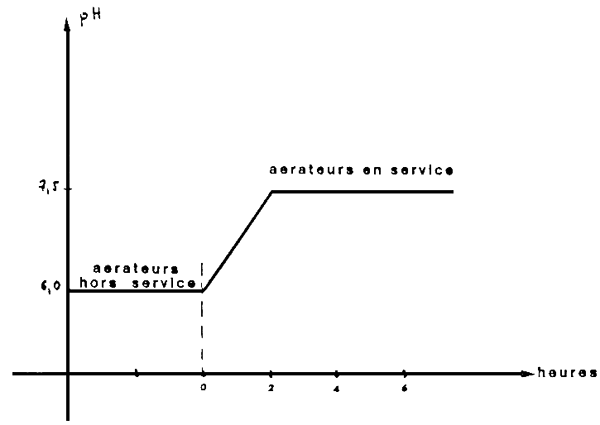
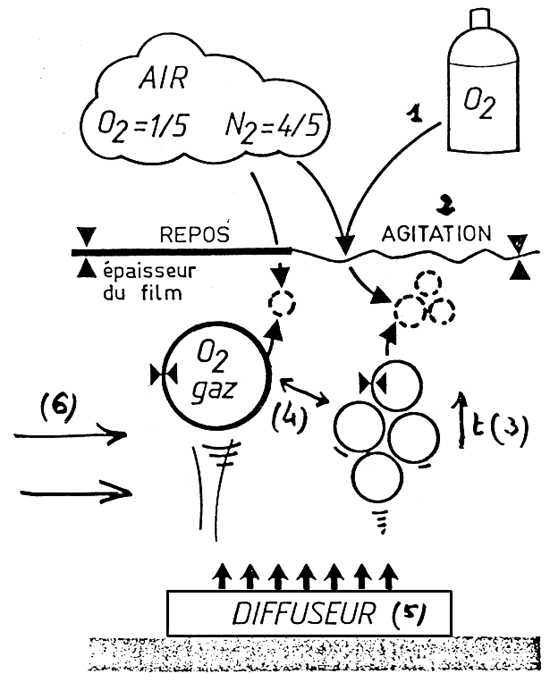
Fig 13. des micanismes de la dissolution de l'oxygéne
Fig 14. Pourcentage d'inactivation de la SHV et de la NPI en fonction de l'intensité germicide utilisée en ecur laire.
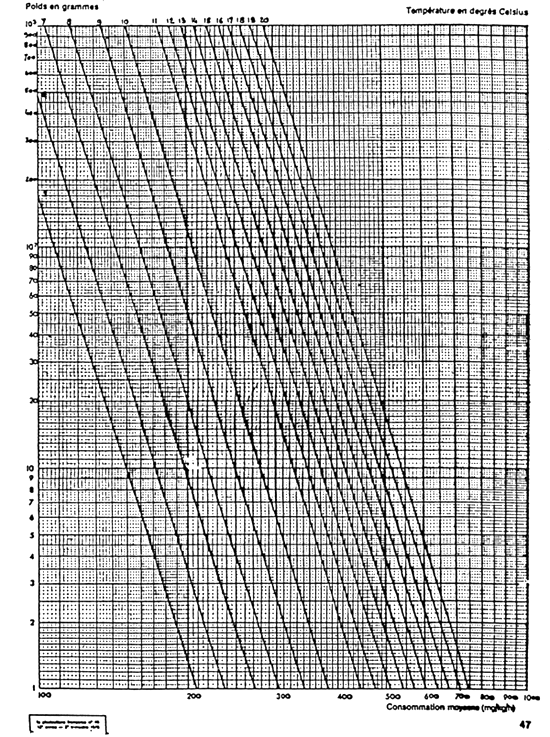
ANNEXE № 1 (№ 1)
CONSOMMATION D'OXYGÈNE DE LA TRUITE ARC-EN-CIEL
en mg/kg/h de 5 à 20° et de 1 à 1 000 g (d'après LIAO, 1970)

ANNEXE 1 (3)
PRISE D'EAU CRAVITAIRE
ANNEXE 2 (1)
PRISE D'EAU ET POMPAGE
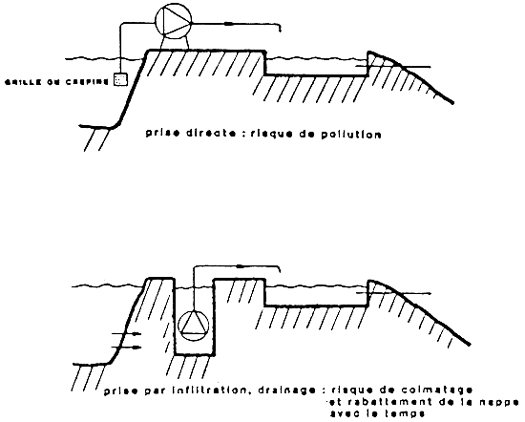
- Prise d'eau et dénivelé : dispositions type.
ANNEXE 2 -(2)
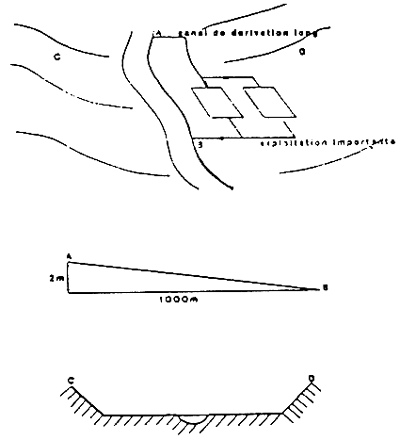
RIVERE A PENTE FAIBLE ET VALLEE LARGE ↑
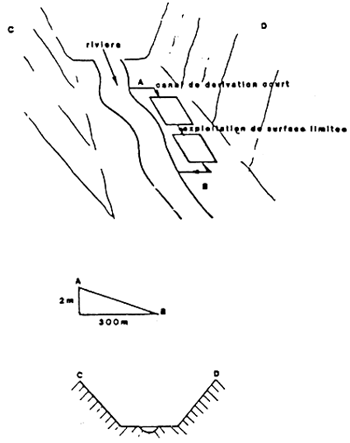
RIVIERE A PENTE FORTE ET VALLEE ETROITE↑
- Prise d'eau - Incidence des profils de la rivière.
ANNEXE 2-(3)
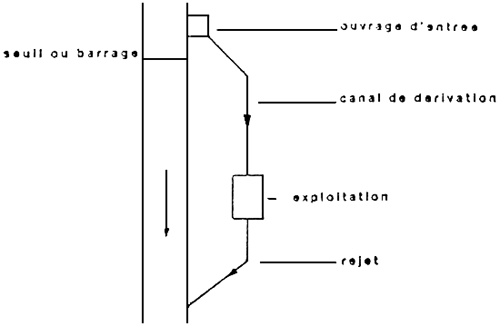
ALIMENTATION EN DERIVATION
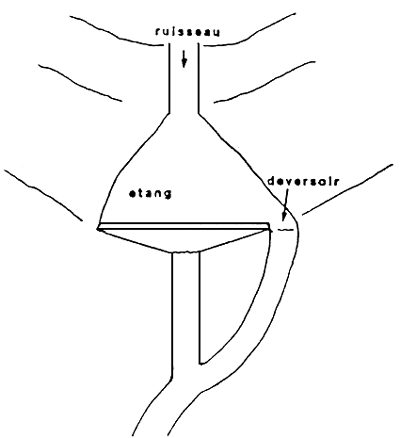
ETANG DE BARRAGE
- Prise d'eau directe, prise d'eau en dérivation.
ANNEXE 2 (4)

(1) RIVIÈRE AVEC PEU DE MATERIAUS CHARRIES.
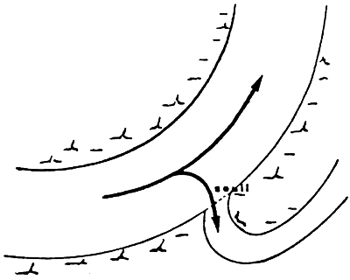
(2) RIVIERE A CHARRIAGE IMPORTENT
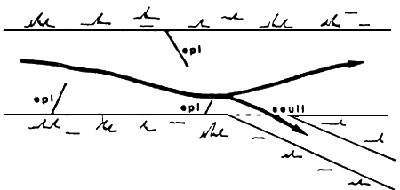
(3) PRISE D'EAU SUR UN ALIGNENT DROIT:
POSITIONNEMENT DES EPIS.
- PRISE D'EAU SUR RIVERE EN COURBE ET EN ALIGNEMENT
ANNEXE 2 (5)
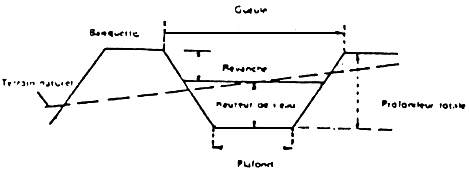
Coupe transversale d'un canal d'alimentation.
| Installations familiales quelques l/s | Installations importantes 20 à 50 l/s | |
| Largeur du plafond | 0,25 à 0,30 m | 0,50 m |
| Profondeur | 0,25 à 0,40 m | 0,60 à 0,80 m |
| Inclinaison des parois | 1,5/1 | 1,5/1 |
| Largeur de la gueule | 0,60 à 1,00 m | 1,50 à 1,80 m |
| Pente du fond | 0 | 1%. (1 cm 10 m) |
- Dimensions d'un canal d'amenée en terre (étangs).
(d'aprés BARD. I et coll. - CTFT)
ANNEXE 2 (6)
Données technique de base pour le dessablage (DECEMNT, 1978).
Le domaine usuel d'application du dessablage porte sur les particules de granulométrie supérieure à 200 microns. L'étude théorique du dessablage se rattache à celle des phénomènes de sédimentation en chute libre faisant appel à la formule de STOKES en régime laminaire qui est le plus fréquement rencontré dans les canaux de pisciculture. En pratique cependant on se base sur les donnéee suivantes (sédimentation libre, densité des particules de sable = 2, 65).
| d (cm) | 0,005 | 0,010 | 0,020 | 0,030 | 0,040 | 0,050 | 0,100 | 0,20 | 0,30 | 0,50 | 1,00 |
| Vs (cm/s) | 0,2 | 0,7 | 2,3 | 4,.0 | 5,6 | 7,2 | 15 | 27 | 35 | 47 | 74 |
| Vc (cm/s) | 0 | 0 | 1,6 | 3,0 | 4,5 | 6,0 | 13 | 25 | 33 | 45 | 65 |
| Ve (cm/s) | 15 | 20 | 27 | 32 | 38 | 42 | 60 | 83 | 100 | 130 | 190 |
| Vc' (cm/s) | 0 | 0,5 | 1,7 | 3,0 | 4,0 | 5,0 | 11 | 21 | 26 | 33 |
avec: d - diamètre de la particule de sable
Vs - vitesse de sédimentation pour fluide à vitesse horizontale nulle
Vc - vitesse der sédimentation pour fluide à vitesse horizontale de 0,30m/s
Ve - vitesse horizontale critique d'entrainement de la particule déposée
Vc' - vitesse de sédimentation pour fluide à vitesse horizontal égale à ve.
Dimensionnement du dessableur: pour des raisons de simplicité, le dessableur sera généralement rectangulaire, du type couloir. La section transversale se calcule selon (Q = Vs) ou V sera inférieure à la vitesse critique d'entrainement (Ve) de la plus petite particule à retenir. La surface horizontale se calcule en fonction de la vitesse de sédimentation Vs des particules de plus petite dimension à retenir et du débit maximum à véhiculer:
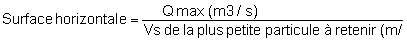
Dans la pratique, il sera moins onéreux de prévour un canal d'alimentation de la pisciculture en dérivation avec le bac de dessablage pour permettre un nettoyage manuel ou mécanique de celui-ci. Si le débit absorbable par le canal d'amenée est très important par rapport a débit en fonctionnement, des chasses hydrauliques et une disposition judicieuse permettent de nettoyer le dessableur.
ANNEXE 2 (7)
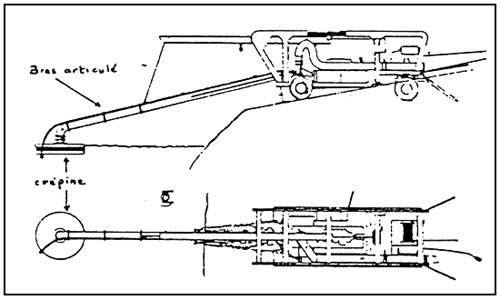
Schéme d'une prise d'eau mobile a nive ou d'aspiration variable
(Procédé Hydromobile)
ANNEXE 2 (8)
POMPE A HELIGE
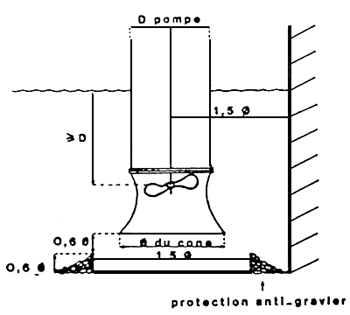
POMPE CENTRIFUCE
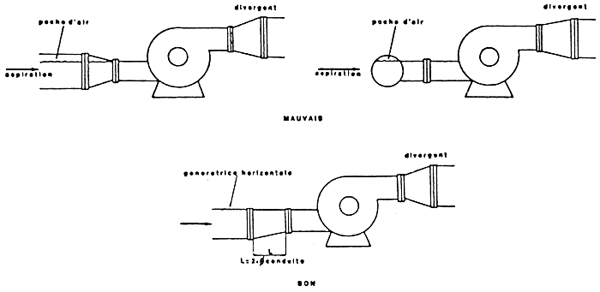
INSTALLATION DES POMPES
PRECAUTIONS A L'ASPIRATION
(d'apres SOGREAN)
ANNEXE 2(9)

CARACTERISTIQUES D'UNE POMPE A EMULSION (AIR LIFT)
ANNEXE 3
- Quelques données utiles:
- La valeur maximum de dissolution de l'oxygène par l'eau (saturation) à la pression atmosphérique en présence d'air est dorinée par les différentes tables. On peut en calculer une valeur approchée, à partir de la température de l'eau, avec la formule (eau douce)
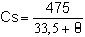 (GAMESON et ROBERTSON)
(GAMESON et ROBERTSON)
Cs, valeur de saturation en gr/m3 (ou ppm)
e, température en degré Celsius
| - Solubilité | de l'oxygène à 15°C | : 47 gr/m3 |
| de l'azote à 15° C | : 20,6 gr/m3 | |
| du gaz carbonique à 15° C | : 1953, 0 gr/m3 |
Formule de transfert des gaz de l'état gazeux à l'état dissous et inversement
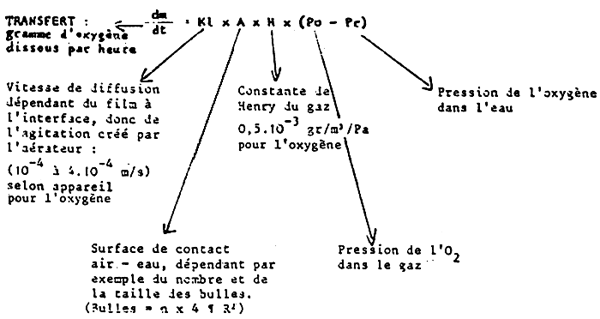
Remarque: Concentration de l'oxygène = H × Pr
ANNEXE 4 (1)
CASCADE: EXEMPLE d'UTILISATION
des TAUX de TRANSFERT
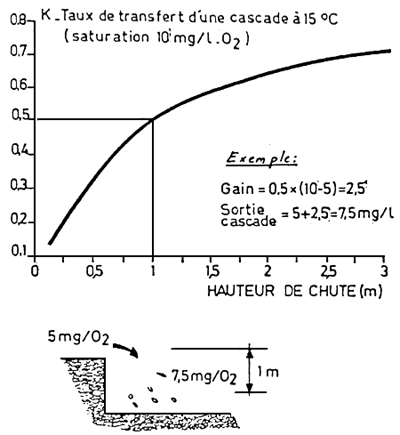
ANNEXE 4 (2)
APORT EN OXYGENE DISSOUS
CASCADE ALIMENTEE PAR POMPE
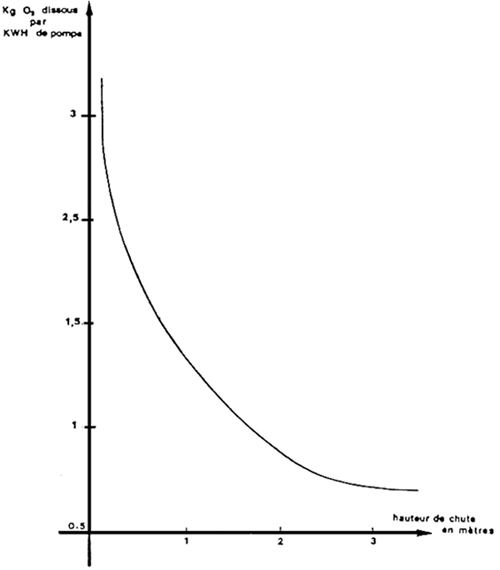
ANNEXE 4 (3)
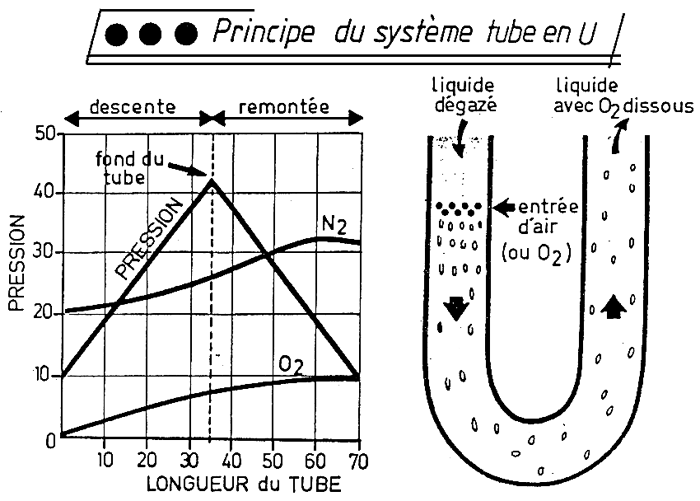
ANNEXE 4(4)
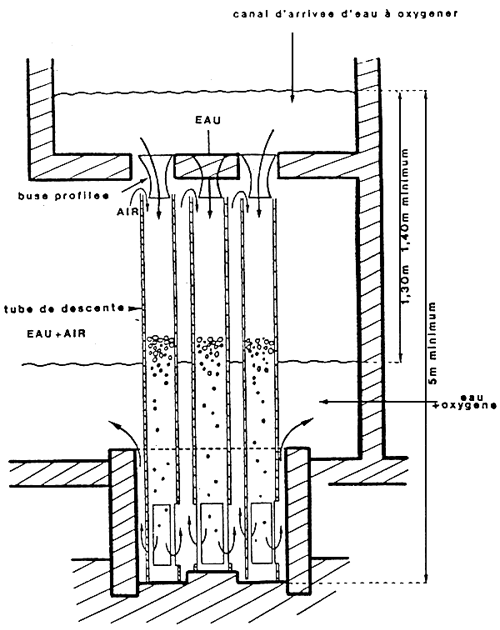
-Schéma de Tube en U gravitaire.
ANNEXE 4(5)
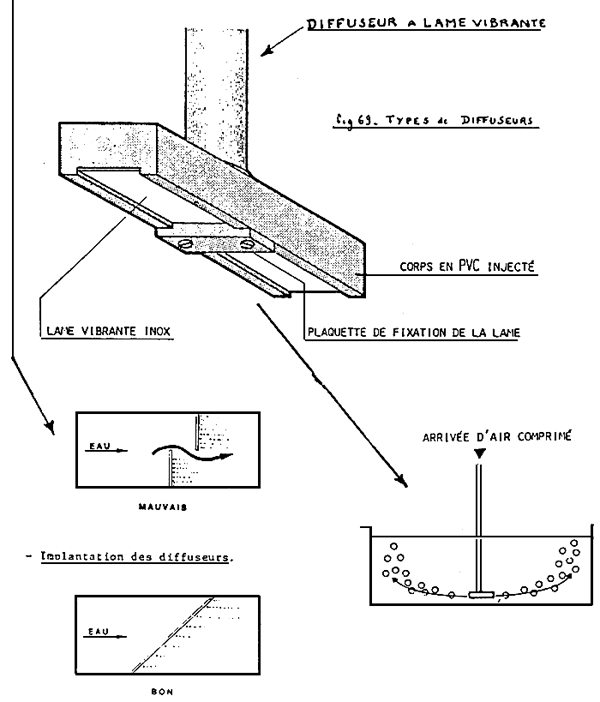
ANNEXE 4 (6)
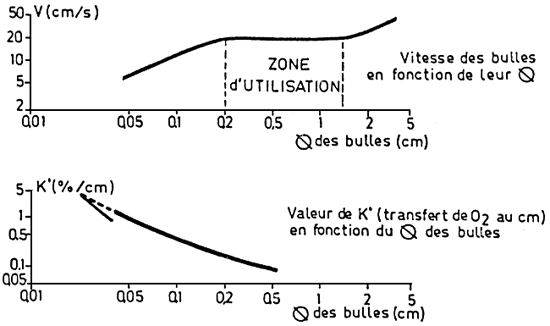
N - Calcul d'un diffuseur : détermination graphique.
ANNEXE 4 (7)
MIXAERATOR
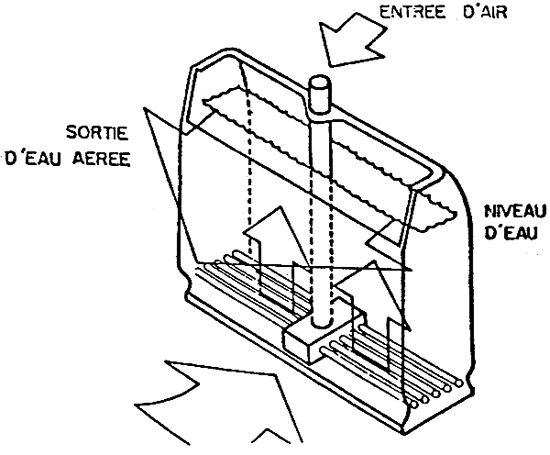
ANNEXE 4 (8)
Fig 56 INSTALLATION D'UNE TURSINE
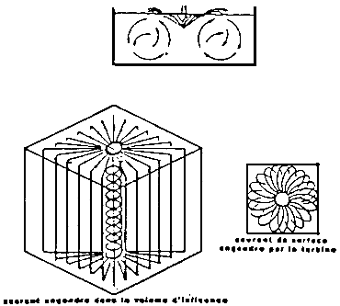
PUISSANCE A INSTALLER ET NOMBRE DE TURSINES
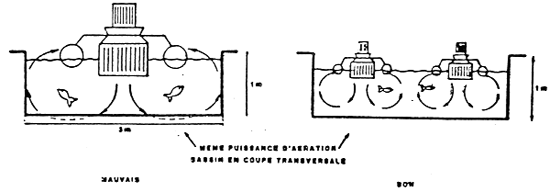
ANNEXE 4 (9)
- Aérateurs - tableau comparatif (placiculture) :
| Cascades | Brosses | Jats | Tube en U | Turbines lentes | Turbines rapides | Diffuseurs | Hydroéjecteur | |||
| odalités d'installations | ||||||||||
| sur Pompes | + | 0 | + | + | 0 | 0 | 0 | + | ||
| avec Soufflantes | 0 | 0 | 0 | + | 0 | 0 | + | 0 | ||
| Mise directe en bassin | 0 | ± | ± | 0 | + | ± | + | + | ||
| Mobilité | 0 | 0 | ± | 0 | ± | + | ++ | +++ | ||
| Performance en conditions coyennes. | 1–1,5 | 1,5 | 1,5–2,0 | 2–3 | 1,5–2,0 | 1,0 | 0,5–1,0 | 0,5–1,0 | ||
| Rapport en O2 standart au | ||||||||||
| Investissement toût moyen | variable mais faible | 3500 F | 2000 F | 12000 F (pompes comprises) | 8500 F | 4500 F | 6000 F (turbines incluses) | 3000 F | ||
| Efficacité en condition de Pisciculture | - | + | + | +++ | +++ | ++ | ++ | ++ | ||
| Maintenance (coût) | aucune | faible | faible | Entretien des pompès | Motoréducteur | Nettoyage des grilles Protection | Eemplacement ou netporeux | Entretie pompes | ||
| Réglage de puissance en Continu | impossible | possible si prévu | impossible | impossible | impossible | impossible | impossible | impossible | ||
| Facilités d'utilisation l'oxygène pur sans modifications importantes. | 0 | 0 | 0 | + | 0 | 0 | + mais coûteux | + | ||
| par principe | ++ | ++ | par principe | 0 | 0 | + avec aménagement | ++ | |||
ANNEXE 4 (10)
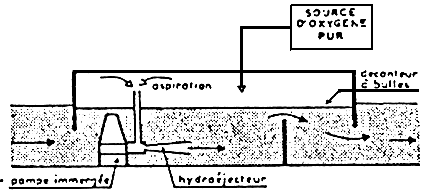
Utilisation d'un hydroéjecteur / + OXYGENE PUR
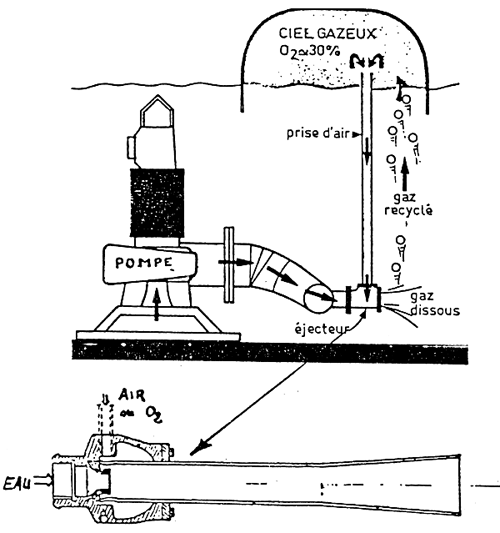
- Principe de l'hydroéjecteur.
ANNEXE 4 (11)
PROBLEME DE L'AZOTE EN OXYGENATION
ANNEXE 4 - (12)
| Aératior classique (turbines avec apport spécifique de 0.8 kg O2/kWh) | Température 20°C teneur de saturation de l'eau en oxygène: 8.88 mg/1 | Installation l'oxygéne pur (hydroéjecleurs sous enceinte étanche) | |||||
| 250 l/s | 250 l/s | Débit traité | 250 l/s | 250 l/s | |||
| 7.5 mg/l | 7.5 mg/l | Puissance électrique du dispositif de dissolution | 7.5 kW | 7.5 kW | |||
| 5 mg/l | 7.5 mg/l | Concentration d'oxygène à l'entré du dispositif | 5 mg/l | 7.5 mg/l | |||
| 5.82 mg/l | 8.15 mg/l | Concentration d'oxygène en sortie de dispositif | 11,6 mg/l | 11.6 mg/l | |||
| 1.23 m3/h | 0.44 mt/h | Volume horaire d'oxygène dissous par le dispositif | 4,48 m3/h | 2.77 m3/h | |||
| 4.7t | 1.7 | mini | Tonnes stock ées gràce au dispositif | mini | 17t | 10.5t | |
| 7.1t | 2.5t | moyen | moyen | 26t | 16t | ||
| 9.4t | 3.3t | maxi | maxi | 34t | 21t | ||
| 0 | 0 | oxygène pur consommé par le dispositif | 6 m3/h | 3.8 m3/h | |||
| 1,52 F | 4,28 F | Cout du m2d oxygène dissous | avec oxygène fourni par bouteilles | 13.74 F à 15.25 F | 14.28 f à 15.79 F | ||
| (kW) ← | (kW + gaz) → | avec oxygène fourni par évaporateur | 4.41 F à 12.22 F | 4.84 F à 13.00 F | |||
| avec oxygène fourni | 1.80 F | 2.32 F | |||||
| 190 F | 540 F | Cout mensuel par tonne stockée gràce au dispositif (tonnage moyen) | avec oxygène fourni par bouteilles | 1 697 F à 1 883 F | 1 777 F à 1 989 F | ||
| avec oxygènes fourni par évaporateur | 544 F à 1 510 F | 603 F à 1 821 F | |||||
| (kW) ← | (kW + gaz) → | avec oxygène fourni par générateur | 222 F | 289 F | |||
Evaluation du coût d'utilisation de l'oxygène pur fourni par générateur ou par évaporateur, comparé à l'utilisation d'aérateurs classiques (conditions économiques du tableau: 1982).
ANNEXE 4 (13)
| 1 - JETS | 4- TURBINE |
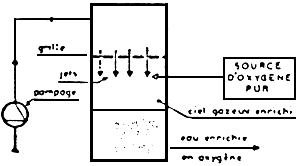 | 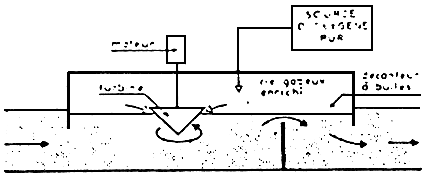 |
| 2 - BICONE | 5 - HYDROEJECTEUR |
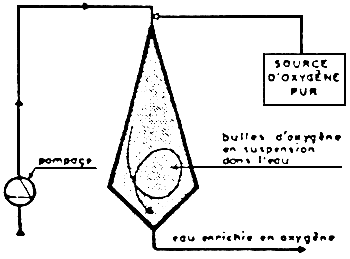 |  |
| 3 - HYDROEJECTEUR | 6 - TUDE EN U |
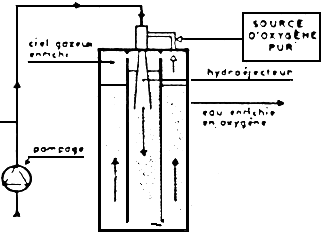 | 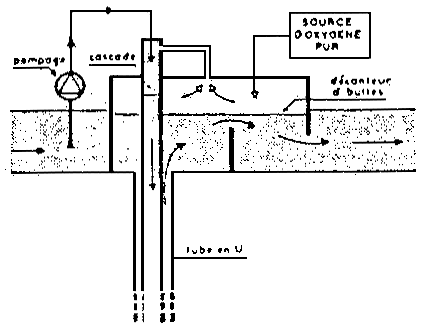 |
| - Principe de la mise en oeuvre de l'oxygène pur. | |
| Ces trois premiers types de dispositifs à l'oxygène pur représentés sur ces schémas correspondent à des installations sur pompage, destinées en principe à des déblts modesles (salles d'incubation alevinage. vlviers). | Ces trois autres types d'installations à l'oxygène pur permettent de traiter des débits importants. Ils comportent tous un calsson formant cloche étanche, par exemple en couverture de canal d'amenée. Celle enceinte termée permet de récupérer l'oxygène qul n's pas été dissous à son premier passage, et de le recycler dans le dispositif de dissolution. |
 | ANNEXE 4 (14) |
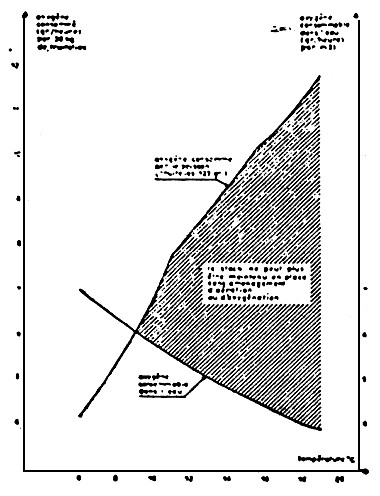
| Fig 75 A Lorsque la teméprature de l'eau augmente, non seulement le poissons |
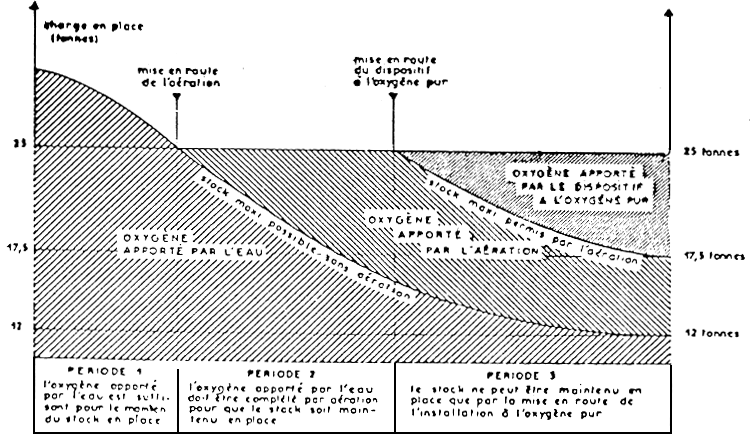
Gestion de l'oxygène dans une pisciculture oû le débit diminue fortement à la saison chaude, et où l'objectif est de maintenir 25 tonnes de truites nourries normalement en stock. En période de fort débit, l'oxygène contenu naturellement dans l'eau sufill à la consommation des 25 tonnes de poisson (période 1). En période 2, le débit a chuté, et Il devient nécessaire de mettre des aérateurs en route. Le débit continuant à diminuer, les aérateurs se trouvent bleniôt à la limite de leurs performances, et ll faut compléler l'apport d'oxygène par un dispositif à l'oxygène pur (période 3). Ce graphique couvre une période de six mois. On a supposé dans cet exemple que la température de l'eau restalt constante foute l'année. L'importance de l'aération et de l'oxygénation serait encore accurue al l'on faisalt intervenir une augmentation de la température.
ANNEXE 5 - (1)
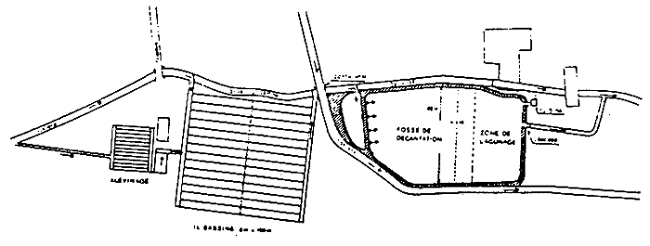
Ce plan montre implantation générale de la pisciculture de Font-Rome et de son ouvrage d'èpuration. Les structures d'é;elvage et le bassin de dècantatión lagunage occupent une place sensiblement èquivalente. (d'après A. Boistel).
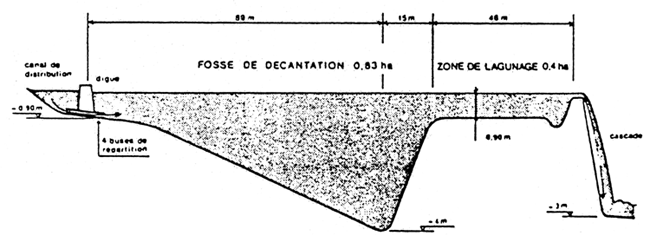
Coupe sur l'ouvrage d'èpuration. Les essais faits sur la zône de lagunage (plantations) ont montrè qu'il faudrait prèvoir des surfaces beaucoup plus importantes pour espèrer traiter l'ammoniaque par cette méthode. La fosse de décantation donne par contre entièrement satisfaction (d'après A. Boistel)
-ETANG de DECANTATION
ANNEXE 5 (2)
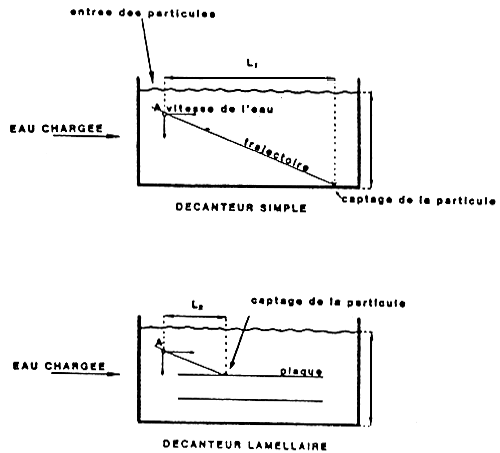
- PRINCIPE DU DECANTEUR LAMELLAIRE: L2< L1
ANNEXE 5 (3)
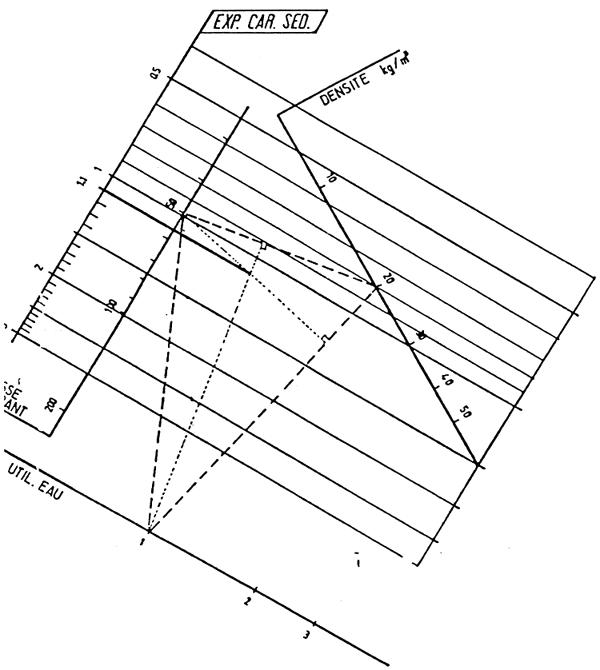
MONOGRAMME DE DETERMINATION
DE L'EXPOSANT CARACTERISOUE OF SEDIMENTATION (B)
FAURE' 1984
ANNEXE 5 (4)
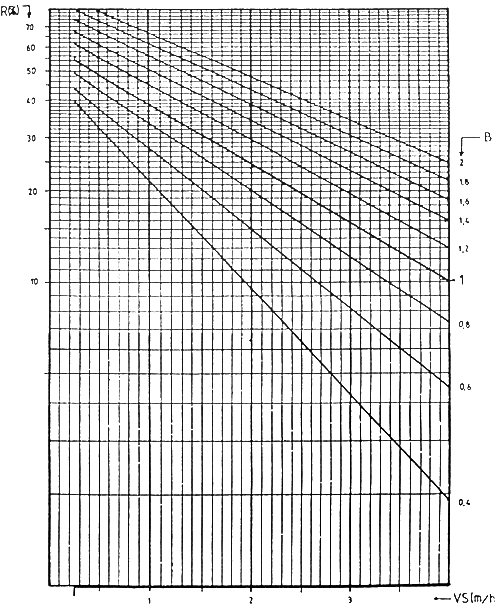
| ABAQUE DE CALCUL DU PRNDEMENT D'UN OUVRAGE DE DECANTATION SUR RE JET DE PISCICULTURE EN FONCTION DE SA VITESSE ASCENSIONNELLE ET DE L'EXPOSANT CARACTERISTIOUE DE SEDIMENTATION |
| FAURE' 1984 |
ANNEXE 6 (1)
ANNEXE 6 -(2)
Effet de la salinité sur la mortalité due à l'ammoniac
ANNEXE 6 - (3)
ANNEXE 6 (4)
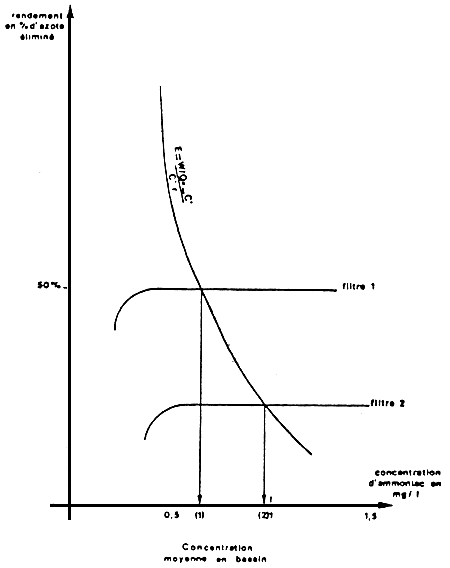
- INTERACTION ENTRE RECYCLAGE ET EPURATION EFFET SUR LA CONCENTRATION de L'AMMONIAC DANS LES BASSINS
ANNEXE 6 (5)
ANNEXE 6 (6)
CUVE D'EPURATION STAHLERMATIC
(prevu pour 1T de production)
ANNEXE 6 (7)
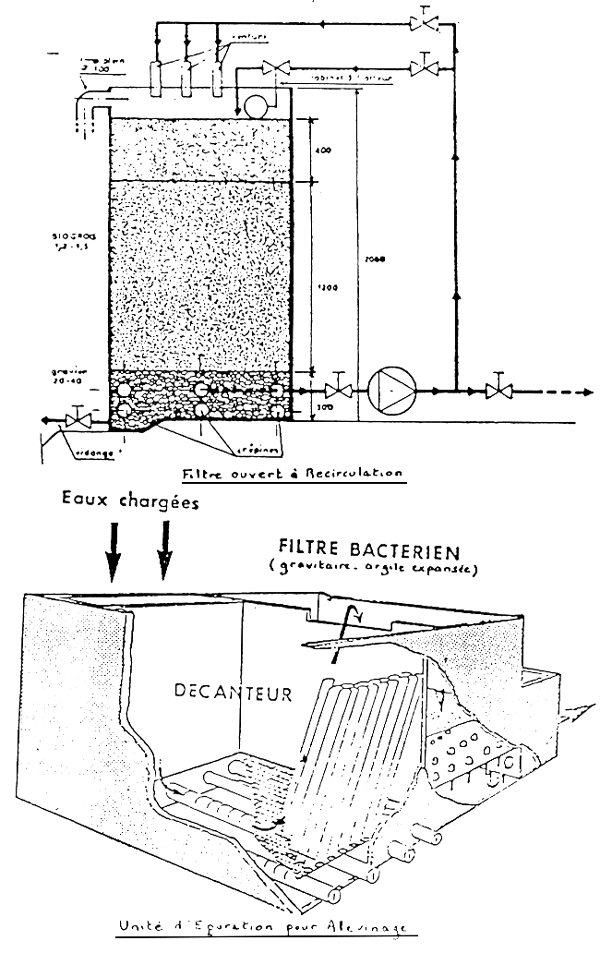
ANNEXE 6 - (8)
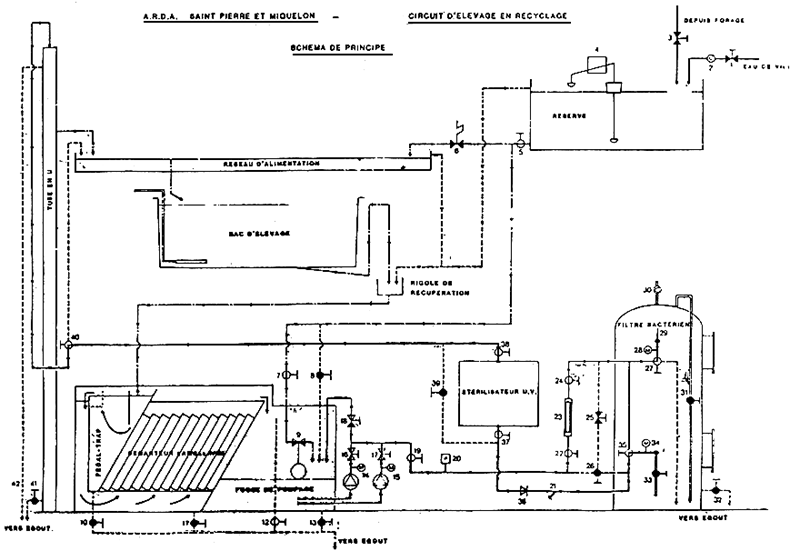
| CUVE DE FILTRATION MONTEE | Module de filtration bacterienne |
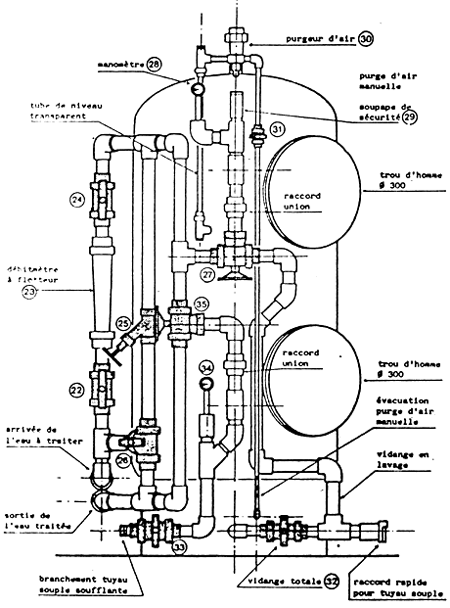 | ELEMENTS DE FACADE DE CUVE LIVRES MON MONTES (1) |
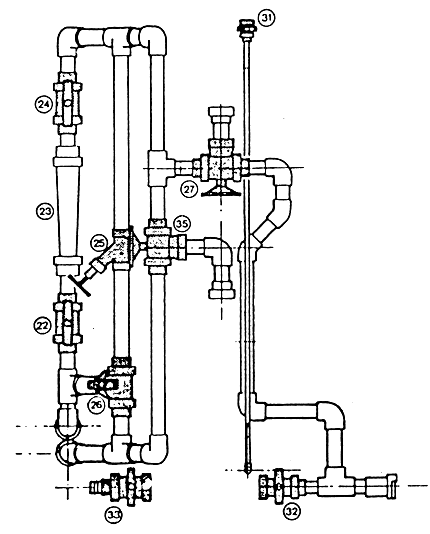 | |
| (1) Sont également livrée non montés: purgeur d'air №30, soupape de sécurité №29, manomètres №28 et 34, tube de niveau transparent. |
ANNEXE 6 - (10)
 |  |
ANNEXE 6 (11)
INTENSITE GERMICIDE NECESSAIRE A LA DESTRUCTION DE DIFFERENTS AGENTS PATHOLOGIQUES