La misión se centró en este departamento tanto a nivel de la organización del trabajo y de consejos técnicos para la producción como para la finalización de la instalación del departamento. En el mes de Mayo, el departamento estaba casi listo. Se decidió arrancar enseguida la producción de algas en previsión de una pronta obtención de algas.
La estructura de producción constituída por esta área es bastante buena. La disposición general del área es conveniente, aunque un poco lejos del de las naves de cría larval. El departamento está bien dimensionado y la disposición de las salas entre ellas favorece la gestión sanitaria. La sala de lavado, cristalería y esterilización, está independiente lo que dificulta su control. El área cuenta con los equipos requeridos.
Hay una sala de cepas y otra de inóculos menores independientes tal como conviene. Las dos comunican con un área central donde se hacen las revisiones de muestras al microscopio, y donde se preparan las soluciones de nutrientes.
Se colocó aire acondicionado en el área central para comodidad y homogeneidad de temperatura con las salas de cepas e inóculos menores. Los algarios utilizados no son óptimos, hay pérdida de espacio debido a las separaciones verticales las que dificultan la limpieza del piso.
Al empezar la producción, estas salas no tenían instalaciones ni de tanques ni de lámparas. Se tenía previsto utilizar pequeños tanques cilíndricos de plástico blanco, no muy transparentes.
Estos volúmenes son bastante regulares:
Por no tener transparencia, la iluminación tiene que hacerse por encima del tanque, sin tapa (las tapas protegen los cultivos del aerosol y bichos, contaminantes en general). Para que no se rieguen los cultivos por la aeración, los tanques no deben utilizarse llenos, de tal forma que éstos tienen un volumen de utilización de 50 litros lo que es bastante limitado como etapa final de cultivo interior (generalmente oscilando entre 200–300 litros)
Se instalaron soportes de madera para las tanquetas y sus respectivas lámparas, con una capacidad de 12 tanquetas por sala. Hechas muy rápidamente, cumplen su función pero no se ven muy presentables. Con el uso, las lámparas metálicas se han oxidado muy rápidamente. Hay posibilidad de disponer más tanquetas en las salas.
1 sala queda destinada para Diatameas, la otra para testraselmis.
El área exterior, con un techo translúcido, recibe tanques de fibra de vidrio semitransparentes sin tapas.
Los volúmenes son :
16 tanques de 500 litros, 8 de 1 m3, 8 de 12 m3, los cuales son repartidos de la misma manera, simétricamente de un lado a otro de un desagüe central. Hay lámparas colocadas encima de los tanques, las cuales no tiene mucha utilidad.
La cantidad de luz provista por dos tubos fluorescentes de 40 cm encima de un tanque de 1 tonelada es casi ineficaz sobre el crecimiento del cultivo pero no sobre los varios y numerosos insectos que amanecen junto con las algas.
El piso no tiene pendiente hacia el canal de drenaje, quedan muchos charcos de agua de mar.
Estas salas son independientes del departamento de fitoplancton en si y se encuentran juntas con los de bacteriologia e hidroquímica. Aunque se encuentren en la misma nave, eso implica idas y vueltas con material delicado y en un sentido estéril. La limpieza y esterilización son muy importantes para la producción ; y el apartamiento de estas salas dificulta el control y la programación del trabajo.
Estas salas disponen de un buen equipamiento :
2 autoclaves lo que permite esterilizar sin problemas toda el agua necesaria para el departamento, l estufa para la esterilización de la cristalería, y l destilador de agua.
El agua disponible en cantidad suficiente, es filtrada a 8 m y atraviesa un fltro de lámparas UV al entrar al departemento.
Generalmente, se considera adecuado un tamaño de filtración de l m para los cultivos de algas. El tamaño de 8 m retiene suficientemente las partículas, de tal forma que microorganismos pueden atravesar las lámparas ultravioletas sin estar expuestos a los rayos, pegados a partículas y protegidos por ellas.
Además, por la estancia del agua en las cisternas exteriores, esta misma filtración presenta una eficiencia relativa. De tal forma que no hay la seguridad de tener un agua libre de microorganismos contaminantes.
• Agua
Lo conveniente es tener una red con pendientes hacia un punto bajo para que se pueda drenar fácilmente. Aqui, para drenar la red, hay que abrir todas las válvulas. Se hizo una extensión hasta el cuarto de limpieza de cristalería para llenar allí con agua de mar los recipientes antes de la esterilización.
• Aire
Igualmente, no hay pendientes ni válvula de drenaje. En las tuberías de aire, siempre se forma agua por condensación, la cual muchas veces trae microorganismos contaminantes. Por no haber pendiente ni drenaje, esta agua termina en los cultivos. Se recomienda instalar un punto de cloación para limpieza de las tuberias de aire con agua clorada cuando se hace un vacío sanitario.
En muchas salas de algas, se añade CO2 al aire para evitar que sea el CO2 un factor limitante al crecimiento. Se recomienda añadir 1 % del aire en CO2. Por eso se coloca un tanque con regulador y conexión a la red de aire. Se controla la cantidad de CO2 echada revisando el pH (Co2 insuficiente, el pH sube; si demasiado CO2, el pH baja) de los cultivos, o instalando debímetros.
Se instaló una tubería de PVC para llevar el fitoplancton por medio de una bomba hasta los tanques de cria larval.
Las algas deben bombearse primero (con una bomba sumergible) desde su tanque de producción hasta un tanque de almacenamiento. De ahí, una bomba fija 3 litros/segundo las bombea en la red de PVC hasta la larvicultura. Este sistema es satisfactorio pero no óptimo, ya que se necesitan dos operaciones de bombeo para alimentar. Pero no habría una bomba suficientemente potente adaptada para bombear directamente de los tanques de producción hasta larvicultura.
Se reorganizarán los tanques exteriores, suprimiendo una etapa, para simplificar el trabajo, ahorrando operaciones de bombeo.
Chaetoceros
El lado destinado a las Diatomeas queda con :
12 tanques de 1 tonelada
3 tanques de 12 toneladas
Contando 5 días de crecimiento en 1 m3 (3 días con un nivel a 500 litros, 2 con tanque lleno) se sacan 2 tanques diarios, de los cuales uno se siembra en 1 tanque grande con 3 m3 de agua y que se puede utilizar a los 2 días.
Este sistema nos permite obtener 5 m3 diarios de densidad aproximadamente 1 millón de células/ml.
Capacidad de producción Diatomeas : 5 m3 ó 5.1012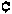 /dia.
/dia.
Tetraselmis
Este lado quedó con :
8 tanques de 500 litros
5 tanques de 12 m3
Los "blooms" de especie tetraselmis demoran más para crecer, pero una vez crecidos, se mantienen varios días en buen estado.
Se siembra 1 tanque de 500 litros por dia. Se deja crecer 5 a 7 días.
Cada 2 días, se siembra un tanque grande con l de 500 litros, (se puede seleccionar a nivel de 500 litros y utilizar solamente los de mejor calidad y crecimiento) y 3,5 m3de agua.
Se deja crecer durante 6 dias, y se utiliza durante 2
días seguidos, de tal forma que se dispone de una
cantidad de 2 m3 por día de concentración aproximada
250 000 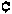 /ml.
/ml.
Capacidad de producción : 2 m3/ día ó 5.1011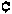 / día.
/ día.
De esta forma, sobran 2 tanques de 12 m3 sin utilización, los cuales pueden sembrarse con una u otra especie si se presentase una necesidad más grande que la prevista de fitoplancton.
Necesidades de larvicultura en fitoplancton
Se van a considerar las necesidades teóricas para 1 nave de larvicultura en las condiciones siguientes :
Densidades de fitoplancton en larvicultura de acuerdo con el protocolo de cría larval utilizado en Cuba.
Producción de mangles correspondientes a la siembra de l tanque al día.
Volumen de los tanques de larvicultura de 20 m3, en los cuales no queda fitoplancton después del recambio de agua, se tiene que añadir cada día la cantidad correspondiente a la densidad requerida.
Chaetoceros
De Nauplii hasta Zoea3, desarrollo de 1 bloom por tanqueta, generalmente sin necesidad de añadir fitoplancton hasta Zoea3.
De Zoea hasta Mysis3, son 5 días entonces 5 tanques necesitando una densidad de 40 000 Chaetoceros/ml.
No de células requeridas por tanque : 4 103 103.2.104= 8.1011 = 0,8 m3
Se requieren 4 m3 de cultivo 1 M/ml al día.
Tetraselmis
De Z2 hasta PL2, son 8 días entonces 8 tanques
Densidad requerida : 2 000 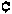 /ml
/ml
No total células requeridas : 3,2.1011 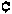
Volumen de cultivo de densidad : 250 000 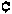 /ml = 1,3 m3
/ml = 1,3 m3
Producción de fitoplancton para las 2 naves
Diatomeas
Las necesidades son en tal caso de 8 m3 al día.
Se puede utilizar la misma secuencia hasta 1 m3, y sembrar los 2 cultivos diarios de 1 m3 en un mismo tanque de 12 m3, con 6 m3 de agua. Este cultivo se utilizaría el cuarto día de crecimiento ; así se necesitarían 4 tanques de 12 m3 en rotación.
Tetraselmis
En este caso, las necesidades son de 3 m3 al día.
Como señalado anteriormente se puede disponer de 1 tanque de 0.5 m3 al día. Entonces hay que inocular cada 2 días, 1 tanque grande con 2 cultivos de 0,5 m3 y 5 m3 de agua, dando un volumen de cultivo de 6 m3. Tal tanque, se utilizaría el séptimo y octavo día; así se necesitarian 4 tanques de 12 m3.
Se puede entonces producir los volúmenes requeridos para las dos naves de larvicultura cambiando solamente la secuencia exterior de producción.
Aquí se indica la producción efectuada en el departamento, asi como los problemas encontrados y algunos comentarios. En este documento técnico se reúnen los esquemas de producción, los consejos técnicos y la rutina diaria de trabajo, constituyendo así un protocolo de trabajo (anexo).
Hubo 2 fases de producción : en Junio/Julio, y en Setiembre.
En previsión de desoves próximos en maduración, se inició la producción el 27 de Mayo, mientras se terminaban los últimos arreglos del departamento. A fines de Julio, se decidió parar la producción por falta de nauplii y la poca probabilidad de tener desoves.
Durante este período, se produjeron 60 toneladas de Chaetoceros y 30 toneladas de Tetraselmis en volúmenes exteriores, se puede decir que son cultivos listos para alimentar.
Se utilizaron aproximadamente 5 ton. de Chaetoceros y 1 de Tetraselmis como alimento para el único tanque de larvas que se crió. Este alimento dió entera satisfacción. Eso permitió probar el sistema de distribución, que resulta satisfactorio.
Se fueron implementando poco a poco los métodos de trabajo adecuados y se estableció una rutina, pero el tiempo de producción real resultó muy corto para que ésto quedara establecido de manera definitiva.
Comentarios relativos a la producción de este período
a) Crecimiento de los cultivos
Al empezar la producción, las concentraciones obtenidas en los volúmenes son muy bajas y el tiempo para obtenerlos muy largo, se puede decir que el crecimiento es insuficiente.
Eso es muy frecuente al iniciar una producción en un departamento de fitoplancton, pues se cometen errores en las manipulaciones, y se presenta que las cepas necesitan siempre un tiempo de aclimatación a las condiciones propias del departamento.
Para obtener mejores concentraciones en los volúmenes iniciales (250 m), se pasaron estos Erlens en la sala de volúmenes menores con aeración (Diatomeas). Al mes las concentraciones eran convenientes.
Concentraciones promedio obtenidas en los diferentes volúmenes en millones de células por ml :
| Volúmenes | Chaetoceros | Tetraselmis | |
|---|---|---|---|
| 250 | ml | 2,8 | 0,8 |
| 1 | l | 2,2 | 1,4 |
| 4 | l | 3,3 | 1,1 |
| 40 | l | 1,2 | 0,32 |
| 0,5 | m3 | 0,8 | 0,3 |
| 1 | m3 | 0,8 | - |
| 4 | m3 | - | 0,35 |
De manera general, la clave para obtener cultivos de buena calidad y con un buen crecimiento es de contar con buenas cepas para sembrar el volumen inicial de cultivo. Eso se alcanza trabajando las cepas, seleccionando los mejores tubos y las mejores células (véase protocolo).
Son las cepas que determinan en su mayor parte la calidad de toda la secuencia que sigue, por lo cual es sumamente importante trabajarlas de manera adecuada.
Se aconseja trabajar las cepas y los volúmenes menores con medio Guillars F/2 que es más completo que el medio A.M.
Hay que señalar en cuanto a este aspecto la influencia negativa de los cortes de luz sobre las cepas (teniendo en cuenta que durante todo este tiempo no había planta funcional) lo que provoca variaciones de temperatura muy dañinos.
b) Contaminación
Este problema es muy frecuente en las salas de algas. Su erradicación o no, es un buen criterio para evaluar la calidad de un departamento de fitoplancton.
Durante este período, las contaminaciones de los cultivos por microorganismos puede atribuirse a varios factores.
Para los volúmenes estériles : falta de mesas de trabajo en las salas correspondientes. Las siembras y repiques estériles se hacen en la sala principal (donde hay bastante movimiento de personal y de material) con un mechero de alcohol dando una llama muy débil. Se insistió para instalar los implementos necesarios : mesas de trabajo y mecheros de gas.
La calidad del agua y de la filtración 8 micras es dudosa. Al parecer protozoarios llegan a pasar vivos en la red del departamento. En este período, el programa de limpieza de los filtros, cartuchos y cisterna no se cumplía aún, y se utilizaron los mismos cartuchos todo el tiempo sin lavarlos. También hay que controlar que el UV se prenda de manera sitemática.
Falta de entrenamiento, de cuidado y de disciplina del personal en los manipuleos, las limpiezas, etc. Eso es normal al iniciar una sala de producción de fitoplancton pero debe corregirse con el tiempo.
Falta de respeto de los tiempos de cultivo de un volumen. Cuando se deja un cultivo más tiempo de lo necesario se corre más riesgos de contaminación ; sobre todo si se deja de estar en fase exponencial de crecimiento, se vuelve en substrato potencial para los macroorganismos y si se contamina se convierte en fuente de contaminación para los otros cultivos.
Importancia de la contaminación
Se notó una tendencia en creer que la contaminación por protozoarios en los cultivos es algo casi normal e inevitable sobre todo en los tanques exteriores. Hay que evitar eso, considerando que :
Más la calidad de un cultivo es buena, menos se contamina.
Lo que se da de alimentos a las larvas son algas y no protozoarios. En un tanque de larvas estos últimos se desarrollan al igual que las algas lo cual no es nada bueno para las larvas.
Si se considera que es normal que los cultivos tengan “algunos” protozoarios, siempre los van a tener. Y si se considera que tienen poco, va llegar rápidamente el momento en que muchos cultivos tengan demasiado.
Si hay protozoarios en una parte del departamento, lo más probable es que los haya en todas partes.
Por lo cual hay que considerar como una norma que no hay que tener protozoarios en ningún cultivo. La ausencia de contaminación es un criterio de la calidad de la gestión sanitaria y del trabajo en general, y a largo plazo de la seguridad de la producción.
c) Area exterior
La producción de Tetraselmis no tuvo problemas. En los tanques grandes, los cultivos con un nivel de 4 m3 se mantienen durante varios día en buena calidad, de tal forma se podría decir que la producción de Tetraselmis se encuentra bastante asegurada.
En lo que concierne a las Diatomeas los cultivos de 1 m3 demoran bastante por crecer y una buena parte se contaminan. Eso debido al volumen limitado del inóculo y a la baja transparencia de los tanques. Los resultados se mejoraron llenando primero el tanque con 500 l y completándolo a 1 m3 el tercer día de crecimiento, así que suministrando una aeración más fuerte.
En los tanques grandes (12 m3) el crecimiento es mejor así que la calidad, probablemente debido a la exposición de los cultivos en un área mayor de luz. Se han utilizado con buenos resultados en un volumen de 4 m3.
El bloom se presenta óptimo durante 1 día, de tal forma que hay que utilizar estos cultivos el tercer día de crecimiento.
Esta primera fase de producción dió los elementos necesarios para el implemento de métodos y técnicas de trabajo, así como para el adiestramiento del personal.
Se vació el departamento, dejando solamente las cepas.
Hubo falta de trabajo y descuido respecto a las cepas, y al fin del mes estaban en mal estado.
Para remediar esta situación, se aconsejó traer cepas de la Facultad de la Habana, pero la persona encargada de traerlas volvió sin nada, con motivo de que estaban de vacaciones. Se trajeron cepas de Manzanillo, pero estaban contaminadas y no se incluyeron en la producción.
Es una seguridad para el centro de desove de poder contar con una fuente de cepas de calidad en caso de problemas.
En previsión de un abastecimiento de progenitores, se vuelve a producir. La producción se limitó a las etapas interiores esperando desoves para seguir hasta las etapas exteriores finales. Solamente se produjeron algunos tanques exteriores de Diatomeas de 1 m3. A pesar de la mala calidad de las cepas, el trabajo encabezado por el responsable del departamento dió buenos resultados y se produjeron rápidamente cultivos de calidad con concentraciones respetables.
Concentraciones promedio obtenidas. Millones de células/ml :
| Volúmenes | Chaetoceros | Thalassiosira | Tetraselmis | |
| 250 | ml | 3,2 | 0,5 | 1,1 |
| 1 | l | 2,2 | - | 0,7 |
| 4 | l | 2,9 | - | 0,6 |
| 40 | l | 1,6 | 0,4 | 0,3 |
| 0,5 | m3 | 0,9 | - | - |
| 1 | m3 | - | 0,2 | - |
Se instalaron las mesas de trabajo en las salas de cepas de cultivos menores, así como los mecheros de gas, lo que facilita el trabajo y permite evitar contaminaciones en estos volúmenes.
Las cepas se trabajaron por siembras en medio sólido, técnica que dió buenos resultados. Pero la gestión del stock de cepas carecía aún de rigor y puntualidad.
Se inició la producción de la especie Thalassiosira con el fin de utilizarla como alimento en larvicultura junto con los Chaetoceros. Pero no se sabe en que estadios ni en que densidades así como no se sabe si la producción que se planificó para esta especie es la adecuada.
En este período, se mejoró notablemente la calidad y la organización del trabajo de las etapas anteriores. Al exterior las necesidades en alimentos son indispensables para organizar el trabajo real de producción y distribución de alimentos.
Las cantidades de fertilizantes utilizadas en los cultivos exteriores según las normas cubanas son bastante elevadas en comparación con las utilizadas en el Ecuador.
Comparación de estas fertilizaciones, por cultivos de 1 000 1 (dosis en g/m3).
| CUBA | ECUADOR | |||
| Diatomeas | Flagelados | Diatomeas y | Flagelados | |
| KNO3 | 50 g | 200 | 4 g | |
| Superfosfato | 5 | 20 | 1 | |
| EDTA | 10 | 10 | 2 | |
| FeCl3 | ? | ? | 1 | |
| Vitaminas | Sí | Sí | No | |
(FeCl3 : ¿ A que cantidad en g corresponden 50 gotas de una solución saturada ?).
La diferencia es muy alta pero hay que tomar en cuenta que en el Ecuador la etapa exterior es muy breve - visto que los tanques de 1 m3 se siembran con 200 1 de inóculo interior y tiene un tiempo de cultivo de 2 días - mientras que aquí son dos etapas exteriores con un inóculo mucho menor, lo que significa una mayor multiplicación celular al exterior es decir una mayor necesidad de nutrientes.
¿ Pero las dosis preconizadas necesitan realmente ser tan altas ?.
La única manera de saberlo sería de dosificar los nutrientes en fin de cultivo, es decir cuando los cultivos estén aptos para alimentar con las secuencias utilizadas.
El personal dedicado a trabajar en el área es más que suficiente. Con las pocas necesidades de producción que hubo, resultó que algunas personas estaban desocupadas una buena parte del tiempo, lo que no es preciso para implementar un rigor de trabajo.
En cuanto a los responsables del área - y eso no solamente para fitoplancton - que viven en Sancti Spiritus, su trabajo se encuentra afectado por el transporte. Debido a la oganización de los turnos es frecuente que los responsables tengan que trabajar 15 días seguidos sus 8 horas diarias, más 3 1/2 h de transporte (con un almuerzo muy mediocre al medio día). Es obvio que eso contribuye a disminuir la eficacia del trabajo y la motivación.
El papel del responsable es de organizar y supervisar el trabajo; y es muy útil que pueda a veces organizar su trabajo, es decir no verse obligado de permanecer 8 horas en el centro cuando necesita solamente dar una instrucción o verificar el trabajo realizado un día que le corresponde descanzar ; y viceversa tiene que poder liberarse en momentos que le corresponde trabajar cuando tiene todo bajo su control.
Se aconseja, tener además de la “guagua”, otro transporte a la disposición de los responsables de área y del centro con el fin de poder organizar su trabajo en función de las necesidades.
En lo que concierne a la Diatomeas, se recomienda, cuando sea posible cambiar los tanques de la sala interior por volúmenes más adaptados a los cultivos y de capacidad superior, a fin de tener una mayor capacidad y seguridad de producción.
Los tanques adecuados son tanques cilíndricos transparentes.
Se podría implementar una etapa suplementaria adentro por ejemplo con la secuencia 4 l→30 l→200 l→ exterior (véase a continuación esquema de instalación).
Así, los tanques de 1 tonelada necesitarían un tiempo de rotación de solamente 3 días, con una seguridad en el crecimiento, menos probabilidad de contaminación y probablemente concentraciones más altas. Disponiendo de los mismos 12 tanques, se podría producir 4 de éstos en lugar de 2.
Para asegurar la producción, es mejor tener siempre como etapa final varios tanques de menor volumen que uno solo de mayor volumen.
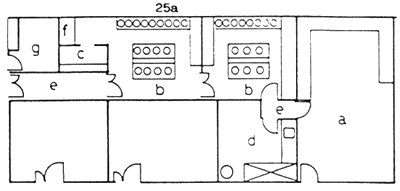
| Figure 1 | scale 1/150 |
ALGAE PRODUCTION UNIT
Laboratory
Culture rooms
Test-tube culture room
Washing and storage room
Air-locks
Filtration
Security blower and electric control
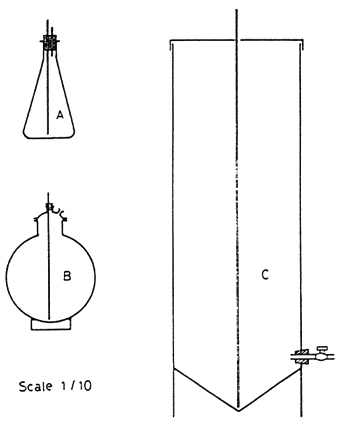
Figure 2
CULTURE VESSELS
2 liter flask
20 liter carboy
300 liter tank