Les produits désinfectants rencontrés sur le marché résultent de l'association d'éléments microbicides et d'éléments qui synergisent leur action, tels que:
Les tensio-actifs qui favorisent le contact entre le produit actif et les germes à détruire.
Les complexants qui évitent les inconvénients dus aux ions calcium et magnésium.
Les sels, les alcalins ou les acides dont le rôle est de maintenir le pH des solutions à la valeur optimale d'activité microbicide du produit.
La connaissance exacte des propriétés des substances désinfectantes est une condition primordiale pour la recherche et la mise en oeuvre de solutions efficaces. C'est ce que nous allons décrire dans les pages suivantes.
Dans les IAA (industries agricoles et alimentaires) les surfaces des équipements ne doivent pas constituer une source de contaminations pour les aliments qui entrent en contact avec elles. Les opérations de nettoyage en fin de fabrication éliminent une partie notable des micro-organismes apportés par les aliments. Mais cette élimination est insuffisante, et un traitement complémentaire s'impose: c'est la désinfection.
Lorsqu'on se propose de réaliser cette opération, il convient de ne pas perdre de vue un certain nombre de données fondamentales.
Il faut tout d'abord connaître la nature des micro-organismes à détruire. Les bactéries gram+, les bactéries gram-, les formes sporulées, les levures, les moisissures, les virus, les bactériophages résisteront différemment à un désinfectant donné.
Il faut ensuite déterminer dans quelles conditions pratiques pourra se dérouler l'opération de désinfection. Les principaux critères à prendre en compte seront:
la possibilité ou non d'utiliser un désinfectant moussant.
Les deux points précédents doivent permettre de sélectionner quelques bases désinfectantes parmi toute la panoplie des molécules actives disponibles. Le choix final sera fait après considération des critères ci-après:
Aspect législatif: dans certains pays, il existe une liste positive. Dans tous les cas, il faudra vérifier que le désinfectant pressenti est bien autorisé.
Vérifier la qualité du nettoyage préalable à la désinfection. En effet, certains désinfectants sont beaucoup plus sensibles que d'autres à la présence de matière organique résiduelle sur les supports à désinfecter.
S'assurer que le désinfectant à la dose d'utilisation n'aura pas d'effet corrosif notable sur le support à désinfecter.
Tenir compte du phénomène d'accoutumance qui peut exister avec certaines molécules désinfectantes.
Vérifier que les composés qui peuvent apparaître secondairement ne sont pas toxiques, ne nuisent pas aux propriétés organo-leptiques du produit, ne gênent pas le bon déroulement du traitement.
Si après avoir considéré tous les critères précédents, plusieurs molécules actives ou plusieurs produits commerciaux peuvent être retenus, le choix final se fera en tenant compte des facilités d'utilisation (sécurité du personnel, facilité du contrôle du rinçage, etc.) de l'efficacité et du prix de revient de l'opération de désinfection.
Le produit de désinfection “miracle” n'existe pas. Dans la pratique industrielle, on se contente donc de compromis qui visent à assurer la sécurité du personnel des usines et celle du consommateur.
Il faut toujours se souvenir que le vrai problème n'est pas toujours l'opération de désinfection en elle même, mais plutôt le maintien des surfaces exemptes de germes en attendant la mise en service de l'installation. En effet, la désinfection est une opération au résultat momentané, limité aux micro-organismes présents au moment de l'opération.
Le problème de l'accoutumance des germes aux substances microbicides a été soulevé par le corps médical qui s'est aperçu qu'après des dosages trop faibles d'antibiotiques, il devenait difficile voire impossible de détruire le micro-organisme combattu. Ceci s'explique lorsqu'on sait que ces substances agissent par l'inhibition à des points précis de métabolisme de cellules sans déranger l'organisation intime de la cellule.
Ce phénomène n'arrive pas, heureusement, avec les désinfectants à action destructive (chlore, iode, oxydants, aldéhydes, etc.) utilisés à des doses convenables. Ces produits ont une action irréversible et ne peuvent, lorsque la dose utilisée est bactéricide, provoquer des phénomènes d'accoutumance. Si la concentration d'utilisation est très proche du seuil d'inhibition, on observe un phénomène que certains assimilent à tort à une résistance. En effet, on peut, si les concentrations d'utilisation sont trop faibles, assister à un développement très important des germes en culture car la fraction du peuplement bactérien épargnée se trouve en présence de réserves nutritives plus importantes et peut s'y développer d'autant mieux. On parlera alors de résistance apparente.
Certaines substances chimiques créent par contre des phénomènes de résistance: ce sont les ammoniums quaternaires, les phénols, et surtout les tensio-actifs amphotères.
Ce phénomène se manifeste chez l'industriel par la nécessité d'augmenter la concentration du produit désinfectant utilisé ou le temps d'action ou encore la température.
Ces phénomènes de résistance soudaine peuvent être dus à:
Une mutation au niveau du matériel génétique de la cellule qui devient ainsi insensible à la substance antibactérienne. La cellule agressée peut shunter le mécanisme bloqué, utiliser une autre voie et s'assurer ainsi un développement normal.
Induction par l'agent antibactérien d'un enzyme spécifique synthétisé par la cellule dégradant l'agent antibactérien.
Induction d'un métabolite compétitif qui inhibe l'action de la substance antibactérienne.
Dans le cas d'accoutumance, il se produit une mutation et les nouveaux microorganismes ainsi modifiés sont appelés “mutants résistants”.
Dans les cas extrêmes, la résistance peut devenir telle que la substance peut devenir indispensable à la croissance de la cellule (cas de la streptomycine).
Expérience
Voici une expérience faite en laboratoire sur trois produits à base d'ammonium quaternaire, de phénol et de savon d'amphotère.
On réalise une série inhibitrice selon le schéma suivant:
| BOUILLON |  |
| + | |
| SUSPENSION | |
| BACTERIENNE | |
| + | |
| DESINFECTANT EN | |
| CONCENTRATION | |
| CROISSANTES |
Après incubation, il se produit un trouble dans les tubes où la concentration est inférieure au seuil d'inhibition.
On ensemence une nouvelle série inhibitrice à partir du dernier tube montrant un développement bactérien et on recommence l'opération sur plusieurs jours.
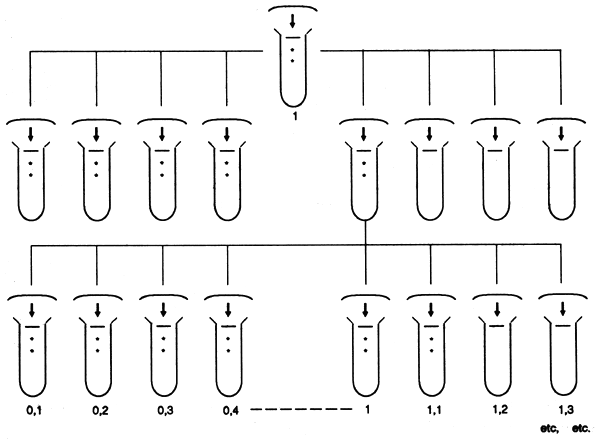
On s'aperçoit, après plusieurs passages, que la concentration nécessaire pour provoquer l'inhibition des germes a sensiblement augmenté. Après 40 passages environ, la concentration d'inhibition n'évolue plus.
On effectue le rapport de la moyenne des 10 concentrations finales sur la moyenne des 10 concentrations initiales. On obtient le facteur d'accroissement.
Après examen des facteurs d'accroissement, on s'aperçoit que les ampholytes sont très sensibles à l'accoutumance sur les pseudomonas, que les ammoniums quaternaires présentent le même phénomène sur ce germe mais de façon moins prononcée et que les phénols sont des produits à utiliser avec prudence sur Escherichia coli.
Cette expérience montre que la sécurité bactériologique initiale donnée par les amphotères, n'est plus satisfaisante. L'industriel qui veut assurer une bonne désinfection de son matériel pour obtenir une meilleure qualité bactériologique de son produit doit au moins multiplier par 16 la concentration d'utilisation du désinfectant. La charge financière devient alors intolérable.
Selon la méthode de neutralisation retenue, on applique la norme NFT 72–150 (méthode par dilution neutralisation) ou la norme NFT 72-151 (méthode par filtration sur membrane).
L'opération consiste à déterminer la concentration minimale à laquelle un produit est capable de réduire d'au moins 105 fois le nombre de cellules vivantes appartenant à des souches définies de cinq espèces bactériennes en 5 minutes de contact à 20 °C.
Les souches de référence sont:
| - Pseudomonas aeruginosa | CNCM A 22 |
| - Escherichia coli | CNCM 54 127 |
| - Staphylococcus aureus | CNCM 53 154 |
| - Streptococcus foecalis | CNCM 58 55 |
| - Mycobacterium smegmatis | CNCM 73 26 |
D'autres espèces bactériennes peuvent être essayées selon le même protocole mais uniquement en complément des cinq souches de référence.
L'expertise se déroule en deux temps:
Essais “préliminaires” visant à déterminer et à valider la méthode de neutralisation utilisée (filtration sur membranes ou dilution-neutralisation).
Essais “proprement dit” où les cinq suspensions bactériennes sont mises en contact pendant 5 minutes à 20 °C avec différentes concentrations du produit essayé.
Par dénombrement des cellules avant et après le temps de contact, on détermine la concentration bactéricide qui correspond à la concentration permettant de réduire les cinq populations bactériennes de 105 fois (99,999%).
Comme pour l'activité bactéricide, deux schémas opératoires peuvent être employés (T 72-200: méthode par dilution-neutralisation ou T 72-201: méthode par filtration sur membranes).
On détermine l'activité fongicide en mesurant la concentration minimale à laquelle un antiseptique ou un désinfectant est capable de réduire d'au moins 105 fois le nombre de spores de moisissures et le nombre de cellules végétatives de levures appartenant à des souches déterminées de quatre espèces de micromyces en 15 minutes à 20 °C ou en 5 minutes à 50 °C. Les souches de référence sont:
| - Aspergillus versicolor | CNCM 1187-79 |
| - Cladosporium cladosporoides | CNCM 1185-79 |
| - Penicillium verrucosum, var cyclopium | CNCM 1186-79 |
| - Candida albicans | CNCM 1180-79 |
Le schéma opératoire et le mode d'interprétation des résultats sont identiques à ceux décrits pour la bactéricidie.
Les normes T 72-230 et T 72-231 permettent de déterminer les activités sporicides dans des conditions standards, mais également en présence de substances définies (voir NFT 72-170 et T 72-171).
Les schémas opératoires sont les mêmes à l'exclusion des conditions de contact entre le désinfectant et les spores bactériennes qui deviennent 60 minutes à 20 °C ou 5 minutes à 75 °C. Les souches de référence utilisées sous formes sporulées sont:
| - Bacillus cereus | CNCM 7803 |
| - Bacillus subtilis, var. niger | CNCM 7718 |
| - Clostridium sporogenes | CNCM 7939 |
Une formulation est reconnue sporicide si elle peut réduire de 105 fois le nombre de spores de ces trois souches dans les conditions de temps et de température choisis.
La norme T 72-180 permet de déterminer la virucidie vis-à-vis de souches virales d'origines humaines et animales (secteur hospitalier). La norme T 72-181, établit de même l'activité virulicide mais utilise comme modèle viral, trois souches de bactériophages (secteur bio-industriel).
La méthode est calquée sur celles correspondant aux autres pouvoirs désinfectants.
L'activité virulicide vis-à-vis des bactériophages correspond à la capacité de réduire de 104 fois le nombre de virions des trois souches de référence après un contact de 15 minutes à 20 °C.
Les normes NFT 72-170 et T 72-171 sont établies sur les mêmes principes que les normes NFT 72-150 et T 72-151 auxquelles elles font référence. Elles permettent d'apprécier la destruction en 5 minutes de contact à 20 °C et en présence de substances interférentes, de 99,999% des bactéries de cinq espèces différentes.
Appliquées secondairement aux méthodes de base, elles permettent de comparer les concentrations bactéricides en absence et en présence de substances diverses susceptibles de modifier l'activité désinfectante des antiseptiques ou désinfectants.
Quatre substances interférentes sont proposées en référence:
Si ces conditions ne représentent pas la situation pratique, d'autres mélanges peuvent être essayés selon le même protocole (matière grasse, lait, sucre, etc.). Il s'agit ici de normes d'application dont l'intérêt est considérable.
L'essai consiste à déposer des bactéries sur un support inerte de référence. Après séchage de l'inoculum, on recouvre le support ainsi contaminé massivement d'une solution désinfectante à essayer.
Le temps et la température de contact sont choisis par le fabricant.
Après traitement, on recherche les bactéries survivantes par rinçage et agitation puis filtration sur membranes.
Cette norme permet ainsi d'établir des concentrations auxquelles un désinfectant est capable de réduire d'au moins 105 fois le nombre de bactéries appartenant à des souches déterminées de quatre espèces bactériennes.
Les souches de référence sont les mêmes que pour les autres essais de bactéricidie à l'exclusion de mycobactérium smégmatis.
Les supports de référence proposés sont:
Ici encore d'autres supports non poreux et des souches complémentaires peuvent être employés.
La norme NFT 72-271 a pour objet la description d'une méthode de détermination de l'activité antibactérienne des procédés de décontamination par voie aérienne à la surface des supports déterminés dans des conditions de température et d'hygrométrie contrôlées et dans des enceintes closes. Elle permet de qualifier les couples “produit/matériel” qui restent indissociables. La méthodologie est calquée sur celle de la norme NFT 72-190.
Les souches de référence utilisées sont:
| - Escherichia coli | CNCM 54127 |
| - Staphylococcus aureus | CNCM 53154 |
| - Streptococcus foecalis | CNCM 5855 |
| - Bacillus subtilis, var. niger | CNCM 7718 (spores) |
L'efficacité des procédés est basée sur la démonstration d'une réduction de 103 fois des bactéries et des spores bactériennes dans les conditions fixées par la norme.
L'ensemble des normes proposées est parfaitement cohérent dans l'esprit et par la méthodologie; il permet une exploration complete des propriétés antimicrobiennes et l'étude des qualités technologiques des formulations.
Il existe un très grand nombre de composés chlorés antimicrobiens disponibles dans le commerce.
Parmi les composés chlorés utilisés en industrie alimentaire nous citerons:
Les hypochlorites alcalins: le plus populaire est certainement l'eau de javel ou hypochlorite de sodium.
Les phosphates trisodiques chlorés.
Les acides chlorocyanuriques et les chlorocyanurates.
Les chloramines.
La dénomination “eau de Javel” fut d'abord donnée par Berthollet à la solution obtenue par absorption du chlore dans une solution de potasse. C'est Labarraque qui proposa une solution d'hypochlorite de soude au lieu de potasse, la soude devenant un produit plus courant que la potasse, et c'est ainsi que la dénomination “eau de Javel” fut par la suite attribuée aux solutions d'hypochlorite de sodium et le mot “javellisant” étendu à tout produit donnant naissance à des hypochlorites.
L'hypochlorite de sodium s'obtient suivant la réaction théorique suivante:
2 Na OH + 2 Cl →Na O Cl + Na Cl + H2O
Le produit commercial contient un excès de soude et un peu de bichromate qui joue le rôle de stabilisant et surtout de colorant.
On définit une eau de Javel par son degré chlorométrique. C'est le nombre de litres de chlore gazeux, mesurés à 0 °C et 760 mn de mercure, nécessaires pour fabriquer un litre d'eau de Javel suivant la réaction théorique citée précédemment.
Le produit commercial change de nom en fonction de la dilution et on parlera:
D'extrait de javel pour un produit titrant 40 °C chlorométriques minimum.
D'eau de Javel si la concentration est comprise entre 12° et 35° chlorométriques.
D'eau de Labarraque pour un produit titrant 2° chlorométriques.
La liqueur de Dakin est une eau de Labarraque dont l'alcalinité a été neutralisée par l'acide borique.
Un litre d'extrait de javel à 50° chlorométrique pèse environ 1 250 grammes et renferme approximativement:
937,0 grammes d'eau
166,0 grammes Na O Cl
132,0 grammes Na Cl
15,0 grammes Na OH
0,5 grammes Bichromate
Comme on le voit, 50% seulement du chlore initial se trouve dans ce que l'on considère comme étant le principe actif, c'est-à-dire Na O Cl.
NaCl et NaOH sont également des désinfectants mais aux conditions habituelles d'utilisation, leurs concentrations ne sont pas suffisantes et il faut considérer essentiellement l'action de l'hypochlorite.
Ces produits sont caractérisés par le groupement -N -Cl
Ce groupement réagit avec dés ions chlore (par exemple de H Cl) en donnant du chlore actif suivant la réaction:
-N -Cl + H Cl →N - H + Cl2
Ces corps dont l'action est voisine de celle des hypochlorites, présentent sur ceux-ci l'avantage d'une meilleure stabilité au stockage.
L'ammoniaque réagit avec l'acide hypocloreux ou les chlorites pour donner de la chloramine (NH2Cl) ou de la chlorimine (NHCl2).
NH3 + H ClO →NH2Cl + H2O
Ce nom de chloramine a été improprement étendu aux composés résultant de la chloration des sulfonamides, de composés hétérocycliques ou de l'acide cyanurique et qui libèrent de l'acide hypochloreux par l'hydrolyse.
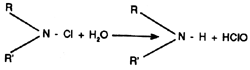
Parmi les chloramines dérivant des sulfonamides on utilise:
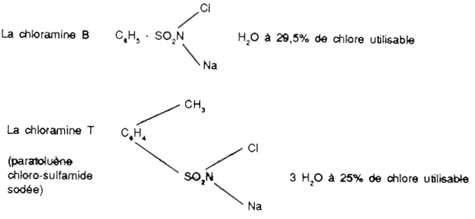
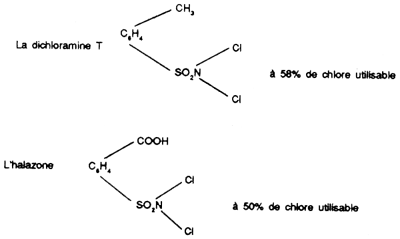
Parmi les chloramines dérivant d'électrocycles, nous citerons:
| Le dactin ou halane avec 77,6% de chlore utilisable |  |
| La succinchloramide avec 52% de chlore utilisable |  |
Les chloramines dérivant de l'acide cyanurique ont acquis une importance particulière. Elles libèrent de l'acide hypochloreux ou des hypochlorites suivant le pH. Ces dérivés sont ajoutés en pourcentages variables à des mélanges de trypolyphosphate, de métasilicate, de sulfate pour constituer des détergents-désinfectants et des agents de blanchiment. On les emploie également pour le traitement des eaux de piscine, pour le chlorage des dextrines servant à fabriquer des colles.
| Acide trichloroisocyanurique teneur réelle en chlore actif 85%. Solubilité en g dans 100 ml eau: à 27 °C: 1,21 |  |
| Acide dichloroisocyanurique teneur réelle en chlore 70%. Solubilité en g dans 100 ml eau: à 27 °C: 2,64 |  |
| Dichloroisocyanurate de sodium teneur réelle en chlore actif 60%. Solubilité en g dans 100 ml eau: à 27 °C: 33 |  |
Le chlore agit par oxydation des matières organiques suivant le schéma suivant:

Chlore dissous.
OU Na O Cl + H2O ⇌ H Cl O + Na+ + OH-Hypochlorite.
OU NH2 Cl + H2O ⇌ H Cl O + N H4 + + OH-
Chloramine Acide hypochloreux
L'acide hypochloreux s'ionise dans l'eau suivant le pH et la température:
HOCl ⇌ H+ + Cl O-
Pratiquement, à pH < 6 tout le chlore est sous la forme H O Cl, à pH > 9 il est sous la forme Cl O-.
Pour connaître la proportion relative de chacune des deux formes, l'utilisateur devra se reporter à des tableaux ou à des courbes.
En effet, bien que certains germes, puissent être plus sensibles soit à l'acide hypochloreux, soit à l'ion hypochlorite, l'activité germicide est liée essentiellement à l'acide hypochloreux non dissocié, aussi bien pour les bactéries que pour les virus.
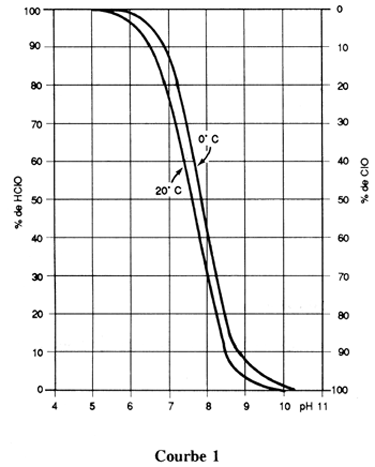
En fonction du pH, on retrouve ces trois espèces
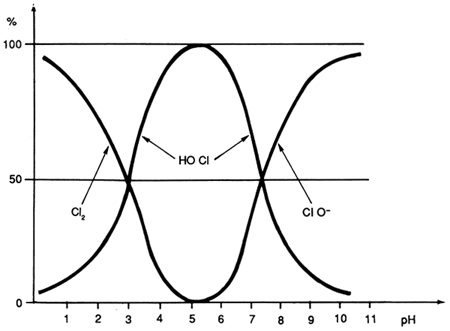
| 4 < pH < 6 | tout en HClO |
| 5 < pH < 9 | formation de ClO- |
| pH > 9 | tout en ClO- |
| pH < 4 | tout en Cl2 |
Valeurs pour une température = 20 °C
| Valeur de pH | % H Cl O non dissocié | % ions hypochlorites |
| 4 | 100 | 0 |
| 5 | 96 | 4 |
| 6 | 95 | 5 |
| 7 | 78 | 22 |
| 7,5 | 58 | 42 |
| 8 | 22 | 78 |
| 9 | 2 | 98 |
| 10 | 0 | 100 |
L'effet du pH
| pH | 6 | 6,5 | 7 | 7,5 | 8 |
| Chlore gazeux | 9,5 | 10,3 | 13 | 20,5 | 47 |
| Cl O Na | 8,5 | 9,2 | 12,8 | 20,5 | 42 |
| (Cl O)2 Ca | 8,5 | 11 | 14,3 | 19 | 48 |
| Chloramine | 105 | 115 | 190 | 250 | 360 |
(Mercer, 1953).
Temps nécessaire en minutes pour stériliser une suspension de spores de bacillus. Tous les produits présents à 15 ppm de chlore disponible dans divers tampons.
Effect de la température
On augmente l'efficacité en élevant la température. Une élévation de 10 °C diminue le temps de stérilisation de 60% à 80% mais la solubilité du chlore gazeux diminue avec la température.
Dans la pratique, les désinfectants chlorés seront toujours utilisés à des températures inférieures à 70 °C.
Les matières organiques
Les produits non azotés (amidon, sucre) ont peu d'action sur l'efficacité du chlore. Le chlore se combine aux produits azotés d'autant plus rapidement que le pH est alcalin.
Résistance au chlore de différentes espèces
Les spores sont 10 à 1 000 fois plus résistantes que les formes végétatives. Mercer a trouvé un parallélisme entre la résistance à la température et la résistance au chlore.
Il a été observé que E. coli est plus résistant au chlore que les autres microbes.
C'est ce qui l'a fait choisir comme germe test pour apprécier la qualité d'une désinfection au chlore.
Les désinfectants à base de chlore actif sont généralement proposés à des pH alcalins afin d'avoir une corrosion beaucoup plus faible qu'en cas d'utilisation d'eau de Javel et d'obtenir une plus grande stabilité du chlore.
Beaucoup de ces désinfectants contiennent des inhibiteurs de corrosion (silicates) afin de pouvoir être utilisés sur l'aluminium et ses alliages.
Ces désinfectants pourront également contenir des complexants, des tensio-actifs et des antimousses.
Le chlore en solution alcaline est actif à partir de quelques ppm sur les bactéries jusqu'à 50 ppm sur les spores bactériennes.
Exemple d'activité d'un détergent désinfectant chloré
Caractéristiques physico-chimiques
| Présentation | Poudre |
| Nature | Alcalin chloré |
| pH de la solution à 1% | 12,6 |
| Teneur en chlore à 1% | 280 ppm |
| Tenue au stockage | 6 à 9 mois |
Activité microbicide
Efficacité microbicide selon le test 3 × 5
(norme AFNOR NFT T 72-150) à 20 °C
| Germes testés | Population
initiale g/ml | Concentration en alcalin chloré | |||||
| 1,5% | 2,0% | 2,5% | 3,0% | 3,5% | |||
| Staphylococus
aureus CNCM 53154 | 5,95.106 | E | 0 | 0 | 0 | 0 | |
| Streptococcus
faecalis ATCC 10541 | 85,2.106 | E | 0 | 0 | 0 | 0 | |
| Pseudomonas
fluorescens ATCC 17397 | 16,5.106 | E | 255 | 0 | 0 | 0 | |
| Escherichia
coli ATCC 10536 | 7,9.106 | E | 1970 | 80 | 0 | 0 | |
| Mycobacterium
smegmatis IPP 7326 | 7,2.106 | E | E | E | E | E | |
| pH de réaction | 10,5 | 10,6 | 10,7 | 10,8 | 10,9 | ||
Détermination de la concentration de chlore
Méthode colorimétrique (pour faibles concentrations)
Appareil: 1 tube jaugé à 10 et à 11 m
Réactif: solution standard d'Orthotoluidine
Mode opératoire:
Remplir le tube jusqu'au trait de jauge 10 ml avec la solution à doser, puis
Ajouter 1 ml d'Orthotoluidine,
Agiter vigoureusement,
Comparer la coloration à celle obtenue avec des solutions de concentration connue.
Méthode volumétrique
Réactifs: solution d'iodure de potassium à 10%;
solution de thiosulfate de sodium N/10
acide sulfurique ou phosphorique à 25%
empois d'amidon à 1%
Mode opératoire:
Prise d'échantillon 100 ml
Ajouter 10 ml de solution d'iodure de potassium, et
Acidifier avec l'acide sulfurique ou phosphorique jusqu'à obtention d'une coloration brun foncé, puis
Titrer par le thiosulfate N/10 avec addition d'empois d'amidon.
Calcul:
Nombre de ml de thiosulfate de sodium N/10 × 35,457 = mg/l de chlore actif.
Avantages
Inconvénients
L'iode est un des produits de désinfection que l'on connaît depuis très longtemps. La première utilisation de l'iode fût le traitement du goitre en 1816. A la même époque fut généralisé l'emploi de la teinture d'iodé et des liniments iodés. Plus tard, l'iode fut largement utilisé comme désinfectant, soit d'instruments, de locaux, de l'eau, etc.
De nos jours, les industries alimentaires n'utilisent plus d'iode mais uniquement des iodophores qui ne sont pas, à proprement parler, des composés de l'iode mais des mélanges d'iode et de substances tensio-actives. Les produits iodés ainsi formulés agissent en phase acide alors que les produits chlorés agissent en phase alcaline.
Les spectres d'action de l'iode et du chlore sont voisins. Tous deux sont actifs contre les micro-organismes, y compris les virus. Pour l'un comme pour l'autre, l'addition d'un mouillant (qui se trouve automatiquement dans l'iodophore) améliore l'action désinfectante.
Dans les iodophores, les substances tensio-actives jouent le rôle de support et de solubilisant de l'iode. Des agents anioniques, cationiques, et non ioniques peuvent être utilisés, mais généralement, les préparations les plus stables sont obtenues avec les substances non ioniques. Parmi celles-ci, toutes ne conviennent pas, les unes ne peuvent pas servir de support à I2, les autres sont insuffisamment solubles dans l'eau.
Dans les solutions aqueuses d'iode en présence d'iodure, il s'établit un équilibre:
I2 + I- ⇋ I3-
Si bien que la quantité de I2 reste toujours limitée par rapport à la quantité d'iode totale.
En désinfection, l'acide hypoiodique ne joue aucun rôle; seul l'iode sous la forme moléculaire I2 est bactéricide. Dans les iodophores où l'iode est amené en solution avec un solubilisant autre que l'ion I- il n'y a pas de perte d'iode par conversion en ion inactif I3-. C'est la raison pour laquelle il suffit d'une concentration moins élevée pour obtenir le même effet létal.
pH de la solution
Les iodophores ne peuvent être confectionnés qu'en milieu acide, l'iode perdant son activité désinfectante en milieu alcalin. On admet que les plus fortes activités bactéricides sont observées entre pH 3 et pH 5.
Pour tamponner les solutions d'iodophores, on utilise généralement l'acide phosphorique.
Les dépôts de tartre qui pourraient parfois se former avec les détergents alcalins ou les produits désinfectants à base de chlore ne risquent bien entendu pas de se former avec l'emploi de produits iodophores acides.
Les quantités de matières actives nécessaires sont avec l'iodophore moins élevées que pour les préparations chlorées; car pour des raisons de stabilité et de sécurité vis-à-vis de la corrosion, ces dernières ne peuvent être utilisées à leur pH optimum (pH 5–7).
La souillure organique
Les halogènes en général sont sensibles aux matières organiques et plus particulièrement, aux protéines. L'halogène et les protéines donnent un complexe non bactéricide, ce qui réduit d'autant la quantité d'halogène bactéricide disponible. Si la quantité de protéines est suffisante, la solution désinfectante peut devenir complètement inefficace. L'iodophore n'échappe pas à cette regle quoique l'on admette généralement qu'en présence de protéines, l'iode est beaucoup plus efficace que le chlore.
Galesloot a calculé que dans un volume de 100 ml de solution d'iodophore à pH 3,5 – 5 ou 7 en une minute, 25 ppm d'iode sont inactivés respectivement par 5 ml, 1,5 ml ou 0,5 ml de lait.
Mueller observe que l'addition de 1 % de lait entier (en eau distillée ou en eau dure) double la durée nécessaire pour détruire complètement les germes en suspension dans le cas d'une solution d'iodophore à 25 ppm d'iode (pH 3) et que cette durée peut être multipliée par 20 dans le cas d'une solution à 12,5 ppm d'iode (pH 3,5) sur P. aeruginosa.
On retrouve souvent dans la littérature des comparaisons telles que “l'iode est 6 à 8 fois plus actif que le chlore” ce qui traduit généralement un rapport des nombres de ppm de l'halogène nécessaire pour obtenir un effet déterminé. Le rapport de matières actives évoqué ci-dessus se modifie en présence d'une légère charge de souillure pour tomber au rapport 1:4.
Dans une solution sans aucune souillure, l'iode concentré entre 15 et 30 ppm à pH 3 est aussi germicide qu'une solution chlorée à pH 9 concentrée entre 100 et 200 ppm de chlore.
La température
Il y a unanimité des auteurs pour reconnaître que l'activité des iodophores n'est pas influencée par une élévation de température.
On conseille d'éviter les températures supérieures à 40 °C en raison des pertes par sublimation de l'iode et des risques d'avoir une corrosion pratiquement incontrôlable.
Les solutions sont généralement utilisées à la température ambiante. On a même observé qu'entre +2 et +5 °C elles ont encore le ¼ de leur activité initiale.
Corrosivité des iodophores
L'aluminium et ses alliages ne sont pas attaqués d'une manière appréciable mais une réserve est à faire, dans la pratique, dans le cas d'une longue utilisation.
Si le produit corrode peu l'acier inoxydable, il semble que les vapeurs d'iode, au contraire, le corrodent sérieusement. C'est ce qu'ont montré des essais en laboratoire et ce que confirme l'examen de réservoirs dans lesquels on a laissé séjourner des solutions d'iodophore en gardant le couvercle fermé ou partiellement fermé.
Sur les parties en caoutchouc (tuyauteries et joints) l'iode se dépose facilement et passe ensuite dans le produit (en risquant de donner une odeur au lait par exemple).
On a noté une grande absorption de l'iode par le buna et le caoutchouc (en 3 jours, 1 ppm d'iode par gramme de caoutchouc) moins par le néoprène.
Stabilité des solutions iodées
Il a été montré que des solutions diluées d'iodophore (33 ppm) se conservent moins longtemps que des solutions d'hypochlorite (187 ppm).
| Temps de conservation | 1 jour | 7 jours | 15 jours |
| Perte désinfectant | |||
| Iodophore (33 ppm) | 6,3% | 12% | 45% |
| Chlore (187 ppm) | 1,8% | 3,7% | 8% |
Note: La conservation a lieu en flacon brun, à l'abri de l'air et de la lumière et à température ambiante.
On devra retenir qu'il y a lieu de préparer extemporanément les solutions aux doses d'utilisation.
La concentration et la durée d'action
Un point intéressant à noter, dans le cas particulier des iodophores, est la relation étroite qui existe entre la couleur des solutions, la teneur en iode et l'action bactéricide. La couleur visible à l'oeil nu disparaît alors qu'il reste encore environ 6 à 8 ppm d'iode et qu'à cette teneur l'activité est très réduite, voire nulle. La couleur suffit pour donner un idée approximative de la “force” d'une solution.
La concentration d'iode efficace vis-à-vis des formes végétatives des bactéries est de l'ordre de 50 ppm ou moins dans certains cas. Les différences d'appréciations que l'on rencontre dans la littérature sont souvent dues aux différences entre les conditions expérimentales (pH, présence de protéines notamment). La dose minimale reconnue efficace par plusieurs auteurs, le plus souvent en l'absence de protéines est de l'ordre de 25 ppm d'iode.
Un iodophore industriel ayant une teneur en iode de 100 ppm à 1% a l'activité indiquée dans les tableaux ci-après:
Activité microbicide
Activité microbicide d'après le test de suspension
| Germes testés | x 106/ml | Concentration | ||
| 0,15% | 0,3% | 0,5% | ||
| Staphylococcus aureus | 510 | 2 | 1 | 0,5 |
| Streptococcus faecalis | 240 | 2 | 1 | 0,5 |
| Escherichia coli | 2 210 | 2 | 0,5 | 0,5 |
| Pseudomonas aeruginosa | 2 500 | 2 | 0,5 | 0,5 |
| Bacillus subtilis | 5,10 | 0,5 | 0,5 | 0,5 |
| Saccharomyces cerevisiae | 5,9 | 30 | 2 | 2 |
| Pichia membranaefaciens | 30 | 8 | 2 | 1 |
| Oospora lactis | 3,6 | 1 | 1 | 0,5 |
| Penicillium camerunense | 28 | 60 | 60 | 30 |
| Aspergillus niger | 6,6 | 60 | 60 | 15 |
| Byssochlamis species | 7 | 15 | 8 | 2 |
Temps de contact en minutes nécessaires à la destruction des germes. Température: 20 °C.
Détermination de la concentration minimale bactéricide
| Germes testés | NaOCl (12%
Cl2) % | Désinfectant iodé % | |||||||||
| ,15 | ,25 | 0,3 | 0,4 | 0,5 | 0,6 | ,15 | 0,2 | ,25 | 0,3 | 0,4 | |
| Escherichia coli 3.108 g/ml | |||||||||||
| Culture | 3/5 | 3/5 | 0/5 | 0/5 | 0/5 | 0/5 | 5/5 | 5/5 | 5/5 | 0/5 | 0/5 |
| Subculture | 0/2 | 0/2 | |||||||||
| Streptococcus faecalis 3.108 g/ml | |||||||||||
| Culture | 5/5 | 5/5 | 5/5 | 0/5 | 0/5 | 0/5 | 5/5 | 5/5 | 0/5 | 0/5 | 0/5 |
Temps de contact: 10 mn
Température: 22 °C
La CMB: est fixée à: 0,3 % pour E. coli
0,25% pour St. faecalis.
Activité bactéricide selon la norme AFNOR NFT 72-150
| Concentration en % | ||||||
| Souches | Populations initiales bact/ml | 0,1 | 0,5 | 1 | 1,5 | 2 |
| Pseudomonas fluorescens ATCC 17397 | 5,4 .106 | E | 460 | 0 | 0 | 0 |
| Escherichia coli ATCC 10536 | 64,2 .106 | E | E | 0 | 0 | 0 |
| Staphylococcus OxfordIPP 53154 | 19,0 .106 | E | E | 0 | 0 | 0 |
| Staphylococcus faecalisATCC 10541 | 0,8 .106 | E | 1 230 | 15 | 0 | 0 |
| Mycobacterium smegmatis IPP 73262 | 26,5 .106 | E | E | 0 | 0 | 0 |
Concentration efficace à 1,5%.
Avantages des produits iodés
Inconvénients des produits iodés