在日益变化的当今世界上,总体而言,食品安全和粮食安全依然是人类的基本需求。在过去的几年中,确保食品安全始终是国际和国家行动的主要重点之一。微生物和化学有害物均令人关注。在化学有害物中,真菌毒素(真菌有毒代谢物)对食品和饲料的污染,藻类毒素(藻类产生的毒素)对水产品的污染以及植物毒素对可食用植物的污染,近来均被世界卫生组织列为食源性疾病的重要根源(世卫组织,2002年a)。在这三大类的自然毒素中,迄今为止最引人注重的还是真菌毒素。在世界许多地方,目前真菌毒素已经构成重要的食品安全问题。
真菌毒素对人类和动物健康可产生严重的影响,这一认识导致了许多国家在近几十年来制定了诸多有关食品和饲料中真菌毒素的法规,以保护人类的健康,并保障生产者和贸易商的经济利益。制定真菌毒素法规是一项复杂的工作,包含诸多的影响因素和利益相关方。真菌毒素的第一个限量标准是二十世纪六十年代末制定的黄曲霉毒素限量标准。到2003年末,大约有100个国家已经为食品和饲料中的真菌毒素制定了各种特定的限量标准,而且该数目还在继续增加之中。
现有大量的出版物均将重点置于真菌毒素的限量标准和法规(Krogh,1977年;Schuller等人,1983年;Stoloff等人,1991年;Gilbert等人,1991年;Resnik等人,1991年;Van Egmond等人,1991年;Van Egmond和 Dekker,1995年;Boutrif和Canet,1998年;Rosner,1998年;Van Egmond,1999年)。根据1994和1995年开展的全球调查结果,粮农组织于1997年发表了有关真菌毒素最新的全面综述。自从这一食品和营养论文发表以来,又有许多真菌毒素新的限量标准和法规开始实施,还有一些正在制定之中,因此,有必要对这一出版物的资料进行更新。2002年和2003年在全世界开展了相关调查,并获得了大量的详细资料。为了编写本文件,2003年对这些资料进行了整理和分析,本文就是依据截至20003年12月31日所收到的信息和修订意见而撰写的。
有一些因素,无论是科学上还是社会经济上的,均可影响真菌毒素限量标准和法规的制定。这些因素包括:
·毒理学数据的可获得性;
·各种商品出现真菌毒素的数据的可获得性;
·对每批次商品中真菌毒素含量的了解程度;
·可用的分析方法;
·贸易伙伴国家现有的法规;
·提供足够的粮食需求。
头两个因素分别为风险评估的主要内容,即危害评估和暴露评估提供了必要的信息。风险评估是科学地评估人类因接触食源性危害物而对健康产生已知和潜在的不利影响的可能性,是制定法规的重要科学基础。
法规的制定主要以已知毒性作用为依据。目前,最重要的真菌毒素有:黄曲霉毒素、赭曲霉素 A、棒曲霉素、伏马菌素、玉米赤霉烯酮和一些单端孢霉烯族,如脱氧雪腐镰刀菌烯醇。粮农组织和世界卫生组织科学咨询机构的食品添加剂联合专家委员会最近对这些毒素的危害进行了评估。食品添加剂联合专家委员会为食品添加剂、兽药残留和污染物的毒性评估提供了评估机制。污染物的安全性评估包括健康风险正常评估方法中的各种步骤。
在提交给食品添加剂联合专家委员会评估的信息中,往往包括污染物对健康可能产生不利影响的定性说明(有害物定性)。同样,有害作用特性的定性和定量评估结果也包括在提交的整套资料之中。食品添加剂联合专家委员会对毒理学资料开展的评估结果,通常会制定出“暂定每周耐受摄入量”(PTWI)或“暂定每日耐受摄入量”(PTDI)。
“暂定”一词的使用,意味着评估结果具有不确定性,因为人类摄入量水平的数据十分有限,而这些数据所产生的结果却是食品添加剂联合专家委员会所关注的。通常,该评估是以毒理学研究中所确定的“无可见不良作用剂量水平”为依据,并采用了不确定系数。不确定系数是指将动物研究中所得出的最低“无可见不良作用剂量水平”除以100,其中先除以10是为了将动物的研究结果外推到人类上,再除以10是针对个体之间的差异,从而获得可接受的摄入量。在数据量不足的情况下,食品添加剂联合专家委员会则采用较高的安全系数。
这种危害评估方法并不适用于毒素,其中关键的致癌性问题是主要原因,例如黄曲霉毒素的情况就是如此。假定无法为具有遗传毒性的化合物确定无作用浓度限量,那么任一小剂量均可能产生相应的诱发作用。如果具有遗传毒性的真菌毒素不是天然污染物,而且如不禁止此类被污染的食品或饲料,将绝不可能完全消除这种污染物,那么强行实施不得含有任何此类毒素的规定将是正确的。在这些情况下,食品添加剂联合专家委员会将不制定暂定每周耐受摄入量或暂定每日耐受摄入量。取而代之的是,建议尽力降低食品中的污染物含量,直至“可以合理达到最低水平”(ALARA)。“可以合理达到最低水平”可以视为是一污染物不能再降低的含量水平,其定义为:除非将连同食品一起扔掉或者严重地破坏重要食品的可食用性,再也无法从一食品中去除的某物质含量。这包括食品添加剂联合专家委员会在1987年和1997年对黄曲霉毒素开展的评估结果。在二十世纪九十年代期间,食品添加剂联合专家委员会还对其他真菌毒素进行了数次的风险评估,这些毒素包括:赭曲霉素A、棒曲霉素和玉米赤霉烯酮。
2001年2月,食品添加剂联合专家委员会专门就真菌毒素召开了一个特别会议(粮农组织,2001年,世卫组织,2002年b)。在此次食品添加剂联合专家委员会第56届会议上,所评估或重新评估的真菌毒素包括伏马毒素B1、B2和B3,赭曲霉素A,脱氧雪腐镰刀菌烯醇,T2和HT-2毒素,以及黄曲霉毒素M1。该会议报告涉及了每一真菌毒素的若干问题,其中包括真菌毒素的解释、通过排泄物的吸收、毒理学研究和最后评估结果。在开展真菌毒素评估的同时,该委员会提出了有关分析方法、取样方法以及相关的摄取问题和控制的总体考虑意见。
对黄曲霉毒素M1的评估更引人关注,该评估是食品添加剂联合专家委员会应食品添加剂和污染物食典规范委员会(CCFAC,还可见第3.5.5.部分)第32届会议(食品法典委员会,2000年)提出的要求,即“检查黄曲霉毒素M1的暴露情况并开展定量的风险分析”,以便比较牛奶污染的两个标准应用情况(目前在欧洲联盟和美国分别采用的限量标准,即0.05微克/千克和0.5微克/千克)。仔细分析结果表明,假定在最坏的情况下,因食用拟定最大限量的黄曲霉毒素M1即0.05微克/千克和0.5微克/千克而导致肝癌的预计风险极小,而食用限量从0.5微克/千克减少至0.05微克/千克时,对健康的益处并不显著。
为了国家一级和国际上(食品法典)应用,将进一步制定食品中黄曲霉毒素M1每日耐受摄入量。在此过程中,除了有害物评估之外,还将受到诸多因素的影响。随后将对这些因素展开讨论。
除了有关毒性的信息外,暴露评估是风险评估的另一个重要内容。为了开展暴露评估,需要有关各种商品上出现黄曲霉毒素的可靠数据以及食品摄取的数据。可能摄取黄曲霉毒素的定量评估相当困难。食品添加剂联合专家委员会在其第56届会议上强调了采用有效分析方法的重要性和采用分析质量保证方法的必要性(还可见有关分析方法的第2.4部分),以确保调查结果能够有益于进行可靠的摄取情况评估(世卫组织,2003b)。
在食品添加剂联合专家委员会对黄曲霉毒素开展的多数审议之中,来自发达国家的污染水平分析数据往往是不完整的,发展中国家根本就没有这些数据。由于大多数黄曲霉毒素的污染是不相同的,所以在收集污染水平信息时,取样是另一个十分重要的问题。
在欧洲委员会的资助下,欧洲联盟在有关食品问题科技合作(SCOOP)项目中努力开展暴露评估,有关食品问题科技合作(SCOOP)项目是为了最准确地评估欧洲联盟居民摄取若干种黄曲霉毒素的数量(欧洲委员会,1997年)。随后发表的有关食品问题科技合作报告涉及到若干其他的黄曲霉毒素,其中包括:赭曲霉素A(Miraglia和Brera,2002年)、棒曲霉素(Majerus和Kapp,2002年)以及若干镰刀菌属的毒素,如单端孢霉烯族、伏马菌素、玉米赤霉烯酮(Gareis等人,2003年)。有关食品问题科技合作的数据一直被欧洲食品安全局所采用,主要用于评估特定黄曲霉毒素对膳食污染而构成的公众健康风险情况,并对此提出咨询意见。
在制定监管取样标准的过程中,产品中黄曲霉毒素的浓度分布情况是应当予以考虑的重要因素之一。例如以花生中的黄曲霉毒素为例,其分布情况的个体差异甚大。在同一批次的产品中,花生仁被污染的数目通常是非常低,但是在一个花生仁内其污染物的含量可能会很高。如果不注重取样的代表性,那么受检批次产品的黄曲霉毒素的浓度很容易出现错误估计值。还有,在花生消费中,可能会偶然出现个别很高的黄曲霉毒素剂量,而不会出现相对低剂量的长期摄取的病例。
开心果和无花果也有类似的情况。在为黄曲霉毒素分布个体差异甚大的产品制定取样标准时,必须同时考虑消费者和生产者的风险。数年来,国际上一直很关注取样程序的设计(粮农组织,1993年;食典委,2000年)。粮农组织和食品法典委员会正在组织若干工作小组和各种讨论会,旨在寻求一种全球协调一致的方法。
有关黄曲霉毒素的官方取样方法的例子,包括美国在花生和玉米上(食品和药物管理局,2002年)和欧洲联盟在花生上(欧洲委员会,2002b)采用的黄曲霉毒素取样法。在美国,美国农业部规定:在每份为22千克的三份实验室样品中,所有黄曲霉毒素的平均含量小于1.5微克/千克为可接受水平。在欧洲联盟,用于进一步加工的花生原料必须采取一份30千克的实验室样品,其黄曲霉毒素含量不得超过15微克/千克;可直接售给消费者食用的花生成品,测试三份10千克实验室样品,所有黄曲霉毒素含量不得超过4微克/千克(黄曲霉毒素B1为2微克/千克)。
尽管途径不尽相同,美国花生产业近来在美国农业部的协助下,与一些从美国进口花生的欧洲联盟重要国家制定了“原产地认证计划”(OCR)。通过谅解备忘录,这些重要的市场已经同意,认可美国在其花生进口到这些市场之前对花生黄曲霉毒素的取样及检验结果(Trucksess等人,2003年)。那些证明批次鉴定和黄曲霉毒素检验结果没有问题的证书文件,可以用于证明这些花生是符合欧洲联盟黄曲霉毒素法规的。在原产地认证计划中,美国出口商采用22千克的首个样本测试结果来鉴别批次产品。美国农业部第二份22千克的样本是依据欧洲联盟的批次产品鉴定协议进行测定的。
原产地认证计划将减少在进口港被拒收的产品批次数,减少进口商产品供应的中断,减少出口商和进口商的经济损失,维护欧洲联盟确保消费者安全的标准。原产地认证计划是两个国家之间通过签署协议,在维护消费者安全的高标准过程中互为受益的例子之一(Adams和Whitaker,2004年)。
食品法规提倡控制方法。为了使法规能够得以实施,必须具有可靠的分析方法。如果容许含量没有可实现的合理预期值,不仅浪费了其所使用的资源,而且可能浪费那些完全适于消费的产品(Smith等人,1994年)。分析方法除了可靠性之外,还应简单易行,因为这将影响所要产生的数据量,而且还会影响到最终采取措施的实用性。通过采用符合特定实施标准的方法(这种标准可以通过多个实验室的研究予以验证),可以提高分析数据的可靠性。
官方分析化学家协会(国际官方分析化学家协会)、欧洲标准化委员会以及欧洲类似于国际标准化组织的机构,具有很多分析真菌毒素的标准方法,这些方法均已经过多个实验室的方法验证研究得以确认。国际官方分析化学家协会的《官方分析方法》最新版本(Horwitz,2000年)包括了约40个测定真菌毒素的有效方法,最近还发表了一篇有关真菌毒素有效分析方法的评论文章(Gilbert和Anklam,2002年)。
欧洲标准化委员会还制定了一份文件,为各种真菌毒素的分析方法提供了特定标准,这些方法可用于官方的测定(欧洲标准化委员会,1999年)。该文件还包括有关方法性能的信息,估计这些信息均是来自富有经验的分析实验室。欧洲标准化委员会的标准反映了目前欧洲联盟在黄曲霉毒素、赭曲霉素A和棒曲霉素的正式法规中对方法性能的要求(欧洲委员会,1998年;2003a;2003a)。预计欧洲联盟未来的法规还将出现食品和饲料的其他真菌毒素分析方法的规定。
除了采用业已证实是有效的方法之外,建议还应利用分析质量保证程序,其中包括采用(经核验的)标准物质,特别是在需要高度的比对和准确度的情况下。为了控制食品中的真菌毒素,今后可能会日趋出现发展分析质量保证体系并使用标准物质的局面。在由欧洲委员会标准、测量和测定计划(原先称之为欧共体标准局)资助的一些项目中,已经开发了或目前正在进行重新开发一些真菌毒素(经核验的)标准物质(Josephs等人,2004年)。表1(附录中)列出了欧共体标准局二十世纪八十年代以来开发的(经核验的)真菌毒素标准物质的概况。通过欧洲委员会标准物质与测量研究所/联合研究中心(JRC/IRMM),目前在全世界均可获得真菌毒素的标准物质[1]。
经核验的标准物质相对昂贵,因为在开发过程投入了大量的时间和巨额资金,而且目前的供应量十分有限。因此,建议各实验室应开发自己的标准物质供日常所用,而其中的毒物含量应根据经核验的物质予以确定。
除了使用(经核验的)标准物质之外,定期参加实验室间比对,例如实验室能力验证计划,变得日趋重要,这是实验室为了证实其合格的能力必须采取的分析质量保证措施的组成部分。对于真菌毒素而言,目前国际上许多实验室都有能力验证计划,其中包括:i) 由食品分析能力评估计划(FAPASÒ)组织、由大不列颠和北爱尔兰联合王国核心科学试验室实施的验证计划(Richard等人,2003年);ii) 由美国石油化学家学会组织、由美国实施的验证计划(美国石油化学家学会,2003年)。
良好的分析方法和分析质量保证,是全面执行食品法规的必要前提条件。特别是在自由贸易地区,执法机构在测量不确定性情况下处理问题的方法也十分重要。在欧洲联盟和欧洲自由贸易区内,各国所用的方法尚未协调一致,这可能会导致不同水平的行动,例如黄曲霉毒素。因此,食品法规执法者(FLEP)的“真菌毒素”工作团体建议采取统一的方法(Jeuring,2004年)。十分有趣地注意到,欧洲联盟有关食品中棒曲霉素的新指令于2003年11月生效,其中就如何处理测量不准确的问题提供了指示(欧洲联盟指令,003a)。迄今为止,这一指示确实有特色,但是期望近期内能就测量一致性问题制定更多的法规文件。
在具有贸易联系的国家之间,最好能有效地促使法规协调一致。事实上,在澳大利亚和新西兰地区、欧洲联盟以及南方共同市场中已经采用了这种方法,这些地区目前已经具有若干统一的真菌毒素法规。严格的监管行动可能导致进口国家禁止或限制某些商品的进口,例如特定的谷物,这可能给出口国家在寻求或维持其产品市场方面带来诸多困难。例如,欧洲联盟(欧共体委员会,1991年)针对动物饲料中黄曲霉毒素制定的严格法规,导致欧洲联盟的动物饲料制造商将饲料中的花生粉换成其他的蛋白质来源,这将对某些发展中国家的花生粉出口产生严重的影响(Bhat,1999年)。
进口国家法规对市场造成的影响,可能会导致受污染的食品和饲料出口量减少,并使得这些次等的食品和饲料进入当地市场。有些国家根据销售地的不同,对特定产品的黄曲霉毒素采用不同的限量标准。
世界银行已经公开发表了有关国际食品安全标准及标准一致性对全球食品贸易模式的影响的研究结果(Wilson和Otsuki,2001年)。在若干个假定的情况下,该研究评估了15个进口国家(包括4个发展中国家)的黄曲霉毒素监管标准对31个国家(包括21个发展中国家)的出口影响。在其中的一个假定情况下,作者研究了所有国家在采用国际标准即食品中黄曲霉毒素B1限量为9微克/千克(相当于食典准则的限量即黄曲霉毒素总量为15微克/千克)情况下的贸易流量。与所有进口国家均保持1998年制定的限量标准(普遍较低)相比,前者使得这些国家的谷物和坚果的贸易量增加了61亿美元(即上升51%)。
在合理的价格下,监管体系将不会危及某些基本商品的可供应量。特别是在食品供应已经有限的发展中国家中,严厉的法律措施可能导致食品的缺乏和价格上涨。例如,在撰写本文时,非洲部分地区在严峻的粮食安全状况下,采取了保证充足的粮食供应优先于食品安全之上的措施。真菌毒素是十分重要的问题,人类真菌毒素中毒的偶然爆发、黄曲霉毒素在非洲西部肝癌上的作用以及伏马菌素在非洲南部食道癌的作用均证实了这一点(Shephard,2004年)。
权衡各种因素在科学、粮食安全及法规各层面上的作用是非常重要的活动,常识问题是实现这一决定的重要因素。负责公共健康的官员面临着一个十分复杂的问题:应当尽可能地从食品中去除真菌毒素,尤其是致癌的真菌毒素。但是,由于食品中存在的物质是天然污染物,人类不可能彻底地免除该物质的危害,人们不得不容忍少量真菌毒素的危害。尽管面临这种困难的选择,但在过去的数十年中,许多国家已经制定了一些真菌毒素法规,而且新的法规仍然在不断地起草之中。
2002年,国家公共卫生和环境研究所发起了一个有关真菌毒素的国际调查。作为该调查的组成部分,要求荷兰驻世界各国大使馆农业处尽可能多地从各国当地主管部门收集有关真菌毒素法规情况的最新信息[2]。在那些按照此程序无法获得所期望信息的国家中,则采用个人调查的方法。
调查中特别关注的问题包括:
·现有的真菌毒素法规情况;
·已经生效或正在拟定的法规所涉及的真菌毒素类型、产品以及最大容许含量;
·负责监管真菌毒素的主管部门;
·官方和公开发表的取样及分析方法的应用情况。
截至2003年年底,已从89个国家获得了资料。加上以往调查所收集的信息,共获得了119个国家具有或不具有食品和饲料真菌毒素特定的限量标准及法规的详细信息。对已获得的所有信息均进行了检查和翻译。只要是必要且可行的,就向信息提供者提出需要澄清的问题。本文认真审核了在2003年12月31日前收到的纠正信息。表2(附录2)展示了每个国家最新信息的概况,包括国家代码和人口密度。对所获得的所有资料均按国家和经济共同体(澳大利亚/新西兰、欧洲联盟、南方共同市场)进行了分类。此外,这些信息还包括由食品法典委员会制定的有关标准。对于每一信息来源,均将所获得的资料分成以下各类:食品、奶类和饲料,然后按国家的首字母顺序列表(见附录2表3)。
根据整个世界的资料,2003年至少有99个国家在食品和(或)饲料上拥有真菌毒素的法规1(见图1),与1995年相比大约增加了30%。这些国家的总人口约占全世界人口的87%。图2展示了1995年和2003年具有真菌毒素法规的特定区域人口占世界人口的比例。1995年世界上23%的人口生活所在地尚无有效的真菌毒素法规。2003年该百分比下降至13%,这是因为拉丁美洲和欧洲的覆盖比例略有上升,非洲和亚洲/大洋洲的覆盖比例大幅度上升所致。
事实上,2003年具有真菌毒素法规的所有国家至少拥有黄曲霉毒素B1或食品和(或)饲料中曲霉毒素B1、B2,、G1和G2总量的法定限量标准,1995年也出现过这种状况。对于其他一些真菌毒素,也有一些特定的法规(例如黄曲霉毒素M1、单端孢霉烯族的脱氧雪腐镰刀菌醇、二乙酰藨草镰刀烯醇、T-2毒素和HT-2毒素;伏马菌素B1、B2和B3;松蕈酸;麦角生物碱;赭曲霉素A;棒曲霉素、拟茎点霉毒素;杂色曲霉素和玉米赤霉烯酮)。过去几年来,对真菌毒素实施监管措施的国家数目显著上升。对1995年和2003年的情况进行比较,看来2003年在更多的商品和产品上对更多真菌毒素实施了监管,但是耐受限量在总体上则保持原状或趋于下降。随着官方程序在取样和分析方法上的新要求,法规已经变得更加多样化和具体化。与此同时,在属于相同经济共同体(澳大利亚/新西兰、欧洲联盟、南方共同市场)的国家之间,一些法规已经实现了协调一致,或者正处于协调一致进程的某些阶段(见第3.5部分)。
图1:具有或尚未具有真菌毒素法规的国家[3]
图3和图4分别展示了非洲在食品和饲料上具有的各种真菌毒素的法定限量标准。已知15个国家具有特定的真菌毒素法规。这些国家的人口占整个非洲大陆人口的59%。非洲绝大多数国家(可能)尚没有专门的真菌毒素法规。事实上,没有专门的真菌毒素法定限量标准的那些国家并不意味着可以忽略这一问题。在这些国家中,有些国家承认真菌毒素给他们造成了诸多问题,并承认他们是应当制定此类法规。这是这些国家在对调查作出的反馈中提及的。
然而,非洲的真菌毒素问题,需要在当地食品安全、卫生和农业问题的整个背景之下予以讨论(Shephard,2004年)。在这些国家中,多数农民所生产的农产品是供他们自己消费(生存农业)的,所以制定真菌毒素法规在健康保护方面的效果有限,这就是多数非洲国家的情况。目前非洲现有的真菌毒素法规中,大多是针对黄曲霉毒素。摩洛哥所拥有的真菌毒素法规最为详细。
图2:真菌毒素法规所覆盖的人口占世界人口的百分比
图3:非洲有关食品真菌毒素法规情况
图4:非洲有关饲料真菌毒素法规情况
亚洲和大洋州占据了世界上非常大的面积,其绝大多数国家位于热带和亚热带地区,因此正如所料,在高温下生长的真菌导致了诸多的真菌毒素问题(Pitt和Hocking,2003年)。只有新西兰是例外,该国家具有低温气候,真菌毒素问题与亚洲和北部的澳大利亚截然不同。图5和图6分别展示了亚洲/大洋州在食品和饲料上真菌毒素法定限量标准情况。在亚洲/大洋州,已知有26个国家具有专门的真菌毒素法规(所包括的人口占该地区人口的88%)。食品上绝大多数法规主要是针对黄曲霉毒素总量,而饲料上的法规主要针对黄曲霉毒素B1含量。澳大利亚和新西兰已拥有一致的真菌毒素法规,其中包括“外来的”真菌毒素松蕈酸和拟茎点霉毒素的限量标准(可见第3.5.1.部分)。到目前为止,最为广泛也最详细的法规当属中国和伊朗伊斯兰共和国。
图5:亚洲/大洋州有关食品真菌毒素法规情况
图6:亚洲/大洋州有关饲料真菌毒素法规情况
2003年,已知欧洲有39个国家具有专门的真菌毒素法规,其所包括的人口占整个欧洲大陆人口的99%。图7和图8分别展示了欧洲在食品和饲料上各种真菌毒素法定限量标准的情况。
图7:欧洲有关食品真菌毒素法规情况
图8:欧洲有关饲料真菌毒素法规情况
与世界上其他区域相比,欧洲在食品上所拥有的真菌毒素法规最为广泛也最为详细。在欧洲联盟内部,对各种食品中的黄曲霉毒素,牛奶中的黄曲霉毒素M1,谷物和葡萄干中的赭曲霉素A,苹果汁和苹果产品中棒曲霉素,各种饲料中的黄曲霉毒素B1,均具有一致的法规。已对谷物和谷物产品中的脱氧雪腐镰刀菌烯醇制定了指导性限量标准。值得注意的是,许多新近加入欧洲联盟的成员国均具有真菌毒素法规,这些国家的法规往往要比欧洲联盟目前正在实施的法规更加详细。
拉丁美洲的主要农产品(玉米、小麦、咖啡、棉花、大豆、大麦、向日葵、花生、树坚果、可可豆和乳产品)极易遭受真菌污染物和真菌毒素衍生物的污染(Pineiro,2004年)。图9和图10分别展示了拉丁美洲在食品和饲料上各种真菌毒素法定限量标准的情况。现已知有19个国家具有专门的真菌毒素法规,其所覆盖的人口占该区域人口的91%。在南方共同市场内部,拥有一致的黄曲霉毒素法规(Mercado Comun del Sur),南方共同市场是由阿根廷、巴西、巴拉圭和乌拉圭组成的贸易集团(还可见第3.5.3部分)。顺便提及,其他一些国家也表示他们愿遵守南方共同市场的法规。食品中的黄曲霉毒素法规通常是针对黄曲霉毒素B1,B2,G1和G2的总量而确定的。乌拉圭拥有最为详细的法规,其中包括饲料中麦角生物碱的限量标准,这也是世界上真菌毒素法规中相当少见的一个标准。
图9:拉丁美洲有关食品真菌毒素法规情况
图10:拉丁美洲有关饲料真菌毒素法规情况
多年来,美国和加拿大就已经具有真菌毒素法规,并在取样和分析中采用了先进的技术。在这两个国家中,黄曲霉毒素的限量标准是按照黄曲霉毒素B1,B2,G1和G2的总含量计算的。图11和图12分别展示了北美洲在食品和饲料上各种真菌毒素的法定限量或指导性限量标准的情况。
图11:北美洲有关食品真菌毒素法规情况
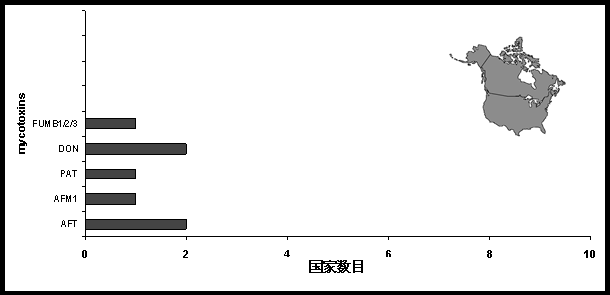
除了镰刀菌属毒素的限量标准外,加拿大还制定了小麦(包括硬粒和软粒小麦)和其他谷物中受镰刀菌侵染籽粒百分比的容许量。加拿大谷物委员会(CGC)已经发布了“官方谷物分级指南”,其中包括谷物检验标准程序[4]。加拿大还为各种作物制定了麦角碱百分比含量的限定标准。美国还具有各种玉米产品中伏马菌素B1,B2和B3总含量的限量标准。这是现有国家中唯一对这三种伏马菌素总含量制定了限量标准的国家。
图12:北美洲有关饲料真菌毒素法规情况
近年来,拥有黄曲霉毒素法规的国家数目显著增加。黄曲霉毒素法规往往非常详细,并是针对各种食品、奶制品和饲料而专门制定的。表4(附录2)尽力比较了1995年和2003年之间在食品、动物饲料(用于饲喂奶牛)上所制定的黄曲霉毒素法定限量标准的国家数目、限量的中值、范围的不同,以便确定其发展趋势。这种比较并非易事,需要根据未来情况进行调整,因为采用的所有数据并不非准确无误。另一个制约因素是有些国家针对各种食品和饲料专门制定了不同的容许含量,而有的国家仅制定了一种容许含量,例如针对“所有的食品”或“所有的饲料”制定一个容许含量。因此,只好进行简化处理。
在食品上,把针对黄曲霉毒素B1和黄曲霉毒素总含量制定的限量标准汇总成“所有食品”类,或者如果在法规中并未提及这一类别,当可以把这些食品的限量标准视为最为接近这一类别。同样,为了对黄曲霉毒素M1限量标准进行比较,将在乳类上制定的法规汇总成一类(尽管许多国家对诸如奶粉、奶酪及婴儿食品的乳产品分别制定了专门的限量标准)。最后,至于动物饲料中的黄曲霉毒素,有些国家往往针对具体的饲料制定了许多限量标准。为了在国家之间对饲料中黄曲霉毒素B1和黄曲霉毒素总含量的限量标准分别进行比较,将那些已知或预计与奶牛饲料有关的限量标准归为一类。就人类健康而言,这些标准往往至关重要,因为黄曲霉毒素B1的残留物进入牛奶和奶产品后会产生黄曲霉毒素M1。
在表4中,对这五大类别的一些特征进行了概述,图13、14、16、17和18展示了2003年限量标准的频率分布情况。对表4和这些插图的分析得出了以下结论:
图13:世界各国对食品中黄曲霉毒素B1的限量情况
3.4.1.1 食品中的黄曲霉毒素B1
与1995年的情况相比,2003年食品中黄曲霉毒素B1的最大容许含量并未出现显著的变化,尽管限量的幅度略为变小(1-20微克/千克),而且至少有29个国家目前均采用2微克/千克的限量标准(见图13)。这些国家绝大多数属于欧洲联盟(自1998年以来,欧洲联盟对各种产品中的黄曲霉毒素B1含量和黄曲霉毒素B1,B2,G1和G2的总含量均采用了一致的限量标准)、欧洲自由贸易联盟成员国及欧洲联盟的候选国。截至2003年止,许多欧洲联盟候选国已经使其国家法规与欧洲联盟保持一致,以便获得其成员国资格(2004年5月1日)。另一个呈明显多数的限量是5微克/千克,有21个国家采用了这一标准,这些国家主要分布在非洲、亚洲/大洋洲、拉丁美洲和欧洲。美国和加拿大对黄曲霉毒素B1没有单一的限量标准。
3.4.1.2 食品中黄曲霉毒素的总量
与1995年一样,2003年许多国家通过黄曲霉毒素B1、B2、G1和G2总量的限量标准对黄曲霉毒素进行了控制,有时也结合黄曲霉毒素B1的特定限量标准进行控制。与1995年相比,限量的变化幅度(0-35微克/千克)略有减小,而限量的中值(10微克/千克)略有上升。采用最多的限量(见图14)是4微克/千克(有29个国家采用),这也是欧洲联盟、欧洲自由贸易联盟成员国及欧洲联盟候选国一致采用的限量标准。在这些国家中强制实施了黄曲霉毒素B1和黄曲霉毒素总量的两个限量标准。另一个较多国家采用的限量是20微克/千克,共有17个国家采用,其中拉丁美洲国家占一半(因为这也是南方共同市场的统一限量标准),有些是非洲国家。此外,美国是第一个制定黄曲霉毒素限值的国家,也采用20微克/千克的限量。近年来,对食品中黄曲霉毒素总量实施限量的做法依然十分“流行”,2003年共有76个国家采用这种法定限量(与之相比,有61个国家采用黄曲霉毒素B1的特定限量标准)。
图14:世界各国对食品中黄曲霉毒素总量的限量情况
黄曲霉毒素总量限值标准需要开展的分析工作要多于黄曲霉毒素B1单个标准。与单一的黄曲霉毒素B1法定限量相比,这种总量限值标准是否能明显有助于更好地保护公众健康还是有争议的。无论从毒理学还是从发生频率而言,黄曲霉毒素B1是黄曲霉毒素中最为重要的毒素。商品中含有黄曲霉毒素B2、G1和G2,而不含黄曲霉毒素B1是极不可能的(Yabe和Nakajima,2004年),而且黄曲霉毒素B2、G1和G2的总含量通常均小于黄曲霉毒素B1的单一含量。
黄曲霉毒素B1和B2(主要是由黄曲霉产生的)典型的发生比率平均为4:1左右。黄曲霉毒素B1和黄曲霉毒素B2、G1和G2(G毒素主要是由寄生曲霉产生)总量的发生比率平均为1:0.8左右,尽管这两个比率确实处于动态变化之中(Van Egmond等人,1978年)。在采用黄曲霉毒素总量法定限值标准的国家中,监管当局应严格地检查监督机构的分析数据,以便经常地了解黄曲霉毒素总量(超过黄曲霉毒素B1含量)数据的获得情况,这对于充分地保护消费者的健康至关重要。对单一对象(黄曲霉毒素B1)含量的分析似乎是高效和足够的,而且更加易于操作。
图15表示了1995年和2003年世界各个区域食品中黄曲霉毒素总量限值的变化幅度和中值。从图中可见,非洲、拉丁美洲和北美洲没有出现显著的变化,相反,在亚洲/大洋洲和欧洲,总量的限值明显出现下降趋势。
图15:世界各区域食品中黄曲霉毒素总量限值的变化幅度和中值
3.4.1.3 乳品中的黄曲霉毒素M1
截至2004年年底,已有60个国家制定了黄曲霉毒素M1的法规,比1995年增加了三倍多。在表16中,采用0.05微克/千克的国家数目最多,其中绝大部分国家仍然是欧洲联盟、欧洲自由贸易联盟的成员国和欧洲联盟候选国,但非洲、亚洲和拉丁美洲的部分国家也采用这一限量。另一个较多国家采用的限量为0.5微克/千克。这一较高的法定限量为美国、若干亚洲和欧洲国家所采用,其中采用最多的是拉丁美洲国家,因为该限量被确定为南非共同市场的统一标准。
两个最主要的黄曲霉毒素M1限量之间相差10倍,而且已经共存许多年,这导致在食典委员会内部引发了一场争论,并使他们要求食品添加剂联合专家委员重新评估黄曲霉毒素M1对人类健康的风险(见危害评估部分)。除了这些亚微克/千克的法定限量外,在2002/2003年间的调查过程中有些国家指出他们将牛奶中的黄曲霉毒素M1限量控制在5微克/千克和15微克/千克之间。这些含量看来是不现实的,然而却不可能确定其是否属于在填写调查表过程中产生的错误。
图16:世界各国对牛奶中黄曲霉毒素M1的限量情况
3.4.1.4 饲料中的黄曲霉毒素B1
在饲料上,现已经具有许多的黄曲霉毒素法规。表17概述了那些适用于奶牛饲料的法规情况。尽管2003年用于控制饲料中黄曲霉毒素B1的法规远远多于1995年的法规数目(1995年为25个而2003年达到39个),但对天然产生的黄曲霉毒素总量实施控制的国家数目仅略有增加(1995年为17个,2003年为21个)。黄曲霉毒素M1是黄曲霉毒素B1的代谢物并导致了健康问题,从这一观点出发,上述结果就不难理解且符合逻辑。因此,限制饲料中黄曲霉毒素B1的含量是控制牛奶中黄曲霉毒素M1的最有效的方法。图17展示了0.5微克/千克的限量在黄曲霉毒素B1法规分布模式中的优势地位。这一限量标准不仅为欧洲联盟和欧洲自由贸易联盟的成员国所采用,而且也被许多欧洲联盟候选国所遵循,在欧洲联盟国家之外只有个别国家采用这一限量。通常,对奶牛饲料严格地实施这一限量标准将能把牛奶中的黄曲霉毒素M1含量有效地控制在0.05微克/千克以下(在这些国家中,业已制定了牛奶中黄曲霉毒素M1的相应限量标准)。
图17:世界各国对奶牛饲料中黄曲霉毒素B1的限量情况
3.4.1.5 饲料中黄曲霉毒素的总含量
限制饲料中黄曲霉毒素总量的法规数目远远少于现有的黄曲霉毒素B1单一限量法规。这些总量限值各不相同,这取决于不同的饲料对象。图18反映了动物饲料中黄曲霉毒素总量限值的分布情况,这些饲料(也)是用于喂养奶牛的。
图18:世界各国对奶牛饲料中黄曲霉毒素总量的限值情况
限值标准的整个分布情况较为均匀,其中使用国家最多的限值是20微克/千克。进一步分析揭示了在全世界饲料法规中黄曲霉毒素B1、B2、G1和G2总量法定限值的分布情况,尤其是在美洲的情况。
目前,除了黄曲霉毒素以外的真菌毒素限量标准主要是针对食品,极少涉及动物饲料。除了黄曲霉毒素以外,预计其他真菌毒素限量标准的数目在不久的将来将显著增加,不仅是在食品上也包括在饲料上。随后第3.4.2.1至3.4.2.5部分中的讨论将主要限定在食品上。
3.4.2.1 棒曲霉素
自1995年以来,越来越多的国家对棒曲霉素含量予以控制,其主要是针对水果产品,例如苹果汁。许多国家针对食品中棒曲霉素的含量制定了法规或准则,其中绝大多数的国家均设立了相同的限量(50微克/千克),正如图19所示。欧洲联盟对棒曲霉素的统一限量标准近来已经开始在各种产品上生效(欧洲委员会,2003a)。这使得棒曲霉素成为世界上受到最严格控制的真菌毒素之一。
图19:世界各国对水果和果汁中的棒曲霉素的限量情况
经核准的分析方法(官方分析化学家协会,欧洲标准化委员会)可容易地用于测定果汁中50微克/千克的棒曲霉素含量。但是,欧洲联盟在限制性条款中已经为婴儿食品和婴儿配方乳粉制定了10微克/千克的新限量标准,适宜的分析方法也将及时出台。这促使位于比利时黑尔的欧洲联盟标准物质与测量研究所/联合研究中心在研究上付出了极大的努力,并已成功地完成了旨在证明新开发方法适用性的协作研究。
3.4.2.2 赭曲霉素A
赭曲霉素A的法规制定情况与棒曲霉素的情况极为相似,这是一目了然的。在食品上采用限量标准的国家数目显著上升,完全同意对谷物和谷物产品采用适宜限量标准的国家数目也明显增加(见图20)。谷物被视为是人类遭受赭曲霉素A危害的主要根源。但是所提供的数据十分有限。许多国家已经对谷物中赭曲霉素A含量制定了限量标准,也有许多国家对谷物产品也制定了限量标准,不同的国家为谷物和谷物产品制定了各自(不同)的限量标准。例如在谷物产品上,欧洲联盟内部就出现了这种情况,其中5微克/千克的限量标准(在图中占主导位置的限量)适用于谷物原粮,3微克/千克的限量(在图20中没有列出)则适用于谷物加工产品。将此类情况全部反映在图中是非常困难的,因此采取一个国家择优选择一个谷物(原粮)限量列于图20之中,如果没有此类限量则选择一个谷物产品的限量(如果有的话)列入图中。在欧洲联盟资助的在研项目-“为改进风险评估提供依据的赭曲霉素A诱发致癌机理研究”[5]得出结果之前,必须在不久的将来对赭曲霉素A现有的和已提出的限量标准进行审核。该项目旨在通过临界值或非临界值方法来确定赭曲霉素A是否致癌的问题。
图20:世界各国对谷物及谷物产品中赭曲霉素A的限量情况
3.4.2.3 脱氧雪腐镰刀菌烯醇
与棒曲霉素和赭曲霉素A的情况一样,许多国家已对食物中的脱氧雪腐镰刀菌烯醇制定了法规性或指导性的限量标准(见图21)。尽管在1995年对食品中这种单端孢霉烯毒素仅是偶尔地加以控制,但是在二十世纪九十年代末发现在谷物及谷物产品上该毒素含量每千克均为毫克数量级(欧洲尤为严重),自那时起,该毒素就成为监督计划和监管当局高度重视的问题。与赭曲霉素A的情况相似,在一幅图表中是难以全面地概述小麦和其他谷物中脱氧雪腐镰刀菌烯醇的最通用限量标准,至于现行的有关脱氧雪腐镰刀菌烯醇法规的详细情况,有兴趣者可以参见表3。采用750微克/千克的限量标准的国家数目占优势地位,该限量为欧洲联盟国家广为采用,这些国家多年来一直采用这一(非官方的)指导性限量,对作为加工原料的面粉中的脱氧雪腐镰刀菌烯醇含量进行控制。
图21:世界各国对小麦(面粉)和其他谷物中脱氧雪腐镰刀菌烯醇的限量情况
近来的资料表明,亚洲一些国家经常出现产生雪腐镰刀菌烯醇(是与脱氧雪腐镰刀菌烯醇有关的单端孢霉烯族毒素)的真菌,有时出现的频率还高于产生脱氧雪腐镰刀菌烯醇的菌系,例如在日本(Tanaka等人,2004年)和韩国(Lee等人,2004年)出现的情况。但是,近年来在英格兰的南部和西部地区经常发现产生雪腐镰刀菌烯醇的真菌(Jennings等人,2004年)。有关雪腐镰刀菌烯醇的法规至今尚未制定,但是鉴于雪腐镰刀菌烯醇的毒性相对高于脱氧雪腐镰刀菌烯醇(欧洲委员会,2002c),从长远的观点而言,应当对雪腐镰刀菌烯醇予以高度的重视。
3.4.2.4 玉米赤霉烯酮
目前,已有16个国家对食物中的玉米赤霉烯酮(含雌激素的真菌毒素)含量进行了控制(见图22),与之相比,1995年仅有6个国家。玉米赤霉烯酮在结构上与a-zearalanol(玉米赤霉醇)有关,是欧洲联盟1988年禁用的合成类生长促进剂。玉米赤霉烯酮经家畜产生代谢变化,并产生各种各样的化学物质,包括玉米赤霉醇。通过对动物饲料中玉米赤霉烯酮含量的控制,就可控制可食用组织中出现天然玉米赤霉醇的问题。目前对玉米和其他谷物中的玉米赤霉烯酮的限量各不相同,变化幅度从50至1000微克/千克。从图22可看出,目前制定的限量要远远高于以前限量的趋势。
图22:世界各国对玉米和其他谷物中的玉米赤霉烯酮的限量情况
图23:世界各国对玉米中伏马菌素的限量情况
3.4.2.5 伏马菌素
伏马菌素是在二十世纪八十年代后期被发现的。虽然在1995年只有一个国家采用法规对伏马菌素进行控制,但是这一数目已经上升至6个国家,这些国家对玉米中伏马菌素的限量幅度从1000至3000微克/千克(见图23)。尽管从比例上呈显著上升,但限制伏马菌素含量的国家数目依然太少,以致无法就普遍接受的限量标准得出有意义的结论。监管当局目前正在讨论有关伏马菌素法规性限量的制定问题,这些当局应认真考虑他们是否仅对伏马菌素B1的制定限量,或者对所有的天然伏马菌素制定总限量。伏马菌素的情况与黄曲霉毒素一样,后者不仅具有黄曲霉毒素B1的限量标准也具有黄曲霉毒素总量的限量标准(见第3.4.1部分)。
3.4.2.6 其他真菌毒素
除了以上各部分提及的真菌毒素外,还对一些其他的真菌毒素采取了法规行动。这些真菌毒素包括二乙酰藨草镰刀烯醇、T-2毒素和HT-2毒素、松蕈酸、麦角生物碱、拟茎点霉毒素以及杂色曲霉素。由于针对这些真菌毒素制定法规的国家数目相对较少,在此就不对其进行深入讨论。
最近,澳大利亚和新西兰已经将其真菌毒素的法规协调一致。目前共同的限量标准已适用于花生和树坚果中的黄曲霉毒素总量和麦角碱(麦角真菌的菌核并非真正的真菌毒素而是真菌的冬季休眠体,其中含有麦角生物碱)。此外,协调一致的法规还包括羽扁豆种子及其产品中的拟茎点霉毒素的特定限量标准,以及食物中(包括蘑菇和含酒精的饮料)松蕈酸的限量标准。因此,据悉只有澳大利亚和新西兰拥有较多的这些毒素限量标准。
如上所述,自1976年以来,欧洲联盟已经统一了欧洲联盟内部各种饲料中黄曲霉毒素的限量,其中包括取样和分析的议定书。1998年欧洲联盟有关食物中真菌毒素的第一个统一法规开始生效(包括取样议定书和分析方法的标准),随后会逐步地扩展到不同食品上的各种真菌毒素。
2004年及随后年份中,预计欧洲联盟将进一步有效地扩大有关食品和饲料中真菌毒素的统一法规。食物上这些法规涉及:婴儿配方食品和断奶后配方食品中的棒曲霉素、黄曲霉毒素B1、黄曲霉毒素M1、赭曲霉素A以及脱氧雪腐镰刀菌烯醇;咖啡、葡萄酒、啤酒、葡萄汁、可可及可可产品中的一些镰刀菌产生的毒素,即单端孢霉烯类毒素(除了脱氧雪腐镰刀菌烯醇外,还包括T-2和H-2毒素);在谷物为主要原料的食物中的伏马菌素和玉米赤霉烯酮。此外,在未来的几年内还将制定一些饲料方面新的限量标准,这些限量标准主要涉及麦角生物碱、脱氧雪腐镰刀菌烯醇、玉米赤霉烯酮、赭曲霉素A(欧洲委员会,2003b)。目前,正在整理欧洲食品安全局专家小组对食品链中的污染物的相关科学意见。
南方共同市场由阿根廷、巴西、巴拉圭和乌拉圭组成。这些国家采用了共同的限量标准,这些标准适用于花生、玉米及其产品中的黄曲霉毒素总含量,以及水果和奶粉中的黄曲霉毒素M1。南方共同市场有关真菌毒素的法规还包括官方的取样和分析方法。巴西和乌拉圭还采用了一些适合于特定真菌/矩阵式组合的限量标准。
东南亚国家联盟(东盟)现有成员国包括文莱达鲁萨兰、柬埔寨、印尼、老挝人民民主共和国、马来西亚、缅甸、菲律宾、新加坡、泰国和越南。这些国家绝大多数均拥有适用于真菌毒素的专门法规(见表3)。虽然东盟(还)未明确制定统一法规,但东盟食品法典特别工作小组已经形成共同的立场,拟支持牛奶中黄曲霉毒素M1的含量不超过0.5微克/千克的限量标准。
在粮农组织和世界卫生组织的支持下,食品法典委员会旨在通过制定食品和饲料的国际标准,促进世界贸易并保护消费者的健康。目前食品法典委员会有168个成员国。在食典委内部,食品添加剂和污染物规范委员会拟定食品中添加剂和污染物的最大限量(标准),这些限量在贸易冲突中发挥了决定性作用。根据《食典委程序手册》以及食典委《食品中污染物和毒素一般标准》所明确的规则与方法,食品添加剂和污染物规范委员会在制定标准时,均应尽可能地遵循风险分析原则。
当有充足理由认为某食品污染物会导致健康和贸易问题,可要求提交有关该污染物各方面的研究论文,从而启动此程序,在全部满足标准制定的必要条件之后,随即制定最大限量的方案。这些条件是指将健康问题具体化,尤其是食品添加剂联合委员会所开展的毒理学研究和暴露评估的结果(见第2.2部分),以及获得大量有关食品中各种含量水平的可靠数据,以便根据“可以合理达到的最低水平”的原则制定其最大含量(Kloet,2002年)。
在真菌毒素领域,2003年食品添加剂和污染物规范委员会制定了以下方面的标准:未经加工的花生中黄曲霉毒素的总量、牛奶中的黄曲霉毒素M1和苹果汁中的棒曲霉素的标准。小麦、大麦、大米及其产品中赭曲霉素A的标准草案以及谷物中脱氧雪腐镰刀菌烯醇的拟议标准目前均在讨论之中。
除了制定标准(最大限量)的目标之外,食品添加剂和污染物规范委员会还决定在必要的领域上高度重视“操作规范”的制定,将栽培、贮藏和加工过程中控制真菌毒素的操作措施的原则及建议汇集在这些规范中。有关这些规范的例子包括在以下方面制定的操作规范:i)减少产奶动物的原饲料和补充饲料中黄曲霉毒素B1的含量(食品法典,1997年);ii)防止和减少苹果汁以及作为其他饮料配料的苹果汁中的棒曲霉素污染(食品法典,2003年a);iii)防止和减少谷物中真菌毒素的污染,包括附件中的赭曲霉素A、玉米赤霉烯酮、伏马菌素和单端孢霉烯类毒素(食品法典,2003年b)。
通过对1995年与2003年情况的比较,发现2003年有更多国家在更多的商品和产品上制定了更多的真菌毒素法规。实际上这一趋势在相当长的一段时间内显而易见。第一个真菌毒素的限量可能是在20世纪70年代制定的,随后制定了真菌毒素限量的国家数目逐渐上升,从1981年至少31个国家增加到1987年的56个、1995年的77个以及2003年的99个国家。如果按照这一(明显呈线性的)趋势外推,预计在2010年前大约将有120个国家将具有已知真菌毒素的法规,在此之后,这一上升趋势将可能趋于平缓。
2003年在食品上拥有真菌毒素专门法规的国家数目显著多于在饲料上拥有的专门法规。但是,在未来几年中,正在制定饲料方面的真菌毒素法规(除了黄曲霉毒素以外)的国家数目预计将显著地增加。在欧洲联盟国家中,这一发展趋势尤为明显,这些国家已经在这一方面实施了重要计划。
在官方的取样及分析方法上产生的更新要求,使得这些法规变得更加多样化和更加具体。测量不确定度的问题已经进入了法规的讨论中。这些发展情况反映了各国政府普遍重视真菌毒素在人类和动物健康上的潜在影响。与此同时,在一些自由贸易区域(欧洲联盟、欧洲自由贸易联盟、南方共同市场、澳大利亚/新西兰),正在出现容许含量趋于一致的情况,而且也正在致力于促进标准协调一致,从而有利于国际贸易中的货物流动(食品法典)。这种协调一致是个缓慢的过程,这因为有关各方的观点和利益不同所致。
尽管一致的容许含量将有益于贸易,但是从整个世界(平等的)人类健康保护的角度看,并不一定非得如此,这一点是具有争议的。真菌毒素所产生的风险取决于有害物和暴露情况。真菌毒素对于个人的危害在世界各地可能相差不大(尽管其他因素有时也会产生一些影响,例如,乙肝病毒感染就与黄曲霉毒素的危害相关)。
由于污染物含量不同以及世界各地的饮食习惯不同,暴露的情况也各不相同。Shephard(2004年)通过对伏马菌素的若干计算证实了这一点。食品添加剂联合专家委员制定了一组暂定每日最大耐受摄入量,其中伏马菌素B1、B2和B3为每日2微克/千克体重。对于膳食以玉米为主的个体而言,很容易超出这一暂定每日最大耐受摄入量,这些人玉米的消费量大约为每人每日400克。Shephard做了计算,当玉米中的伏马菌素污染水平为2000微克/千克时(该水平处于一般限量的范围内,见图9),对于体重为60公斤的成年人来说,膳食暴露量则为13微克/千克体重/每日,或者为暂定每日最大耐受摄入量的650%。在发达国家,玉米的摄入量小于10克/人/日(Shephard等人,2002年),当所食用玉米的污染水平高达12000微克/千克时,膳食暴露量仍不会超过食品添加剂联合专家委员制定的暂定每日最大耐受摄入量。
各国政府或区域社会应鼓励并资助该地区各类有益活动,从而开展可靠的真菌毒素暴露评估。例如在欧洲联盟国家中开展的有关食品问题的科技合作活动,该活动有助于对某些真菌毒素开展安全性评估(见第1.2部分:暴露评估)。经济有效而简单易行的分析方法以及分析质量保证,均是确保当事件发生时能获得有意义数据的基本要素,因此应当促进这些要素的发展。
进一步改进危害评估的工作,最好是在国际一级进行协调和资助。在先进实验室操作条件下开展的慢性毒性研究,既费时又耗资,而且没有必要局限于特定区域。这些研究应当在国际上公认的具有一流水平的中心开展,而且研究结果应当由国际专家小组予以评估,例如食品添加剂联合专家委员。在欧洲生活质量和生命资源管理计划中,正在进行的“为良好风险评估提供依据的赭曲霉素A诱发致癌机理研究”项目就是国际上共同努力的例子[6]。
针对食品和饲料中真菌毒素而制定的法规以及正在制定的法规,均是各利益方精诚合作的结果,其中包括科学界、产业界及政策制定者。只有这样,才能实现真正的健康保护。
[1]见 http://www.irmm.jrc.be
[2]在本文及所附表格中采用的“法规”一词也包括诸如“准则”的其他规定。
[3]本文的插图均是采用Corel软件公司(位于爱尔兰都柏林的Corel 有限公司)的clipart软件制作的。
[4]见 http://www.grainscanada.gc.ca/Pubs/fusarium/backgrounder/don-e.htm
[5]见
http://www.uni-wuerzburg.de/toxikologie/EU-OTA/OchratoxinA.html
[6]见 http://www.uni-wuerzburg.de/toxikologie/EU-OTA/OchratoxinA.html