
La santé animale

11 juillet 2024, 08:30 heures; Rome
Aperçu
Situation: Virus influenza aviaire hautement pathogènes (sous-types H5, H5N1, H5N2, H5N6, H5N8, H7 et H7N6) à potentiel pandémie dans les pays d’Afrique subsaharienne depuis février 2017.
Pays confirmés (H5): Afrique du Sud*.
Pays confirmés (H5N1): Afrique du Sud, Benin, Botswana, Burkina Faso*, Cameroun, Côte d’Ivoire, Réunion (France), Gabon, Gambie Ghana, Guinée, Lesotho, Mali, Mauritanie, Namibie, Niger*, Nigéria*, Sénégal, Afrique du Sud et Togo.
Pays confirmés (H5N2): Nigéria et Afrique du Sud.
Pays confirmés (H5N6): Nigéria.
Pays confirmés (H5N8): Cameroun, République démocratique du Congo, Namibie, Niger, Nigéria, Afrique du Sud, Ouganda, et Zimbabwe.
Pays confirmés (H7): Afrique du Sud.
Pays confirmés (H7N6): Afrique du Sud* et Mozambique*.
Constatations animales: 2 nouveaux évènements depuis la dernière mise à jour du 13 juin 2024.
Nombre de cas humains: 0 évènements depuis la dernière mise à jour (dernière évènement déclaré 10 novembre 2021).
* Pays ayant rapporté des cas d’IAHP durant cette vague (depuis le 1er octobre 2023)
Carte. Foyers d’IAHP officiellement déclarés (sous-types H5, H5N1, H5N2, H7 et H7N6) en Afrique subsaharienne par date de survenue (1 octobre 2023 à ce jour)
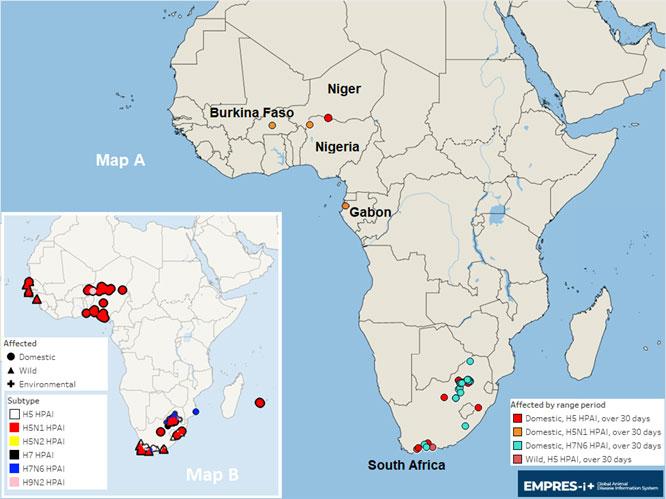
Note: Carte A présente les événements confirmés d’IAHP observés depuis le 1er octobre jusqu’au 11 juillet 2024 (vague actuelle). La carte B présente les événements confirmés d’IAHP observes du 1 octobre 2022 a 30 septembre 2023 (vague précédente).
Mise à jour de la situation
Tableau 1. Evènements d’influenza aviaire hautement pathogène déclarés chez les animaux depuis le 1 octobre 2023 (i.e. vague actuelle)
| Virus | Pays (régions administratives affectées) | Date du dernier évènement observé | Nombre d’évènements depuis la dernière mise à jour | Nombre d’évènements depuis le 1er octobre 2023 | Espèces affectées au cours des derniers évènements |
|---|---|---|---|---|---|
|
H5 |
Afrique du Sud |
20/04/2024 |
0 |
24 |
Autruches commerciales, Volailles, Manchot du Cap, Sterne Huppée |
|
H5N1 |
Nigéria |
27/02/2024 |
0 |
3 |
Volailles, Paons en captivité |
|
Burkina Faso |
26/03/2024 |
0 |
2 |
Volailles domestiques |
|
|
Niger |
13/05/2024 |
0 |
2 |
Volailles domestiques, Pintades |
|
Gabon |
03/05/2024 |
1 |
1 |
Volailles domestiques |
|
|
H7N6 |
Mozambique |
29/09/2023 |
0 |
1 |
Poules pondeuses |
|
Afrique du Sud |
18/12/2023 |
1 |
67 |
Volailles et autres oiseaux domestiques |
Pour un résumé des événements d'IAHP H5N1, H5N6 et H5N8, signalés dans les pays d'Afrique subsaharienne lors des vagues précédentes (c'est-à-dire avant le 1er octobre 2023), veuillez contacter EMPRES-Animal Health.
Publications évaluées par des pairs
Abolnik, C., Roberts, L. C., Strydom, C., Snyman, A., & Roberts, D. G. 2024. Outbreaks of H5N1 High Pathogenicity Avian Influenza in South Africa in 2023 Were Caused by Two Distinct Sub-Genotypes of Clade 2.3.4.4b Viruses. [Les épidémies de grippe aviaire hautement pathogène H5N1, en Afrique du Sud en 2023, ont été causées par deux sous-génotypes distincts des virus de clade 2.3.4.4b]. Viruses, 16(6):896. reference En 2023, l'Afrique du Sud a connu des cas sporadiques de grippe aviaire hautement pathogène (HPAI) H5N1 clade 2.3.4.4b chez les oiseaux de mer côtiers et la volaille. La surveillance environnementale a révélé la circulation de divers sous-types de grippe aviaire, le H5Nx étant le plus courant. Le séquençage du génome des cas de H5N1 HPAI a indiqué que seuls deux des quinze sous-génotypes de 2021-2022 persistaient en 2023. Le sous-génotype SA13 était limité aux oiseaux de mer côtiers, montrant des mutations accélérées de la protéine neuraminidase. Le SA15 était responsable des épidémies chez les poulets, avec des incidents distincts dans les provinces du Cap occidental et du KwaZulu-Natal, suggérant les oiseaux sauvages comme source. Les virus SA15 présentaient une troncation du gène PB1-F2 et un nouvel isoforme PA-X dans les cas du Cap occidental. Les virus H5N1 clade 2.3.4.4b sud-africains montraient moins de marqueurs de virulence par rapport aux souches européennes, ce qui pourrait expliquer l'absence de transmission aux mammifères.
Adesola, R.O., Onoja, B.A., Adamu, A.M., Agbaje, S.T., Abdulazeez, M.D., Akinsulie, O.C., Bakre, A. & Adegboye, O.A. 2024. Molecular epidemiology and genetic evolution of avian influenza H5N1 subtype in Nigeria, 2006 to 2021. [Épidémiologie moléculaire et évolution génétique du sous-type H5N1 de la grippe aviaire au Nigeria, de 2006 à 2021]. Virus Genes, 2024 Jun 19. reference En 2006, le Nigeria a connu l'un des premiers foyers du virus de la grippe aviaire hautement pathogène (GAHP) H5N1, qui s'est ensuite propagé à d'autres pays africains. En 2023, 18 pays ont signalé des foyers de H5N1 chez les volailles, avec des cas humains en Égypte, au Nigeria et à Djibouti. Les données sur l'épidémiologie moléculaire du GAHP H5N1 au Nigeria sont limitées. Nous avons examiné l'épidémiologie moléculaire et l'évolution génétique du virus de 2006 à 2021, analysant sa tendance et sa distribution géographique à travers le Nigeria. L'histoire évolutive de 61 génomes complets provenant de 13 pays a été comparée avec les séquences des épidémies nigérianes. L'analyse phylogénétique avec MEGA 11 a révélé une proximité entre les séquences nigérianes et celles d'autres pays africains. La classification des clades a identifié le clade H5N1 2.2 en 2006, avec l'apparition ultérieure des clades 2.3.2, 2.3.2.1f et 2.3.4.4b d'ici 2021. Ces résultats soulignent l'importance de la surveillance génomique pour suivre les variations antigéniques et les changements de clade, garantissant la santé des humains et des animaux.
Mercy, K., Salyer, S.J., Mankga, C., Hedberg, C., Zondo, P., Kebede, Y. 2024. Establishing an early warning event management system at Africa CDC. [Mise en place d'un système de gestion des événements d'alerte précoce au sein de CDC Afrique]. PLOS Digit Health, 3(7):e0000546. reference L'Afrique est un point chaud pour l'émergence et la réémergence des maladies, nécessitant des systèmes d'alerte précoce tels que la surveillance basée sur les événements (SBE). En 2020, les Centres africains de contrôle et de prévention des maladies (Africa CDC) ont développé un système de gestion des événements (EMS) en utilisant le logiciel libre et open-source District Health Information Software (DHIS2) pour gérer ces événements. L'EMS, créé par un processus collaboratif, a été lancé en juin 2020. D'ici décembre 2022, 416 événements ont été capturés et plus de 140 rapports hebdomadaires, dont 19 spécifiques à la COVID-19, ont été générés pour informer les efforts de réponse. La plupart des événements ont touché les humains (69%), avec des niveaux de risque modérés (50%) à élevés (29%), reflétant des éclosions de maladies émergentes et endémiques. La grippe aviaire hautement pathogène H5N1 a été l'événement animal le plus détecté, tandis que les tempêtes et les inondations étaient des événements environnementaux fréquents. La complétude et la rapidité des données se sont améliorées, ce qui a conduit quatre pays africains à adopter l'EMS en 2022 et deux de plus en 2023. Cela met en lumière comment la technologie numérique et des plateformes comme DHIS2 peuvent améliorer les flux de travail d'alerte précoce et de SBE.
Oguzie, J.U., Marushchak, L.V., Shittu, I., Lednicky, J.A., Miller, A.L., Hao, H., Nelson, M.I. & Gray, G.C. 2024. Avian Influenza A(H5N1) Virus among Dairy Cattle, Texas, USA. [Virus de la grippe aviaire A (H5N1) chez les bovins laitiers, Texas, États-Unis]. Emerging Infectious Diseases, 30(7). reference Pendant les mois de mars et avril 2024, des spécimens de bovins laitiers provenant d'une seule ferme au Texas, États-Unis, ont été étudiés à l'aide de techniques de détection de pathogènes multiples, y compris des méthodes moléculaires, des cultures cellulaires et le séquençage de nouvelle génération. L'analyse a révélé que les souches du virus de la grippe aviaire hautement pathogène A(H5N1) du clade 2.3.4.4b étaient la seule cause de cette épizootie.
Shalaby, S., Awadin, W., Manzoor, R. et al. 2024. Pathological and phylogenetic characteristics of fowl AOAV-1 and H5 isolated from naturally infected Meleagris Gallopavo. [Caractéristiques pathologiques et phylogénétiques de l'AOAV-1 et du H5 de la volaille isolés chez des Meleagris gallopavo naturellement infectés]. BMC Veterinary Research, 20:216. [reference]
Bedair, N.M., Sakr, M.A., Mourad, A., Eissa, N., Mostafa, A. & Khamiss, O. 2024. Molecular characterization of the whole genome of H9N2 avian influenza virus isolated from Egyptian poultry farms. [Caractérisation moléculaire du génome complet du virus de la grippe aviaire H9N2 isolé dans des fermes avicoles égyptiennes]. Archives of Virology, 169(5):99. [reference]
Kutkat, O., Gomaa, M., Aboulhoda, B.E., Moatasim, Y., El Taweel, A., Kamel, M.N., El Sayes, M., et al. 2024. Genetic and virological characteristics of a reassortant avian influenza A H6N1 virus isolated from wild birds at a live-bird market in Egypt. [Caractéristiques génétiques et virologiques d'un virus de la grippe aviaire A H6N1 réassortant isolé chez des oiseaux sauvages sur un marché aux oiseaux vivants en Égypte]. Archives of Virology, 169(5):95. [reference]
Olawuyi, K., Orole, O., Meseko, C., Monne, I., Shittu, I., Bianca, Z., Fusaro, A., et al. 2024. Detection of clade 2.3.4.4 highly pathogenic avian influenza H5 viruses in healthy wild birds in the Hadeji-Nguru wetland, Nigeria 2022. [Détection de virus de la grippe aviaire hautement pathogène H5 du clade 2.3.4.4 chez des oiseaux sauvages en bonne santé dans le marais de Hadeji-Nguru, au Nigéria en 2022]. Influenza Other Respiratory Viruses, 18(2):e13254. [reference]
Olawuyi, K., Orole, O., Meseko, C., Monne, I., Shittu, I., Bianca, Z., Fusaro, A., et al. 2024. The Public Health Importance and Management of Infectious Poultry Diseases in Smallholder Systems in Africa. Influenza Other Respir Viruses, 18(2):e13254. [reference]
Monjane, I. V. A., Djedje, H., Tamele, E., Nhabomba, V., Tivane, A. R., Massicame, Z. E., Arone, D. M., Pastori, A., Bortolami, A., Monne, I., Woma, T., Lamien, C. E. & Dundon, W. G. 2024. H7N6 highly pathogenic avian influenza in Mozambique, 2023. Emerging Microbes & Infections, 13, (1). [reference]
Sanogo, I.N., Guinat, C., Dellicour, S., Diakité, M.A., Niang, M., Koita, O.A., Camus, C. & Ducatez, M. 2024. Genetic insights of H9N2 avian influenza viruses circulating in Mali and phylogeographic patterns in Northern and Western Africa. Virus Evolution, 10(1):veae011. [reference]
Glazunova, A., Krasnova, E., Bespalova, T., Sevskikh, T., Lunina, D., Titov, I., Sindryakova, I. & Blokhin, A. 2024. A highly pathogenic avian influenza virus H5N1 clade 2.3.4.4 detected in Samara Oblast, Russian Federation. Front Vet Sci, 11 – 2024. [reference]
Grace, D., Knight-Jones, T. J., Melaku, A., Alders, R. & Jemberu, W. T. 2024. The Public Health Importance and Management of Infectious Poultry Diseases in Smallholder Systems in Africa. Foods, 13(3), 411. [reference]
Kenmoe, S., Takuissu, G.R., Ebogo-Belobo, J.T., Kengne-Ndé, C., Mbaga, D.S., Bowo-Ngandji, A. & Ondigui Ndzie, J.L. et al. 2024. A systematic review of influenza virus in water environments across human, poultry, and wild bird habitats. Water Res X, 22:100210. [reference]
Roberts, L.C., Abernethy, D., Roberts, D.G., Ludynia, K., O'Kennedy, M.M., Abolnik, C. 2023. Vaccination of African penguins (Spheniscus demersus) against high-pathogenicity avian influenza.Vet Rec, e3616. [reference]
Abolnik, C. 2023. Spillover of an endemic avian Influenza H6N2 chicken lineage to ostriches and reassortment with clade 2.3.4.4b H5N1 high pathogenicity viruses in chickens. Vet Res Commun. [reference]
Fagrach, A., Arbani, O., Karroute, O., El-Ftouhy, F.Z., Kichou, F., Bouslikhane, M., Fellahi, S. 2023. Prevalence of major infectious diseases in backyard chickens from rural markets in Morocco. Vet World, 16(9):1897-1906. [reference]
Meseko, C., Ameji, N.O., Kumar, B. & Culhane, M. 2023. Rational approach to vaccination against highly pathogenic avian influenza in Nigeria: a scientific perspective and global best practice. Arch Virol, 168(10):263. [reference]
Agha, A.S.K., Benlashehr, I., Naffati, K.M., Bshina, S.A. & Khashkhosha, A.A. 2023. Correlation of avian influenzaH9N2 with high mortality in broiler flocks in the southwest of Tripoli, Libya. Open Vet J, 13(6):715-722. [reference].
Bongono, E.F., Kaba, L., Camara, A., Touré, A., Ngoma, M.P., Yanogo, P.K., Kanyala, E. & SOW A. 2023. Évaluation de la biosécurité et facteurs associés à l'influenza aviaire dans les fermes avicoles de Coyah, Guinée, 2019-2020. Med Trop Sante Int. 2023 3(2):25. [reference].
Isibor, P.O., Onwaeze, O.O., Kayode-Edwards, I.I., Agbontaen, D.O., Ifebem-Ezima, A.M., Bilewu, O., Onuselogu, C., Akinniyi, A.P., Obafemi, Y.D. & Oniha, M.I. 2023. Investigating and combatting the key drivers of viral zoonoses in Africa: an analysis of eight epidemics. Braz J Biol, 84:e270857. [reference]
Lebarbenchon, C., Boucher, S., Feare, C., Dietrich, M., Larose, C., Humeau, L., Le Corre, M. & Jaeger, A. 2023. Migratory patterns of two major influenza virus host species on tropical islands. R Soc Open Sci, 10(10):230600. [reference]
Jbenyeni, A., Croville, G., Cazaban, C. & Guérin, J.L. 2023. Predominance of low pathogenic avian influenza virus H9N2 in the respiratory co-infections in broilers in Tunisia: a longitudinal field study, 2018-2020. Vet Res, 54(1):88. [reference]
Alhaji, N.B., Adeiza, A.M., Godwin, E.A., Haruna, A.E., Aliyu, M.B. & Odetokun, I.A. 2023. An assessment of the highly pathogenic avian influenza resurgence at human-poultry-environment interface in North-central Nigeria: Sociocultural determinants and One Health implications. One health, 16:100574 [reference]
Miller, LmNm, Elmselati, H., Fogarty, A.S., Farhat, M.E., Standley, C.J., Abuabaid, H.M. & Zorgani, A. 2023. Using One Health assessments to leverage endemic disease frameworks for emerging zoonotic disease threats in Libya. PLOS Glob Public Health, 3(7):e0002005 [reference]
Abolnik, C., Phiri, T., Peyrot, B., de Beer, R., Snyman, A., Roberts, D., Ludynia, K. et al. 2023. The Molecular Epidemiology of Clade 2.3.4.4B H5N1 High Pathogenicity Avian Influenza in Southern Africa, 2021–2022. Viruses, 15(6):1383. [reference]
Meseko, C., Milani, A., Inuwa, B., Chinyere, C., Shittu, I., Ahmed, J., Giussani, E. et al. 2023. The Evolution of Highly Pathogenic Avian Influenza A (H5) in Poultry in Nigeria, 2021–2022. Viruses,15:1387. [reference]
Nma Bida Alhaji, Abdulrahman Musa Adeiza, Enid Abutu Godwin, Aliyu Evuti Haruna, Mohammed Baba Aliyu and Ismail Ayoade Odetokun. 2023. An assessment of the highly pathogenic avian influenza resurgence at human-poultry-environment interface in North-central Nigeria: Sociocultural determinants and One Health implications. One Health, 16:100574. [reference]
Lo, F.T., Zecchin, B., Diallo, A.A., Racky, O., Tassoni, L., Diop, A., Diouf, M., Diouf, M., Samb, Y.N., Pastori, A., Gobbo, F., Ellero, F., Diop, M., Lo, M.M., Diouf, M.N., Fall, M., Ndiaye, A.A., Gaye, A.M., Badiane, M., Lo, M., Youm, B.N., Ndao, I., Niaga, M., Terregino, C., Diop, B., Ndiaye, Y., Angot, A., Seck, I., Niang, M., Soumare, B., Fusaro, A. & Monne, I. 2022. Intercontinental Spread of Eurasian Highly Pathogenic Avian Influenza A(H5N1) to Senegal. Emerg Infect Dis. 28(1):234-237. [reference]
Panzarin, V., Marciano, S., Fortin, A., Brian, I., D'Amico, V., Gobbo, F., Bonfante, F., Palumbo, E., Sakoda, Y., Le, K.T., Chum D.H., Shittu, I., Meseko, C., Haido, A.M., Odoom, T., Diouf, M.N., Djegui, F., Steensels, M., Terregino, C. & Monne, I. 2022. Redesign and Validation of a Real-Time RT-PCR to Improve Surveillance for Avian Influenza Viruses of the H9 Subtype. Viruses. 14(6):1263. [reference]
L'appui de la FAO aux pays ou par pays
Niveau Global
- OFFLU, le Réseau d'expertise de l'OMSA/FAO sur la grippe animale, a tenu une réunion technique mondiale du 2 au 4 juillet à la FAO à Rome.
- La FAO et l'OMSA ont lancé la Stratégie mondiale de prévention et de contrôle de la grippe aviaire hautement pathogène (2024-2033) dans le cadre mondial pour le contrôle progressif des maladies animales transfrontalières (GF-TADs) [lien] le 27 mai 2024 en marge de la session Générale annuelle de l’OMSA.
- OFFLU a organisé un webinaire "OFFLU Avian Influenza Matching (AIM) pour les vaccins pour la volaille" le 10 juillet.
- Le Centre Virtuel d'Apprentissage de la FAO a récemment lancé un nouveau cours d'auto-apprentissage en ligne portant sur la grippe aviaire (GA). L'objectif du cours est de sensibiliser aux enjeux de la GA et de développer les compétences nécessaires pour sa détection et sa prévention. Vous pouvez accéder au cours en suivant ce lien. Ce cours introductif a été conçu pour divers intervenants manifestant un intérêt pour la GA, et il s'adresse notamment aux vétérinaires, aux paraprofessionnels vétérinaires, ainsi qu'à toute personne travaillant dans le secteur avicole. Il se compose de six modules, chacun d'une durée d'environ quinze à vingt minutes. Vous avez la flexibilité d'y accéder à tout moment selon votre convenance, et de les utiliser comme ressource en fonction de vos besoins. Le cours est compatible avec plusieurs plateformes et peut être suivi aussi bien sur un smartphone que sur un ordinateur ou une tablette. Le cours est maintenant aussi disponible en espagnol et en portugais.
Niveau Régional
- Un atelier interrégional sur la biosécurité et la biosécurité pour les laboratoires vétérinaires - l’Afrique de l’Est et du Sud et de l’Afrique de l’Ouest et Centrale sera organisé conjointement par les bureaux régionaux du Centre d’urgence de la FAO pour la lutte contre les maladies animales transfrontalières (ECTAD) en Afrique de l’Est et australe (ESA) et en Afrique de l’Ouest et du Centre (AOC), à Lusaka, en Zambie, pendant la troisième semaine de juillet.
- Du 11 au 14 juin 2024, se tiendra, à Ada au Ghana, un atelier sur la planification, la coordination, et le renforcement des capacités pour la prévention, la préparation, et la réponse rapide en matière de santé animale dans la région africaine.
- La FAO ECTAD AOC suit les foyers suspects d'influenza aviaire hautement pathogène dans plusieurs pays de la région et fournit diverses aides, notamment des réactifs et des consommables de laboratoire, ainsi que le transport des échantillons vers le laboratoire de référence Istituto Zooprofilattico Sperimentale delle Venezie (IZSVe-Italie) pour la confirmation et le séquençage.
- En Afrique de l'Ouest, ECTAD AOC de la FAO a soutenu des études sur la chaîne de valeur de la volaille et l'élaboration de manuels de biosécurité pour les élevages de volailles et les marchés d'oiseaux vivants au Togo et au Bénin, dans le cadre du projet financé par l'USAID intitulé “Assistance d'urgence pour la prévention et le contrôle de la grippe aviaire hautement pathogène (IAHP) dans les pays choisis d'Afrique”.
- Les bureaux régionaux de la FAO ECTAD AOA soutiennent l'achat de réactifs (amorces, sondes, kits de réaction en chaîne par polymérase (PCR), kits d'extraction) et de consommables pour soutenir les tests de diagnostic en temps opportun et pour améliorer la préparation en Éthiopie, au Kenya, la République-Unie de Tanzanie et l'Ouganda à travers programme de sécurité sanitaire mondiale (GHS) financé par l'USAID.
- ECTAD AOA soutient le Kenya, l'Éthiopie, la République-Unie de Tanzanie, la Zambie et le Zimbabwe pour améliorer la biosécurité dans les élevages de volailles ; ce qui contribue à minimiser l'incursion de l'IAHP. Une évaluation des risques liés à la chaîne de valeur tout au long de la chaîne de valeur de la volaille est prévue dans 10 pays, à savoir l'Éthiopie, le Kenya, Madagascar, le Malawi, le Mozambique, le Rwanda, le Soudan du Sud, la République-Unie de Tanzanie, l'Ouganda et la Zambie, dans le cadre du soutien continu d'ECTAD pour l’atténuation/gestion des risques liés à l'IAHP.
- Le centre d'apprentissage virtuel (CAV) en Afrique de l'Ouest propose un cours tutoré de quatre semaines sur l'influenza aviaire en anglais et en français.
- Une formation régionale sur le Transport des substances infectieuses selon la réglementation de l'Association du transport aérien international (IATA) pour l'Afrique de l'Est et Australe 'est déroulée à Nairobi en juin 2024.Cette même formation est prévue, en français à Dakar, et en anglais à Accra en août 2024.
Niveau National
Benin:
- Une étude de la chaîne de valeur de la volaille a été menée, aboutissant à l'élaboration d'un manuel de biosécurité visant à renforcer les mesures de biosécurité dans les exploitations avicoles et les marchés d'oiseaux vivants. Les rapports intitulés "Étude des chaînes de valeur de la volaille et des facteurs de risque de l'IAHP au Bénin" ont été finalisés.
- Une formation de formateurs sur les mesures de biosécurité et les bonnes pratiques en matière de gestion des exploitations avicoles a été réalisée, en utilisant à la fois le Manuel de biosécurité dans les élevages avicoles commerciaux et le Manuel de biosécurité dans les marchés de volailles vivantes au Bénin.
- La FAO ECTAD a soutenu la Benin en fournissant des réactifs, des désinfectants et des équipements de protection individuelle (EPI) et à l’envoi des échantillons à IZSVe (Padova, Italie) pour séquençage de confirmation.
Burkina Faso:
- Les échantillons prélevés en mars 2024 ont été analysés à l'IZSVe; les résultats ont montré que les quatre virus isolés appartenaient au virus de l’IAHP (H5N1) de clade 2.3.4.4b; ces virus se regroupent dans une longue branche phylogénétique, ce qui suggère que ces virus ont pu circuler; et sont apparentés aux virus de l’IAHP (H5N1) du Nigeria (2021-2022) et du Niger (2022-2023), mais ne se regroupent pas avec les isolats du Burkina de 2021, ce qui suggère l'introduction d'un virus distinct.
Côte d’Ivoire:
- Avec l'appui de la FAO, la surveillance de l'IAHP est menée par le Département des Services Vétérinaires et le Laboratoire National d'Appui au Développement Agricole (LANADA), en collaboration avec l'Institut Pasteur de Côte d'Ivoire et l'Office Ivoirien des Parcs et Réserves dans le cadre de l'approche Une Seule Santé, afin d'évaluer la situation de l'influenza aviaire.
Éthiopie:
- Pour prévenir l'incidence et la propagation des principales maladies aviaires dans une ferme avicole, la FAO ECTAD Éthiopie, soutenue par le Fleming Fund, met en place actuellement des Écoles Pratiques Fermiers de Poulets de Chair (FFS) dans cinq sites. L´approche holistique intégrera les principes de base de la biosécurité, la prévention des maladies et la réduction de l'utilisation des antimicrobiens. Pour les producteurs volontaires des écoles d'élevage de poulets de chair, une production avicole saine, l'amélioration de la production et de la productivité ont été identifiées comme des sujets clés. Une évaluation de base a été réalisée pour évaluer le contexte de l'exploitation et le statut de la mise en œuvre de la biosécurité, la transmission des maladies, et pour collecter des données économiques de base sur l'exploitation à l'aide de l'outil Kobo dans le cadre de l'école d'élevage de poulets de chair. Il s'agit d'une partie de l'étude/expérimentation du FFS pour les élevages de poulets de chair visant à prévenir/réduire les principales maladies des volailles ayant un impact sur l'économie et la santé publique, et donc à réduire le besoin d'antimicrobiens et à améliorer la productivité.
Gambie:
- Le Département des Services d'Élevage, en collaboration avec la FAO, a mené une campagne nationale de sensibilisation et d'information publique. La campagne sensibilise les communautés rurales sur la IAHP, la nécessité de signaler les incidents suspects, et les mesures de biosécurité essentielles pour protéger la santé publique, améliorer la production avicole et protéger les moyens de subsistance.
Gabon:
- Le Gabon a rapporté la détection du virus de la grippe aviaire hautement pathogène H5N1 dans seulement 2 échantillons sur les 26 collectés chez des poules pondeuses dans un marché aux volailles vivantes, sans mortalité associée au moment de l'échantillonnage.
Ghana:
- L'initiative PMP-TAB de la FAO est mise en œuvre pour préserver la santé des volailles et assurer la durabilité de l'industrie grâce à des efforts de biosécurité qui répondent à des besoins spécifiques.
Kenya:
- FAO - ECTAD, à travers le Programme de Sécurité Sanitaire Mondiale, soutient la Direction des Services Vétérinaires du Kenya, en collaborant sur les actions de biosécurité et de sûreté biologique à travers le développement, a la révision et à la validation du Manuel de Biosécurité et des Lignes Directrices Nationales de Gestion des Déchets Vétérinaires. Concernant cette initiative, un événement sponsorisé par le gouvernement kenyan a annoncé un atelier sur "La protection des secteurs biotechnologiques et biochimiques du Kenya par le renforcement des pratiques de biosécurité", prévu du 20 au 21 août 2024 à Nairobi.
- La FAO soutient le déploiement de la plateforme de notification des maladies biosurveillance animale du Kenya (KABS) pour la surveillance syndromique et les formations de recyclage.
Liberia:
- Le ministère de l’Agriculture, en collaboration avec la FAO, prévoit de mener une surveillance active de l'influenza aviaire à faible pathogénicité (LPAI)/IAHP dans cinq comtés à haut risque (Montserrado, Nimba, Grand Cape Mount, Bomi, Grand Bassa) du 1er au 7 juillet 2024. L'enquête a ciblé les volailles des fermes commerciales et celles traditionnelles en liberté (poulets, pintades, canards), avec 173 écouvillons cloacaux et de frottis nasaux collectés et testés, mais tous ont été négatifs au kit de test rapide AIV Anigen (Bionote).
- Des réactifs de laboratoire, pour le diagnostic de la grippe aviaire et de la maladie de Newcastle, sont en cours d'acquisition dans le cadre du programme GHS d'ECTAD.
- Les agents de l'élevage en charge de la surveillance seront formés sur la surveillance et sur l’identification des maladies animales (juillet 2024).
- La formation d'une nouvelle promotion d'Agents Communautaires de Santé Animale (ACSA) est prévue en juillet 2024 afin de renforcer la surveillance au niveau local. La formation donnera la priorité à la détection des maladies (y compris le signalement de rumeurs) au niveau communautaire pour les maladies zoonotiques prioritaires (MZP), y compris la grippe aviaire.
- Diverses formations sont prévues, notamment : une formation de formateurs pour les techniciens de santé animale sur les lignes directrices en matière de biosécurité et de sûreté biologique ; une formation des acteurs de la chaîne de valeur de la viande sur les pratiques sanitaires et hygiéniques pour la sécurité alimentaire. Les mentors et formateurs recevront une instruction dans le cadre du programme de formation en épidémiologie vétérinaire appliquée de terrain (ISAVET).
Mali:
- FAO ECTAD Mali a mené une étude sur la biosécurité dans les élevages de volailles, de produits laitiers et de porcs afin d'évaluer les meilleures pratiques et de recommander des actions pour améliorer les mesures de biosécurité dans les exploitations. À la suite des recommandations de l'étude, une formation de 50 personnes a été réalisée en décembre 2023 et une autre est programmée en juillet 2024 au profit des acteurs communautaires (femmes et jeunes) travaillant dans les élevages avicoles, laitiers et porcins.
- Une formation de 25 acteurs communautaires, portant sur la définition des cas et de notification des maladies zoonotiques prioritaire, a été réalisée du 21 au 22 mai 2024 à Ségou. L'objectif était de susciter la prise en compte de ces maladies dans le système national de surveillance des maladies animales et zoonotiques.
- Une formation de 26 personnes (vétérinaires centraux, régionaux et privés ainsi que les cadres des laboratoires et des agents en charge de la faune sauvage) a été organisée du 28 au 30 mai 2024 à Bougouni. Cette formation a porté sur les bonnes pratiques de gestion des urgences de santé animale (GEMP). L'objectif de la formation était d’outiller les participants à la bonne préparation et gestion des urgences sanitaires.
Niger:
- Un foyer d'influenza aviaire hautement pathogène à H5N1 a été confirmé le 13 mai 2024 par le Laboratoire Central de l'Élevage (LABOCEL) suite à des mortalités observées sur un lot de 22 pintades à Aguié, dans la région de Maradi. Le reste de l'effectif a été abattu après la confirmation de la maladie qui s'est déclarée après l'introduction de nouveaux sujets venus d'un pays voisin. Un arrêté portant déclaration d'infection a été pris le 15 mai.
- Suite à une requête de la Direction générale des Services vétérinaires, la FAO-ECTAD a appuyé une mission d'investigation, conduite du 22 au 25 mai 2024, et composée d'une équipe centrale et d'une équipe OH régionale. La mission s'est déroulée en quatre étapes : i) visite du foyer, ii) visite d'un marché de volailles vivantes (Gazaoua), iii) visite du poste d'inspection frontalier le plus proche (Guidan Kané) et iv) synthèse et élaboration d'un plan de surveillance renforcée de l'influenza aviaire dans la région de Maradi. Des désinfectants (virucide, chaux vive, eau de javel), un pulvérisateur à dos d'une capacité de 16 litres, des gants, du matériel de prélèvement (tubes EDTA, tubes secs, pots) issus d'un stock offert par la FAO-ECTAD à la DGSV et une trousse chirurgicale pour la nécropsie, ont été remis à la Direction Départementale de l'Elevage d'Aguié pour aider à la gestion d'éventuels nouveaux foyers.
Nigeria:
- La FAO ECTAD, en collaboration avec le Ministère fédéral de l'Agriculture et de la Sécurité alimentaire, prévoit un atelier national des parties prenantes sur le contrôle et la prévention de la GAHP.
- La FAO ECTAD a soutenu l'élaboration et la validation des guides bonnes pratiques en matière de biosécurité pour la chaîne de valeur avicole.
Sierra Leone:
- Du 21 au 27 avril 2024, la FAO ECTAD, en collaboration avec les Ministères dans le cadre de l'approche Une Seule Santé (ministère de l'Agriculture et de la Sécurité Alimentaire, ministère de la Santé et ministère de l'Environnement et du Changement Climatique), les universités et avec le soutien de l'USAID dans le cadre du programme GHS, a mis en place une surveillance active de la grippe aviaire dans les districts de Bonthe et Pujehun en Sierra Leone afin de préserver la santé publique et la sécurité alimentaire. Ces deux districts sont considérés comme présentant un risque élevé d'influenza aviaire hautement pathogène parce qu'ils sont situés le long de la route des oiseaux sauvages migrateurs (la voie de migration des oiseaux sauvages de l'Atlantique Est), de l'Asie à l'Afrique du Sud en passant par l'Europe. Au cours de cette activité, 114 sérums de poulet et des oiseaux sauvages collectés ont été testés négatifs pour H5, H7 et H9 par ELISA et inhibition de l'hémagglutination.
Soudan du Sud:
- La FAO, à travers le Programme de Sécurité Sanitaire Mondiale, prévoit de former 520 ACSA sur la déclaration des maladies, la surveillance communautaire et d'améliorer leurs capacités en matière de déclaration en temps opportun et de système d'alerte précoce, de détection des MZP, y compris les maladies aviaires, en particulier dans les zones difficiles d'accès.
- En mars 2024, la FAO ECTAD, dans le cadre du Programme GHS, a réalisé l'évaluation du Laboratoire Vétérinaire Central (LVC) de Juba en utilisant l'outil de cartographie des laboratoires (LMT) de la FAO et FAO LMT - évaluation de la sécurité pour évaluer la fonctionnalité, la sécurité et les aspects de biosécurité du laboratoire, et identifier les lacunes et les priorités en matière d'amélioration. À la suite de l'évaluation, des recommandations, à court et à moyen termes, ont été formulées pour répondre aux lacunes et aux domaines d'amélioration identifiés. La FAO du Soudan du Sud soutient le LVC de Juba pour renforcer sa fonctionnalité dans le test des MZP, telles que la GAHP.
- La FAO, en collaboration avec la Fondation Africaine pour la Médecine et la Recherche (AMREF), a formé 32 techniciens de laboratoire en santé unique sur la gestion des risques biologiques pour une durée de 5 jours.
Liens importants
- FAO-OMSA Stratégie mondiale de prévention et de contrôle de la grippe aviaire hautement pathogène (2024-2033)
- FAO Consultation technique mondiale sur le cadre stratégique pour l'alerte précoce en cas de menaces pour la santé animale
- FAO-OMS-OMSA Évaluation préliminaire conjointe de la FAO/OMS/OMSA des récents virus de l'influenza A(H5N1)
- USDA Détections de l'Influenza Aviaire Hautement Pathogène (IAHP) chez le Bétail
- OMS Influenza Aviaire A (H5N1) - États-Unis d'Amérique
- OMSA Influenza Aviaire Hautement Pathogène chez les Bovins
- FAO Rester Vigilant contre l'Influenza Aviaire Hautement Pathogène A(H5N1)
- CDC Update technique: Résumé de l'analyse génétique des séquences des virus de l'Influenza Aviaire Hautement Pathogène A(H5N1) au Texas
- CDC Comment le CDC surveille les données relatives à la grippe chez les personnes afin de mieux comprendre la situation actuelle de la grippe aviaire A (H5N1)
- La liste des espèces d'oiseaux sauvages et de mammifères infectés par l'IAHP H5Nx [lien]
- Groupe de travail scientifique sur la grippe aviaire et les oiseaux sauvages H5N1 Grippe aviaire hautement pathogène chez les oiseaux sauvages - Impacts sans précédent sur la conservation et besoins urgents
- EFSA Aperçu de l’influenza aviaire mars-juillet 2024
- EFSA Rapports de synthèse sur l'influenza aviaire [lien]
- OMS Évaluation du risque associé aux virus récents de la grippe A(H5N1) du clade 2.3.4.4b
- OMS Documentations relatives aux consultations de la composition du vaccin antigrippal (du 2011 à ce jour)
- WOAH Défis stratégiques afférents au contrôle mondial de l’influenza aviaire de haute pathogénicité [lien]
- OFFLU Le site de l’OFFLU
- OFFLU Détections d'IAHP dans le bétail page
- OFFLU Avian influenza matching (OFFLU-AIM) report
- OFFLU L’ensemble de données aviaires pour le VCM - février 2023 à septembre 2023
- OFFLU Rapports de synthèse de la contribution de l'OFFLU à la VCM de l'OMS (2013-2023)
- ECOWAS, FAO, USAID Rapport de la réunion consultative régionale la prévention et le contrôle de l'influenza aviaire hautement pathogène en Afrique de l'Ouest
- Rapports de synthèse de la contribution de l'OFFLU à la VCM de l'OMS (2013-2023)
- FAO-OMS-OMSA Un guide tripartite pour la gestion des zoonoses
- FAO-OMS-OMSA Tripartite outil opérationnel d'évaluation conjointe des risques (JRA OT)
- FAO-OMS-OMSA Les foyers permanents de grippe aviaire chez les animaux représentent un risque pour l'homme - Analyse de la situation et conseils aux pays par la FAO, l'OMS et le WOAH
- FAO Rapport de la consultation globale sur l'influenza aviaire hautement pathogène
- FAO Manuel de gestion des opérations en cas de situation d’urgence zoosanitaire
- FAO Méthode de bonne gestion des urgences : les fondamentaux : Guide de préparation aux urgences de santé animale la troisième édition
- FAO Directives relatives à la gestion des carcasses : Élimination efficace des carcasses animales et des matières contaminées dans les exploitations de petite à moyenne taille
- FAO Protocoles d'analyse en laboratoire vétérinaire pour les zoonoses prioritaires en Afrique
- FAO Principes directeurs pour la conception de la surveillance active de l'influenza aviaire en Asie : Conception d'une surveillance active, globale et basée sur les risques de l'influenza aviaire
- FAO Webinar Gestion des foyers d’influenza aviaire hautement pathogène (IAHP) à grande échelle chez les oiseaux sauvages [PARTIE 1] et [PARTIE 2]
- FAO Analyse de Risque Qualitative traitant de la propagation du virus Influenza Aviaire Hautement Pathogène H5N1 en Afrique centrale.
- Focus sur «La propagation de l’influenza aviaire hautement pathogène H5N8 (IAHP) en Afrique subsaharienne au cours de la période 2016-2018 : observations épidémiologiques et écologiques».
- Focus sur «La grippe aviaire hautement pathogène H5 en 2016 et 2017 - Observations et perspectives».
ECTAD AES
- Bien qu'aucun événement d'IAHP n'ait été signalé dans la région, la FAO-ECTAD continue de soutenir les programmes annuels de tests d'aptitude pour les AIV depuis 2018 par le biais du programme GHSA finance par l'USAID au niveau national et sous-national en Afrique de l'Est (Éthiopie, Kenya, Tanzanie et Ouganda) et de soutenir l'achat de réactifs (fournitures moléculaires - amorces, sondes, kits PCR, kits d'extraction) et de consommables pour soutenir les tests de diagnostic et améliorer la préparation.
ECTAD AOC
- En Afrique de l'Ouest, la FAO ECTAD-AOC a organisé une formation régionale sur l'expédition de substances infectieuses du 26 au 28 juillet 2023 avec un formateur de l'OMS. Un total de 11 stagiaires de 7 pays francophones ont terminé avec succès leur formation et ont été certifiés pour expédier des matières infectieuses par voie aérienne.
- FAO ECTAD AOC a aidé le Bénin, la Côte d'Ivoire, le Ghana, la Guinée, le Mali, le Niger, le Nigeria, le Sénégal et le Togo à gérer la mortalité des volailles et des oiseaux sauvages en 2022 dus à l'IAHP H5, y compris la fourniture de réactifs et consommables de laboratoire et d'EPI pour les activités de terrain, ainsi que les pays à risque pour faire face à la situation dans le cadre d'une coordination régionale en 2022.
- En 2023, avec le lancement d'un projet régional OSRO/GLO/501/USA " Aide d'urgence pour la prévention et le contrôle de l'influenza aviaire hautement pathogène (IAHP) dans certains pays d'Afrique de l'Ouest" financé par l'USAID notamment pour renforcer les capacités des services vétérinaires et la prévention et le contrôle de l’IAHP au Benin, en Gambie et au Togo dans la région de l'Afrique de l'Ouest.
- FAO ECTAD WCA conducted backstopping missions: to Benin and Togo in from 9 to 13 May 2023 to provide follow up support also for the implementation of the HPAI project, assessed the readiness, reviewed planned activities, visited the veterinary laboratory of Lomé and provided recommendations to improve biosafety/biosecurity measures and working environment; and to the Gambia from 22 to 26 May 2023 to provide technical support in the HPAI project implementation, reviewed additional response needs for the recent HPAI outbreak and handed over emergency supplies (rapid test kits, disinfectants, personal protective equipment [PPE]) from the USAID funded Stockpile Project to the Department of Livestock Services of the Ministry of Agriculture.
Burkina Faso:
- Du 25 au 27 juin 2023, une réunion s'est tenue à Koudougou pour sensibiliser les petits éleveurs de volailles à la reconnaissance des maladies et à leur responsabilité dans la détection précoce de la mortalité. Quarante-cinq producteurs de volailles ont participé à la session. Avant la réunion, une formation technique a été organisée et destinée aux agents vétérinaires de terrain qui répercuteront la formation dans leurs régions respectives. L'objectif est de sensibiliser 650 éleveurs de volailles à l'IAHP et à la biosécurité.
- Le projet TCP/BKF/3901 a permis de former 175 personnes à la surveillance épidémiologique de l'IAHP; il a développé des modules de formation sur les bonnes pratiques d'élevage de volailles, les mesures d'hygiène et de biosécurité dans les fermes et a formé 46 formateurs; les formateurs ont sensibilisé 300 éleveurs de volailles modèles de 10 régions du Burkina. Le projet a également permis de former 30 communicateurs et journalistes de la presse écrite et audiovisuelle sur l'IAHP.
Ethiopia:
- Les maladies dues à l'absence ou au manque de biosécurité représentent plus de 56 % de la mortalité annuelle dans le secteur avicole en Éthiopie, ce qui décourage les éleveurs d'accroître leur production. La FAO, en collaboration avec l'Institut éthiopien de recherche agricole, a préparé une brochure sur la biosécurité couvrant trois domaines clés : les mesures de biosécurité conceptuelles, structurelles et opérationnelles. La brochure fournit des conseils aux petites et moyennes exploitations avicoles commerciales sur la mise en œuvre de mesures de biosécurité efficaces pour une productivité accrue et une industrie plus durable et plus rentable, et est destinée à être utilisée par les écoles d'agriculture de terrain (Farmers Field School - FFS).
Gabon:
- Une mission de terrain d'urgence le Centre de gestion des urgences de la FAO (FAO-EMC) a été menée au Gabon du 4 au 8 juillet 2022 en réponse aux récents foyers d'IAHP H5N1 signalés dans la province de l'Estuaire. L'équipe FAO-EMC a collaboré avec la Direction générale de l'élevage pour enquêter sur les exploitations touchées, évaluer la capacité d'intervention d'urgence, identifier les lacunes actuelles du système de surveillance de la santé animale, y compris la capacité du Laboratoire Central Vétérinaire de Libreville pour le diagnostic des maladies prioritaires et élaborer des recommandations sur mesure. L'épidémie a été contrôlée et aucun foyer additionnel n'a été signalé depuis la mi-mai 2022.
Ghana:
- FAO, en collaboration avec l'USAID, a organisé un atelier de sensibilisation d'une journée dans trois régions du Ghana (Ashanti, Bono et Bono East) en janvier 2023 pour prévenir les zoonoses résultant de la manipulation, du commerce et de la consommation de viande de brousse [lien]
Liberia:
- En décembre 2022, FAO-ECTAD Liberia a aidé le ministère de l'agriculture à enquêter sur les foyers présumés d'IAHP à Nimba; tous les échantillons se sont révélés négatifs pour l'IAHP.
Mali:
- En 2022, la FAO ECTAD Mali a appuyé le renforcement des pratiques de biosécurité au niveau des exploitations agricoles en ciblant 35 agriculteurs dont 8 femmes.
Niger:
- La FAO ECTAD-Niger a soutenu l'élaboration d'un guide de biosécurité (2022) pour les acteurs des chaînes de valeur du lait, de la viande et de la volaille au Niger.
Nigeria:
- La FAO ECTAD-Nigeria, en collaboration avec la CEDEAO et l'UA-BIRA, a soutenu l'évaluation du risque de propagation de l'IAHP dans le pays en avril 2023.
Senegal:
- La mission d'experts de la FAO EMC-AH s'est rendue à Saint-Louis dans le cadre du soutien à la lutte contre les foyers d'influenza aviaire hautement pathogène en mai 2023. Une session de débriefing et une revue après action (AAR) sur le SOP utilisé pour la mission ont été organisées virtuellement le 26 mai et le 24 juillet respectivement, à laquelle ont participé le coordinateur national et l'expert en épi de l'ECTAD Sénégal.
- En janvier et février 2023, la FAO a formé 32 agents (25 du ministère de l'Environnement, du Développement Durable et de la Transition Ecologique et 7 du ministère de l'Elevage et de la Production Animale) sur les techniques d'échantillonnage des oiseaux sauvages.
Sierra Leone:
- En 2022, lorsque la Guinée voisine a signalé des foyers d'IAHP, la FAO ECTAD Sierra Leone a soutenu le ministère de l'agriculture et de la sécurité alimentaire pour entreprendre une recherche active de l'IAHP dans les districts de Koinadugu, Karene, Pujehun et Kambia adjacents aux zones infectées/à haut risque en Guinée. 161 échantillons (sérum et écouvillons) ont été collectés et testés au laboratoire vétérinaire central à l'aide de la méthode ELISA et de la PCR. Tous les échantillons se sont révélés négatifs pour le H5. En collaboration avec la FAO ECTAD Guinée, la FAO ECTAD Sierra Leone a fourni des informations actualisées sur la situation de l'IAHP en Guinée lors des réunions hebdomadaires du Groupe de préparation et de réaction aux urgences d’une seule santé, ce qui a aidé le gouvernement à suivre l'évolution du foyer et à évaluer les menaces potentielles d'introduction de l'IAHP en Sierra Leone. Ce soutien a complété les efforts du gouvernement pour prévenir les incursions de l'IAHP dans le pays.
8 août 2024
Avertissement
Les informations fournies dans le présent document sont à jour à la date de publication. Les informations ajoutées ou modifiées, depuis la dernière mise à jour de la situation de l'IAHP en Afrique subsaharienne, apparaissent en orange. Pour les cas de volailles dont les dates d’apparition sont inconnues, les dates de déclaration ont été utilisées à la place. La FAO compile les informations communiquées par les agents sur le terrain dans les pays touchés, par les bureaux régionaux et par l'Organisation mondiale de la santé animale [WOAH], ainsi que des articles scientifiques évalués par des pairs. La FAO s'efforce d'assurer, mais ne garantit pas l'exactitude, l'exhaustivité ou l'authenticité des informations. Les limites et les noms indiqués, ainsi que les désignations utilisées sur ces cartes, n'impliquent l'expression d'aucune opinion de la part de la FAO concernant le statut juridique de tout pays, territoire, ville ou zone ou de ses autorités, ou concernant la délimitation de ses frontières et limites. Les lignes pointillées sur les cartes représentent des frontières approximatives pour lesquelles il n’y a peut-être pas encore d’accord total.
Contact
Pour un bilan des cas d’IAHP H5N1, H5N6 et H5N8 déclarés par les pays d’Afrique subsaharienne avant la vague actuelle (i.e. avant le 1er octobre 2021), veuillez contacter EMPRES-Animal Health
